
����Ŀ���ڻ�ƿ�м��롰�ʻ����ʼ��������ӳ��ʻ����������±���ijͬѧ���Ƶ�500mL���ʻ����ʼ����к��еijɷ֣��Ķ���ش��������⣺
�ɷ� | ���� | ����� | ��˾ƥ�� | ������� | ������ |
������g�� | 25.00 | 0.174 | 0.17 | 0.316 | 0.340 |
��1�����С��ʻ����ʼ����ijɷ��У����ڷǵ���ʵ����� �� ��
A.����
B.�����
C.�������
D.������
��2�����ʻ����ʼ�����K+����˾ƥ���в���K+�������ʵ���Ũ��Ϊ mol/L��
��3�������������ʻ����ʼ�������������У�������ƽ��ҩ�ס��ձ�����Ͳ������������ �� ���ں�������д��ȱ���������ƣ�
��4������Һ���ƹ����У����в��������ƽ��û��Ӱ������� �� ��
A.����ʱ��������ƿ�̶���
B.����ƿ��ʹ��ǰδ�����������������ˮ
C.ת�ƺ�ϴ���ձ�2��3�Σ�����ϴ��Һ��������ƿ��
D.����ҡ�Ⱥ���Һ���������ƿ�Ŀ̶��ߣ���δ���κδ�����
���𰸡�
��1��A
��2��0.008
��3����ͷ�ι�,500mL����ƿ
��4��B,C,D
���������⣺��1��A��������ˮ��Һ�к�����״̬�¶�������Ļ��������ڷǵ���ʣ�
B���������ˮ��Һ�л�������״̬���ܹ�����Ļ��������ڵ����
C�����������ˮ��Һ�л�������״̬���ܹ�����Ļ��������ڵ���ʣ�
D����������ˮ��Һ�л�������״̬���ܹ�����Ļ��������ڵ���ʣ�
�ʴ�Ϊ��A��
��2��n��K+��=n��KMnO4��+2n��K2SO4��= ![]() +2��
+2�� ![]() =0.004mol��
=0.004mol��
��C��K+��= ![]() =0.008mol/L��
=0.008mol/L��
�ʴ�Ϊ��0.008��
��3������һ�����ʵ���Ũ����Һ��һ�㲽�裺���㡢�������ܽ⡢��ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȡ�װƿ���õ��������У�������ƽ��ҩ�ס��ձ�����Ͳ����������500ml����ƿ����ͷ�ιܣ����Ի�ȱ�ٵ�������500ml����ƿ����ͷ�ιܣ�
�ʴ�Ϊ��500ml����ƿ����ͷ�ιܣ�
��4��A������ʱ��������ƿ�̶��ߣ�������Һ���ƫС����ҺŨ��ƫ�ߣ���A��ѡ��
B������ƿ��ʹ��ǰδ�����������������ˮ�������ʵ����ʵ�������Һ�����������Ӱ�죬��ҺŨ�Ȳ���Ӱ�죬��Bѡ��
C��ת�ƺ�ϴ���ձ�2��3�Σ�����ϴ��Һ��������ƿ�У�������ȷ����ҺŨ��ȷ����C��ȷ��
D������ҡ�Ⱥ���Һ���������ƿ�Ŀ̶��ߣ�����Ϊ������Һմ������ƿƿ���ϣ�������ȷ����������Ҫ��������ҺŨ��ȷ����D��ȷ��
�ʴ�Ϊ��BCD��
��1�����ݵ���ʡ��ǵ���ʵĸ�������жϣ�
��2��K+���Ը�����ء�����صĵ��룬���ݼ������غ��֪n��K+��=n��KMnO4��+2n��K2SO4�����ٸ������ʵ���Ũ�ȶ��������������ʵ���Ũ�ȣ�
��3����������һ�����ʵ���Ũ����Һ��һ�㲽��ѡ����Ҫ��������
��4���������������ʵ����ʵ���n����Һ���V��Ӱ�죬�������ʵ���Ũ�ȶ������������������ʹnƫ�����ʹVƫС�IJ�������ҺŨ�ȶ�ƫ�ߣ�������ҺŨ��ƫ��.



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() U����Ҫ�ĺ˹�ҵԭ�ϣ�����Ȼ��Ĵ��ں��٣���Ũ��һֱΪ��������ע�������й�
U����Ҫ�ĺ˹�ҵԭ�ϣ�����Ȼ��Ĵ��ں��٣���Ũ��һֱΪ��������ע�������й� ![]() U˵����ȷ���ǣ�������
U˵����ȷ���ǣ�������
A.![]() Uԭ�Ӻ��к���92������
Uԭ�Ӻ��к���92������
B.![]() Uԭ�Ӻ�����143������
Uԭ�Ӻ�����143������
C.![]() U��
U�� ![]() U��Ϊͬλ��
U��Ϊͬλ��
D.![]() U��
U�� ![]() U��Ϊͬ��������
U��Ϊͬ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йص����仯����˵����ȷ����
A. ʵ����������Ƭ��ϡ�����ϡ���ᷴӦ��ȡH2
B. ����Һ�����������������
C. �������ſ������ռ�ͭ����ϡ���ᷴӦ������NO
D. �����£�N2������O2��Ӧ��������H2��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������OH��������ͬ�������͵��������ǣ� ��
A.Na+
B.NH4+
C.Ne
D.F��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ũ����ķ�ӦΪ3H2S��H2SO4=4S����4H2O������˵����ȷ����( )
A. �������屻��������B. ���ᱻ��������
C. ���ᱻ��ԭ��ˮD. �������屻��ԭ��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���200mLij���������Ļ����Һ�ֳ����ȷ֣�һ�ݼ������BaCl2��Һ����ַ�Ӧ��ó���4.66g����һ�ݼ���100mL2.0molL��1NaOH��Һ����ַ�Ӧ����Һ������������Ũ��Ϊ0.2molL��1����Һ�����Ϊ200mL�����Լ��㣺ԭ�����Һ����������ʵ���Ũ��ΪmolL��1 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����14�֣���ϩ��һ����Ҫ�Ļ���ԭ�ϣ����ɶ���������Ʊ����ش��������⣺
��1�������飨C4H10��������1-��ϩ��C4H8�����Ȼ�ѧ����ʽ���£� ��C4H10(g)= C4H8(g)+H2(g) ��H1
��֪����C4H10(g)+ ![]() O2(g)= C4H8(g)+H2O(g) ��H2=-119 kJ��mol-1
O2(g)= C4H8(g)+H2O(g) ��H2=-119 kJ��mol-1
��H2(g)+ ![]() O2(g)= H2O(g) ��H3-242kJ��mol-1
O2(g)= H2O(g) ��H3-242kJ��mol-1
��Ӧ�ٵĦ�H1Ϊ kJ��mol-1��ͼ��a���Ƿ�Ӧ��ƽ��ת�����뷴Ӧ�¶ȼ�ѹǿ�Ĺ�ϵͼ��x0.1������ڡ���С�ڡ�������ʹ��ϩ��ƽ�������ߣ�Ӧ��ȡ�Ĵ�ʩ�������ţ���
A.�����¶� B.�����¶� C.����ѹǿ D.����ѹǿ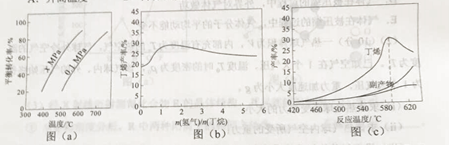
��2������������Ļ��������һ������ͨ������д����ķ�Ӧ���������������ǻ���������������к��ж�ϩ�����顢�����ȡ�ͼ��b��Ϊ��ϩ�������������n��������/n�����飩�Ĺ�ϵ��ͼ�����߳��������ߺ͵ı仯���ƣ��併�͵�ԭ������
��3��ͼ��c��Ϊ��Ӧ���ʺͷ�Ӧ�¶ȵĹ�ϵ���ߣ���������Ҫ�Ǹ����ѽ����ɵĶ�̼����������ϩ������590��֮ǰ���¶����߶������ԭ�����������590��֮��ϩ���ʿ��ٽ��͵���Ҫԭ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£�ͨ�����з�Ӧ��ʵ��ȼú��������Ļ��գ�
SO2��g��+2CO��g�� ![]() 2CO2��g��+S��s��
2CO2��g��+S��s��
����Ӧ�ں��ݵ��ܱ������н��У������й�˵����ȷ���ǣ� ��
A.ƽ��ǰ�����ŷ�Ӧ�Ľ��У�������ѹǿʼ�ղ���
B.ƽ��ʱ�������������䣬�����������Ӧ���ʼӿ�
C.ƽ��ʱ���������¶ȣ�CO�������������÷�Ӧ�ġ�H��0
D.�����������䣬ʹ�ò�ͬ�������÷�Ӧƽ�ⳣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���У���ȷ���ǣ� ��
A. ԭ���������������ԭ��Ӧ����ѧ��ת��Ϊ���ܵ�װ��
B. ���������к�̼�����Աȴ�����ʴ
C. ��ԭ����У����Ӵ���������
D. ��ԭ����У������Ϸ�����ԭ��Ӧ�������Ϸ���������Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com