
 对于密闭容器中的反应:N2(g)+3H2(g)
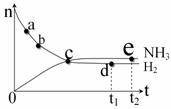
对于密闭容器中的反应:N2(g)+3H2(g)![]() 2NH3(g),400℃,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是:
2NH3(g),400℃,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是:
A.点a的正反应速率比点b的大
B.点c处反应达到平衡
C.点d (t1时刻) 和点 e (t2时刻) 处n(N2)不一样
D.点c处氢气与氨气的物质的量浓度一样
科目:高中化学 来源: 题型:
 对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),400℃,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )
对于密闭容器中的反应:N2(g)+3H2(g)?2NH3(g),400℃,30MPa下n(NH3)和n(H2)随时间变化的关系如图所示.下列叙述正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
 合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)  2NH3(g)(正反应为放热反应),673K、30MPa下,n(NH3)和n(H2)随时间 t变化的关系如图所示.下列叙述中,正确的是( )
2NH3(g)(正反应为放热反应),673K、30MPa下,n(NH3)和n(H2)随时间 t变化的关系如图所示.下列叙述中,正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210.01 | -252.77 | -77.74 |
| 沸点(℃) | -195.79 | -259.23 | -33.42 |
查看答案和解析>>
科目:高中化学 来源: 题型:
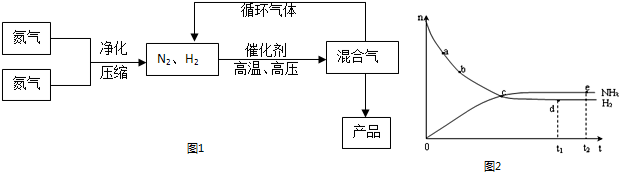
 合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:| A、点a的正反应速率比点b的小 | B、点 c处反应达到平衡 | C、点d(t1时刻) 和点 e(t2时刻) 处n(N2)不一样 | D、其他条件不变,773K下反应至t1时刻,n(H2)比上图中d点的值大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)
合成氨工业对国民经济和社会发展具有重要的意义.对于密闭容器中的反应:N2(g)+3H2(g)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com