
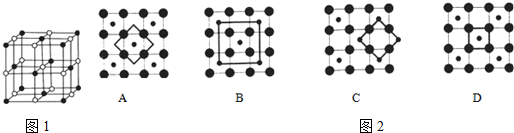
分析 由氧化物晶胞结构可知晶胞中Co、O原子数目之比为1:1,假设黑色球为Co原子,以顶点Co原子为研究对象,与之等距离且最近的钴原子位于面心,每个顶点为8个晶胞共用,每个面心为2个晶胞共用;CoO2的重复结构单元示意图中Co、O原子数目之比应为1:2,结合均摊法计算判断.
解答 解:由氧化物晶胞结构可知晶胞中Co、O原子数目之比为1:1,假设黑色球为Co原子,以顶点Co原子为研究对象,与之等距离且最近的钴原子位于面心,每个顶点为8个晶胞共用,每个面心为2个晶胞共用,在该晶体中与一个钴原子等距离且最近的钴原子数目为$\frac{3×8}{2}$=12;
CoO2的重复结构单元示意图中Co、O原子数目之比应为1:2,由图象可知:
A中Co、O原子数目之比为1:4×$\frac{1}{2}$=1:2,符合,
B中Co、O原子数目之比为(1+4×$\frac{1}{4}$):4=1:2,符合,
C中Co、O原子数目之比为4×$\frac{1}{4}$:4×$\frac{1}{2}$=1:2,符合,
D中Co、O原子数目之比为1:4×$\frac{1}{4}$=1:1,不符合,
故答案为:12;D.
点评 本题是对物质结构与性质的考查,涉及均摊法的应用、晶胞计算等,侧重考查学生对知识的理解与迁移应用,注意利用均摊法的灵活应用,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
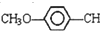 =CHCOOCH2CH2CH(CH3)2合成路线如下:
=CHCOOCH2CH2CH(CH3)2合成路线如下: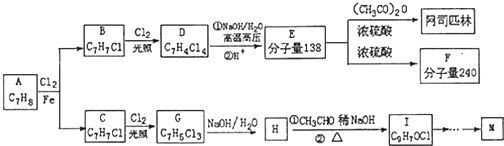
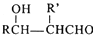 $\stackrel{△}{→}$RCH═
$\stackrel{△}{→}$RCH═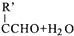
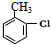 ,H→I两步反应的反应类型加成反应、消去反应
,H→I两步反应的反应类型加成反应、消去反应
 任意1种.
任意1种.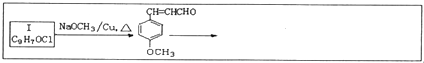
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.| 0.01mol/LKIO3酸性溶液 (含淀粉)的体积/mL | 0.01mol/L Na2SO3溶液 的体积/mL | H2O 的体积 /mL | 实验温 度/℃ | 溶液出现 蓝色时所 需时间/s | |
| 实验1 | 5 | V1 | 35 | 25 | |
| 实验2 | 5 | 5 | 40 | 25 | |
| 实验3 | 5 | 5 | V2 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2 L乙醇所含分子数为0.5NA | |
| B. | 40 g氢氧化钠含有氧原子数为NA | |
| C. | 1mol任何纯净物都含有6.02×1023个原子 | |
| D. | 标准状况下,22.4 L氢气含有NA个氢原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com