
 ����λ���á��������
����λ���á������������ A��B��C��D��E��F��G��ǰ�����ڣ���ϡ�����壩ԭ�������������������Ԫ�أ�A��ԭ�Ӻ������ֻ��һ���˶�״̬����AΪHԪ�أ�����Ԫ��B��Cԭ�ӵĺ���ɶԵ�������δ�ɶԵ�������2������B��C��������Ų�Ϊ1s22s22p2��1s22s22p4��ΪC��OԪ�أ�B��C��Dͬ������ԭ������һ������DΪF��E�����s��p�ܼ��ĵ���������ȣ���EΪMgԪ�أ�F��Eͬ�����ҵ�һ�����ܱ�EС��FΪNa��G��+1�����ӣ�G+���ĸ������ȫ������Ԫ�صĻ�̬ԭ�������ܲ�ֻ��һ�����ӣ������ܲ���ѳ������ӣ�����������Ϊ2+8+18+1=29����GΪCu���ݴ˽��
��� �⣺A��B��C��D��E��F��G��ǰ�����ڣ���ϡ�����壩ԭ�������������������Ԫ�أ�A��ԭ�Ӻ������ֻ��һ���˶�״̬����AΪHԪ�أ�����Ԫ��B��Cԭ�ӵĺ���ɶԵ�������δ�ɶԵ�������2������B��C��������Ų�Ϊ1s22s22p2��1s22s22p4��ΪC��OԪ�أ�B��C��Dͬ������ԭ������һ������DΪF��E�����s��p�ܼ��ĵ���������ȣ���EΪMgԪ�أ�F��Eͬ�����ҵ�һ�����ܱ�EС��FΪNa��G��+1�����ӣ�G+���ĸ������ȫ������Ԫ�صĻ�̬ԭ�������ܲ�ֻ��һ�����ӣ������ܲ���ѳ������ӣ�����������Ϊ2+8+18+1=29����GΪCu��
��1��EΪMgԪ�أ���̬ԭ�ӵĵ����Ų�Ϊ1s22s22p63s2��
�ʴ�Ϊ��1s22s22p63s2��
��2��B��C����C��O�����γɻ�����BC��CO����BC2��CO2����CO2�ṹʽΪO=C=O����������غϣ�Ϊ�Ǽ��Է��ӣ�CO�ĽṹʽΪC��O������2mol�м���
�ʴ�Ϊ���Ǽ��ԣ�2��
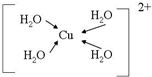
��3��Cu��H2O��42+��ˮ��ͭ�����γ�4����λ�����ṹΪ ��
��
�ʴ�Ϊ�� ��
��
��4���ⶨA��D�γɵĻ�����HF����Է�������ʱ��ʵ��ⶨֵһ���������ֵ��ԭ����HF����֮�����������γɵϷ��ӣ�
�ʴ�Ϊ��HF����֮�����������γɵϷ��ӣ�
��5����Ԫ��H��C��Al��ɵ�ԭ�Ӹ�����9��3��1��һ�����ʣ������к�������ͬ��ԭ���ţ���ṹ��ʽΪAl��CH3��3�����ݼ۲���ӶԻ������ۼ�����Ӷ���Ϊ3+$\frac{1}{2}$��3-3��1��=3���ӻ�����Ϊsp2����������ˮ��ը�����ɰ�ɫ��������ɫ���壬��Ӧ�Ļ�ѧ����ʽΪAl��CH3��3+3H2O=Al��OH��3��+3CH4����
�ʴ�Ϊ��Al��CH3��3��sp2��Al��CH3��3+3H2O=Al��OH��3��+3CH4����
���� �����Ƕ����ʽṹ�����ʵĿ��飬�漰��������Ų��������ܡ��ӻ���������Ӽ��Ե��жϡ���λ��������ȣ���Ŀ�Ѷ��еȣ�����Ԫ��ԭ�ӵĵ����Ų���ԭ�ӽṹ���ƶ�Ԫ���ǽ���Ĺؼ�����Ҫѧ���߱���ʵ�Ļ����������ڿ���ѧ���ķ��������ͶԻ���֪ʶ��Ӧ��������


 �����Ծ���Ԫ���Ծ�ϵ�д�
�����Ծ���Ԫ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ǵ�ԭ�Ӻ�����Ӳ����������������Ӷ����� | |
| B�� | ���ǵ�L�����������ͬ | |
| C�� | ���ǵ�ԭ�Ӻ˶��������ӵ��������� | |
| D�� | ������������ˮ��ӦʱԽ��Խ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ۢ� | C�� | �ڢ� | D�� | �٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ${\;}_{8}^{17}O$ԭ�Ӻ��ں���8������ | B�� | ${\;}_{8}^{17}O$ԭ�Ӻ��ں���8������ | ||
| C�� | ${\;}_{8}^{17}O$ԭ�Ӻ�����17������ | D�� | ${\;}_{8}^{17}O$ԭ�Ӻ��ں���17������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �¶ȣ��棩 | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| ƽ��������Ũ�� ��10-3mol/L�� | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
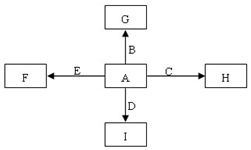 ͼ�У�A��B��C��D��E�ǵ��ʣ�G��H��I��F��B��C��D��E�ֱ��A�γɵĶ�Ԫ�������֪���ٷ�ӦC+G$\stackrel{����}{��}$B+H�ܷų��������ȣ��÷�Ӧ��Ӧ��������ĺ��ӣ�
ͼ�У�A��B��C��D��E�ǵ��ʣ�G��H��I��F��B��C��D��E�ֱ��A�γɵĶ�Ԫ�������֪���ٷ�ӦC+G$\stackrel{����}{��}$B+H�ܷų��������ȣ��÷�Ӧ��Ӧ��������ĺ��ӣ� �����Ŀռ乹����ֱ���ͣ�
�����Ŀռ乹����ֱ���ͣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| N2H4 | N2O4 | |
| �ܶ�/g/cm3 | 1.004 | 1.44 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com