
A.在100 ℃、101 kPa条件下,液态水的气化热为40.69 kJ·mol-1,则H2O(g) H2O(l) 的 ΔH =" —40.69" kJ·mol-1 H2O(l) 的 ΔH =" —40.69" kJ·mol-1 |
| B.在25℃、101kPa,2mol S的燃烧热是1mol S的燃烧热2倍 |
| C.CH4(g) +2O2(g) =CO2(g) +2H2O(g) ΔH=-akJ·mol-1,这里ΔH代表燃烧热 |
| D.已知: |
| 共价键 | C-C | C=C | C-H | H-H |
| 键能/ kJ·mol-1 | 348 | 610 | 413 | 436 |
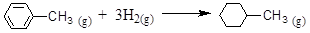 的ΔH为-384 kJ·mol-1
的ΔH为-384 kJ·mol-1 H2O(l) 的ΔH =" —40.69" kJ·mol-1。正确。B.燃烧热是1mol的物质完全燃烧产生稳定的氧化物时所释放的热量。在25℃、101kPa,2mol S的燃烧放出的热量是1mol S的燃烧放出热量2倍,但是燃烧热是相同的。错误。C.CH4(g) +2O2(g) =CO2(g) +2H2O(g) ΔH=-akJ·mol-1,这里ΔH并不代表燃烧热。因为水在气态时是不稳定的状态,液态才是水的稳定状态。错误。D.在苯分子中不含C-C及C=C,而是存在一种介于单键与双键之间的一种特殊的化学键。因此根据表格提供的数据不能计算出该反应的反应热。正确。
H2O(l) 的ΔH =" —40.69" kJ·mol-1。正确。B.燃烧热是1mol的物质完全燃烧产生稳定的氧化物时所释放的热量。在25℃、101kPa,2mol S的燃烧放出的热量是1mol S的燃烧放出热量2倍,但是燃烧热是相同的。错误。C.CH4(g) +2O2(g) =CO2(g) +2H2O(g) ΔH=-akJ·mol-1,这里ΔH并不代表燃烧热。因为水在气态时是不稳定的状态,液态才是水的稳定状态。错误。D.在苯分子中不含C-C及C=C,而是存在一种介于单键与双键之间的一种特殊的化学键。因此根据表格提供的数据不能计算出该反应的反应热。正确。

科目:高中化学 来源:不详 题型:单选题
| A.在水中的氢原子和氧原子有的以化学键结合,有的以氢键结合 |
| B.阴、阳离子之间除了有静电引力之外还有静电排斥力 |
| C.根据电离方程式:HCl====H+ + Cl- ,可判断HCl里存在离子键 |
| D.活泼金属元素与非金属元素之间可形成离子键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.烧杯a中的溶液pH不变 |
| B.烧杯a中发生氧化反应 |
| C.烧杯a中发生的反应为2H2O+2e-=H2↑+2OH- |
| D.烧杯b中发生的反应为Zn-2e-=Zn2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
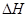 =-a kJ·mol-1 ② 2A → A-A;
=-a kJ·mol-1 ② 2A → A-A;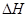 =-b kJ·mol-1
=-b kJ·mol-1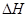 =-c kJ·mol-1
=-c kJ·mol-1 X(g);
X(g);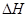 =-a KJ·mol-1(a>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
=-a KJ·mol-1(a>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 2 mol A2、1 mol BC | 1 mol X | 4 mol A2、2 mol BC |
| 平衡时n(X) | 0.5mol | n2 | n3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 体系的压强 | P1 | P2 | P3 |
| 反应物的转化率 | 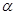 1 1 | 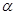 2 2 | 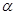 3 3 |
 ( A2)为 。
( A2)为 。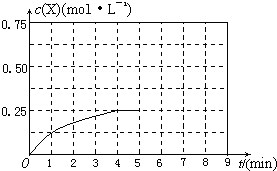
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碳原子的杂化类型发生了改变 |
| B.微粒的形状发生了改变 |
| C.微粒的稳定性发生了改变 |
| D.微粒中的键角发生了改变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 物质 | CH4 | C2H2 | H2 |
| 燃烧热/kJ/mol | 890.3 | 1299.6 | 285.8 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.过渡金属的原子或离子一般都有接受孤电子对的空轨道,易形成配合物 |
| B.中心原子或离子采取sp3杂化轨道形成的配离子均呈正四面体结构 |
| C.当中心原子或离子的配位数为6时,配离子一定呈八面体结构 |
| D.含有两种配位体且配位数为4的配离子一定存在顺反异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com