
| A、标准状况下,2.24LH2O含有的分子数等于0.1NA |
| B、20g重水(D2 O)所含的电子数为10NA |
| C、标准状况下,2.24LCl2与过量的稀NaOH 溶液反应,转移电子总数为0.2NA |
| D、25℃时,pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA |
| m |
| M |
| V |
| 22.4 |
| 20g |
| 20g/mol |


 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、露天焚烧秸秆 |
| B、直接用煤作燃料? |
| C、汽车排放尾气 |
| D、利用太阳能发电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、区别地沟油(加工过的餐饮废弃油)和矿物油(汽油、煤油、柴油等)的方法是加入足量氢氧化钠溶液共热,不分层的是地沟油 |
| B、发泡塑料饭盒不适于盛放含油较多的食品 |
| C、光化学烟雾的产生与汽车排放的尾气有关 |
| D、将废电池深埋,可以避免其中的重金属污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、把SO2通入紫色石蕊试液,可验证SO2的漂白性 |
| B、构成如图所示装置时,盐桥中的K+向左池移动 |
| C、配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会使所配溶液浓度偏高 |
| D、将10克ZnSO4?7H2O溶解在90克水中配制10%的ZnSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:

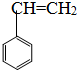 ;②CH3-CH=CH-CH3; ③CH2=CH-CH=CH2;④CH≡C-CH3;⑤
;②CH3-CH=CH-CH3; ③CH2=CH-CH=CH2;④CH≡C-CH3;⑤
| A、①② | B、④⑤ | C、③⑤ | D、①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol?L-1CH3COOH溶液加水稀释,n(H+)增大 |
| B、0.2 mol?L-1盐酸与等体积0.05 mol?L-1Ba(OH)2溶液混合后,溶液pH为1 |
| C、向含等浓度的KCl和KI的混合溶液,滴加少量AgNO3溶液生成黄色沉淀,说明同温度下Ksp(AgCl)大于Ksp(AgI) |
| D、若NH4HCO3溶液、NH4HSO4溶液和NH4NO3溶液中c(NH4+)相等,则c(NH4HSO4)<c(NH4NO3)<c(NH4HCO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在如图用石墨作电极的电解池中,放入500mLCuSO4溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量.请回答下列问题:
在如图用石墨作电极的电解池中,放入500mLCuSO4溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com