
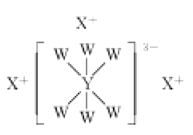
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,它们的原子最外层电子数之和为17,其中W、X、Y三种元素的简单离子的核外电子排布相同,且可形成结构如图所示的化合物。下列说法正确的是( )
A.X、Y、Z的最高价氧化物对应水化物两两之间均能反应
B.X与Z形成的化合物会抑制水的电离
C.W的简单气态氢化物的热稳定性比Z的弱
D.原子半径: Z>Y>X>W
【答案】A
【解析】
根据W、X、Y形成化合物的结构,X的化合价为+1,短周期元素有H、Li、Na,且W、X、Y三种元素的简单离子的核外电子排布相同,故X为钠;根据形成物质的阴离子YW63-,若W化合价为-1,则Y化合价为+3,其他假设均不符合题意,则W为氟,Y为铝;W、X、Y、Z的最外层电子数之和为17,则Z为硫。
A. 根据分析,X、Y、Z的最高价氧化物对应水化物分别为NaOH、Al(OH) 3、H2SO4,由于Al(OH) 3是两性氢氧化物,既可以与强酸反应,又可以与强碱反应,故三者可以两两相互反应,A说法正确;
B. 根据分析,X与Z形成的化合物为Na2S,S2-为弱酸根离子发生水解,促进水的电离,B说法错误;
C. 非金属性越强,气态氢化物的热稳定性越强,根据元素周期律非金属:F>S,气态氢化物的热稳定性:HF>H2S,C说法错误;
D. 根据元素周期律,同周期随着核电荷数增加,原子半径减小,同主族随着核电荷数的增加,原子半径增大,原子半径: Na> Al >S>F,D说法错误;
答案选A。


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:
【题目】(1)写出下列各烷烃的分子式.
①烷烃A在同温同压下蒸气的密度是H2的43倍__________。
②烷烃B的分子中含有200个氢原子____________。
③1L烷烃C的蒸气完全燃烧时,生成同温同压下15L的水蒸气____________。
④0.1mol烷烃D完全燃烧,消耗标准状况下的O2 11.2L________________。
(2)乙烯是一种重要的化工原料.根据下列转化关系回答:

①乙烯分子中官能团的名称是_________ 。
②E的分子式是___________。
③乙烯转化成A的化学方程式是____________________ ,反应类型是_________ 。
④已知D是一种常见的高分子材料,写出它的结构简式__________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用生活中常见的材料可以进行很多科学实验,甚至制作出一些有实际应用价值的装置来,下图就是一个用废旧材料制作的可用于驱动玩具的电池的示意图。当电池工作时,有关说法正确的是( )
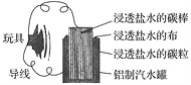
A.铝罐将逐渐被腐蚀
B.碳粒和碳棒上发生的反应为O2+2H2O-4e-=4OH-
C.碳棒应与玩具电机的负极相连
D.该电池工作一段时间后碳棒和碳粒的质量会减轻
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用沉淀滴定法快速测定NaBr等卤化物溶液中c(Br-),实验过程包括标准溶液的配制和滴定待测溶液。
I.标准溶液的配制
准确称取AgNO3基准物8.5g,配制成500mL标准溶液,放在棕色试剂瓶中避光保存,备用。
II.滴定的主要步骤
a.取待测NaBr溶液25.00mL,配制成100mL溶液,取其中25.00mL于锥形瓶中。
b.加入K2CrO4溶液作指示剂。
c.用AgNO3标准溶液进行滴定,记录消耗的体积。
d.重复上述操作三次,测定数据如下表:
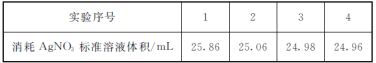
e.数据处理。
请回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的玻璃仪器除烧杯和玻璃棒外还有___,配制的AgNO3溶液的浓度为___。
(2)AgNO3标准溶液应使用___ (填“酸式”或“碱式”)棕色滴定管,检漏后装液前需要进行的操作有___。
(3)实验可用铬酸钾(K2CrO4)作指示剂,一方面,是由于Ag2CrO4是砖红色沉淀,现象变化明显,另一方面,是由于___。
(4)滴定应在近中性或弱碱性(6.5<pH<10.5)的条件下进行,其原因是酸性过强,发生如下离子反应:___;碱性过强,会导致___。
(5)达到滴定终点时的现象为___。
(6)由上述实验数据测得原溶液c(Br-)=___ mol·L-1。
(7)若在配制AgNO3标准溶液时,未洗涤玻璃棒和烧杯,则对c(Br-)测定结果的影响为___ (填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A是石油裂解气的主要成份。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。回答下列问题:

(1)A转化为B的反应类型___________。
(2)D分子中官能团的名称_______。
(3)写出B与金属钠反应的化学方程式是____________________。
(4)下列说法正确的是________________。
A.B分子中的所有原子在同一平面上
B.一定条件下,C中的官能团可以用银氨溶液来检验
C.A可以在其他条件下被氧气氧化成乙酸
D.A使酸性KMnO4溶液褪色和使溴水褪色,其原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三代混合动力车目前一般使用镍氢电池(M表示储包合金),电池总反应式为H2+2NiOOH![]() 2Ni(OH)2。汽车上坡或加速时,电动机提供推动力:下坡或刹车时,电池处于充电状态。下列说法中正确的是( )
2Ni(OH)2。汽车上坡或加速时,电动机提供推动力:下坡或刹车时,电池处于充电状态。下列说法中正确的是( )
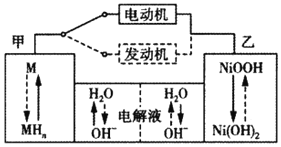
A.放电时甲为负极,充电时为阳极
B.汽车上坡时发生图中虚线所示的过程
C.汽车下坡电流的方向为:甲电极→发动机→乙电极
D.汽车下坡时,甲电极周围溶液的pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2与H2的混合气体5g,在150℃时和足量的氧气混合,用电火花充分引燃,在相同状况下,再将反应后所得混合气体通入到足量的Na2O2中,测得Na2O2固体增重的质量为3.4g,则原混合气体中CO2的物质的量分数为
A.88%B.75%C.25%D.32%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾晶体)为翠绿色晶体,溶于水,难溶于乙醇,110℃下失去结晶水,230℃分解;是制备负载型活性铁催化剂的主要原料。实验室利用(NH4)2Fe(SO4)2·6H2O(硫酸亚铁铵)、H2C2O4(草酸)、K2C2O4(草酸钾)、30%双氧水等为原料制备三草酸合铁酸钾晶体的部分实验过程如下:
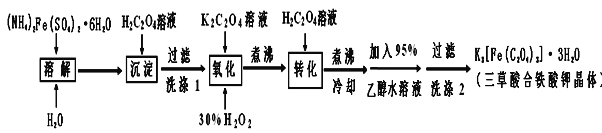
已知:沉淀: FeC2O4·2H2O既难溶于水又难溶于强酸
6FeC2O4+3H2O2+6K2C2O4=4K3[Fe(C2O4)3]+2Fe(OH)3↓、2Fe(OH)3+3H2C2O4+3K2C2O4=2K3[Fe(C2O4)3]+6H2O
(1)溶解时加几滴稀硫酸的目的是___________________________。
(2)沉淀过滤后,洗涤1的操作方法是______。
(3)在沉淀中加入饱和K2C2O4溶液,并用40 ℃ 左右水浴加热,再向其中慢慢滴加足量的30%H2O2溶液,不断搅拌。此过程需保持温度在40 ℃ 左右,可能的原因是____________。加入30%过氧化氢溶液完全反应后,煮沸的目的是________ 。
(4)洗涤2中所用洗涤试剂最合适的是________(填选项字母)。
A 草酸钠溶液 B 蒸馏水 C 乙醇 D KCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或者是水溶液),盐酸必须避开它们,否则就无法通过。
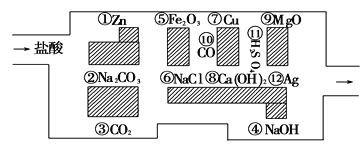
(1)迷宫内12种物质中属于碱性氧化物的有________________,写出其中一种与盐酸反应的化学方程式________________________________________。
(2)迷宫内12种物质中金属单质及其活动顺序是_________________,试写一个相互置换的化学方程式:________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com