
【题目】某溶液中含如下离子组中的若干种:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,且物质的量浓度相同。某同学欲探究该溶液的组成,进行如下实验:
,且物质的量浓度相同。某同学欲探究该溶液的组成,进行如下实验:
Ⅰ![]() 用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰
用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰
Ⅱ![]() 另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成
另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成
Ⅲ![]() 取Ⅱ反应后的溶液分置于两支试管中,第一支试管中加入
取Ⅱ反应后的溶液分置于两支试管中,第一支试管中加入![]() 溶液,有白色沉淀生成,再滴加KSCN溶液,上层清液变红;第二支试管中加入
溶液,有白色沉淀生成,再滴加KSCN溶液,上层清液变红;第二支试管中加入![]() ,充分振荡静置后溶液分层,下层出现紫红色。下列说法正确的是
,充分振荡静置后溶液分层,下层出现紫红色。下列说法正确的是![]()
A.原溶液中![]() 和
和![]() 至少有一种,一定没有
至少有一种,一定没有![]() 、
、![]()
B.步骤Ⅱ中无色气体可能含有![]() ,原溶液中可能含有
,原溶液中可能含有![]()
C.原溶液中肯定含有![]() 、
、![]()
D.为确定是否含有![]() ,可取原溶液加入少量硝酸银和稀硝酸,观察是否产生沉淀
,可取原溶液加入少量硝酸银和稀硝酸,观察是否产生沉淀
【答案】C
【解析】
Ⅰ![]() 用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰,证明溶液中一定含有钾离子;
用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰,证明溶液中一定含有钾离子;
Ⅱ![]() 另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成,证明含有
另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成,证明含有![]() 、
、![]() ,一定不含有硅酸根离子、碳酸根离子;
,一定不含有硅酸根离子、碳酸根离子;
Ⅲ![]() 取Ⅱ反应后的溶液分置于两支试管中,第一支试管中加入
取Ⅱ反应后的溶液分置于两支试管中,第一支试管中加入![]() 溶液,有白色沉淀生成,即为硫酸钡,证明含有硫酸根离子,再滴加KSCN溶液,上层清液变红,即出现了三价铁离子,是Ⅱ过程中亚铁离子被硝酸氧化的结果;第二支试管中加入
溶液,有白色沉淀生成,即为硫酸钡,证明含有硫酸根离子,再滴加KSCN溶液,上层清液变红,即出现了三价铁离子,是Ⅱ过程中亚铁离子被硝酸氧化的结果;第二支试管中加入![]() ,充分振荡静置后溶液分层,下层出现紫红色,证明碘单质出现,一定含有碘离子,则含有
,充分振荡静置后溶液分层,下层出现紫红色,证明碘单质出现,一定含有碘离子,则含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,一定不含
,一定不含![]() ,由于物质的量浓度相同,由电荷守恒可知还应含有
,由于物质的量浓度相同,由电荷守恒可知还应含有![]() 、
、![]() 。
。
A.由以上分析可知原溶液中含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,不含
,不含![]() 、
、![]() 、
、![]() 、
、![]() ,故A错误;
,故A错误;
B.步骤Ⅱ中无色气体为NO,且原溶液含![]() ,则不含有
,则不含有![]() ,故B错误;
,故B错误;
C.由以上分析可知原溶液中含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,故C正确;
,故C正确;
D.取原溶液加入少量硝酸银和稀硝酸,生成白色沉淀为硫酸银、AgCl,不能检验氯离子,故D错误;
故选C。


科目:高中化学 来源: 题型:
【题目】下列各反应对应的离子方程式正确的是
A.向100 mL 0.12 mol·L1的Ba(OH)2溶液中通入0.02 mol CO2: Ba2++3OH+2CO2=![]() +BaCO3↓+H2O
+BaCO3↓+H2O
B.向Ca(OH)2溶液中加入过量的NaHCO3溶液:Ca2++2OH+2![]() =
=![]() CaCO3↓+
CaCO3↓+![]() +2H2O
+2H2O
C.硫酸氢钠与氢氧化钡两种溶液反应后溶液恰好呈中性:H++![]() +Ba2++OH=BaSO4↓+H2O
+Ba2++OH=BaSO4↓+H2O
D.向含0.1 mol NaOH和0.2molNa2CO3的溶液中加入1L0.4 mol·L1稀盐酸:OH+![]() +3H+=CO2↑+2H2O
+3H+=CO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为一重要的烃的衍生物,以下关于它的说法中不正确的是( )
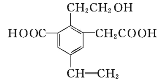
A.1mol该物质,最多可以和4molH2发生加成反应
B.1mol该物质消耗Na、NaOH、NaHCO3的物质的量之比为3∶2∶2
C.可以用酸性高锰酸钾溶液检验其中的碳碳双键
D.该物质能够在催化剂作用下被氧化为醛
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请回答氯碱工业的如下问题:
(1)氯气、烧碱是电解食盐水时按照固定的比率k(质量比)生成的产品。理论上k=_______(要求计算表达式和结果);
(2)原料粗盐中常含有泥沙和Ca2+、Mg2+、Fe3+、SO42-等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)③BaCl2,这3种试剂添加的合理顺序是______________(填序号);
(3)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺可以节(电)能30%以上。在这种工艺设计中,相关物料的传输与转化关系如下图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
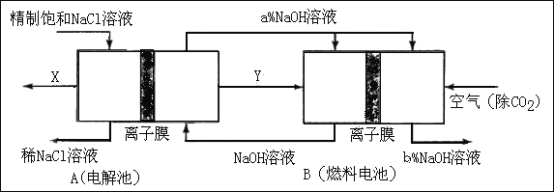
①图中X、Y分别是_____、_______(填化学式),分析比较图示中氢氧化钠质量分数a%与b%的大小_________;
②分别写出燃料电池B中正极、负极上发生的电极反应正极:______;负极:_____;
③这样设计的主要节(电)能之处在于(写出2处)____________、____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。
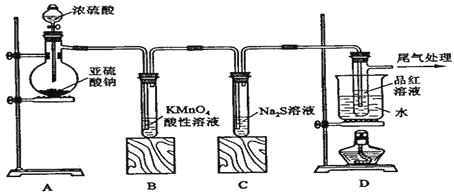
请到答F列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是 ,其中发生反应的化学方程式为 ;
(2)实验过程中,装置B、C中发生的现象分别是 、 ,这些现象分别说明SO2具有的性质是 和 ;装置B中发生反应的离子方程式为 ;
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象 ;
(4)尾气可采用 溶液吸收。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验硫酸铵的热分解产物,某同学设计了如图所示实验装置。
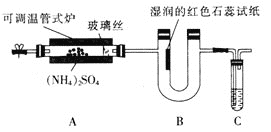
回答下列问题:
(1)![]() 装置A中玻璃丝的作用是________。
装置A中玻璃丝的作用是________。
![]() 若在
若在![]() 时加热,B中湿润的红色石蕊试纸变蓝,则有________(填化学式
时加热,B中湿润的红色石蕊试纸变蓝,则有________(填化学式![]() 产生;若C中盛放
产生;若C中盛放![]() 溶液,有白色沉淀产生,________(填“能”或“不能”
溶液,有白色沉淀产生,________(填“能”或“不能”![]() 说明分解产物中有
说明分解产物中有![]() ,理由是________________;若要检验是否有
,理由是________________;若要检验是否有![]() 产生,C中应盛放的试剂是________。
产生,C中应盛放的试剂是________。
(2)若在A中装入![]() ,按下图连接,在
,按下图连接,在![]() 时加热至完全分解。
时加热至完全分解。
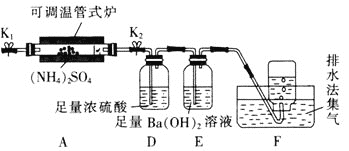
![]() 实验结束后,为防止倒吸,正确的操作是________。
实验结束后,为防止倒吸,正确的操作是________。
![]() 浓硫酸吸收的气体是________
浓硫酸吸收的气体是________![]() 填化学式
填化学式![]() 。
。
![]() 若D中增重
若D中增重![]() ,E中增重
,E中增重![]() ,F中收集的气体为
,F中收集的气体为![]() 已折算为标准状况
已折算为标准状况![]() ,分解反应的化学方程式为________。
,分解反应的化学方程式为________。![]() 已知分解产物中没有
已知分解产物中没有![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质A~G有下图所示转化关系(部分反应物、生成物没有列出)。其中A为某金属矿的主要成分,经过一系列反应可得到B和C。单质C可与E的浓溶液发生反应,G为砖红色沉淀。
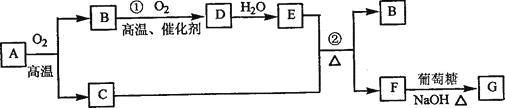
请回答下列问题:
(1)写出下列物质的化学式:B__________、E__________、G__________;
(2)利用电解可提纯C物质,在该电解反应中阳极物质是____________,阴极物质是__________,电解质溶液是__________;
(3)反应②的化学方程式是__________。
(4)将0.23 mol B和0.11 mol氧气放入容积为1 L的密闭容器中,发生反应①,在一定温度下,反应达到平衡,得到0.12 mol D,则反应的平衡常数K=___________。若温度不变,再加入0.50 mol氧气后重新达到平衡,则B的平衡浓度___________(填“增大”、“不变”或“减小”),氧气的转化率___________(填“升高”、“不变”或“降低”),D的体积分数___________(填“增大”、“不变”或“减小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,1 mol·L-1的HClO2和1 mol·L-1的HMnO4两种酸溶液,起始时的体积均为V0,分别向两溶液中加水进行稀释,稀释后溶液体积为V,所得曲线如图所示。下列说法正确的是( )

A.在0≤pH≤5时,HMnO4溶液满足pH=lg![]() +1
+1
B.当稀释至pH均为3时,溶液中c(ClO2-)>c(MnO4-)
C.稀释前分别用1 mol·L-1的NaOH溶液中和,消耗的NaOH溶液体积:HMnO4>HClO2
D.当稀释至pH均为3时,HMnO4溶液中的V等于1000 V0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像符合题意的是
A.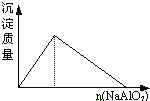 盐酸溶液中逐滴加入NaAlO2
盐酸溶液中逐滴加入NaAlO2
B.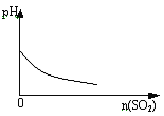 SO2气体逐渐通入溴水中
SO2气体逐渐通入溴水中
C.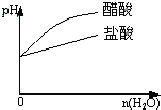 pH=1的醋酸与盐酸溶液分别加水稀释
pH=1的醋酸与盐酸溶液分别加水稀释
D.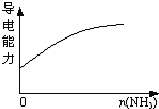 氨气逐渐通入醋酸中
氨气逐渐通入醋酸中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com