
����Ŀ�������г����۵�ij��ʳ�þ����ΰ�װ����������˵����
��Ʒ�� | GB5461 |
��Ʒ�ȼ� | һ�� |
�� �� | ʳ�Ρ�����ء������ |
�⺬��(��I�ƣ� | 20~50mg/kg |
��װʱ�� | |
��װ��ҵ |
��1���������⻯�������������·������·�Ӧ����ƽ��ѧ����ʽ������ѧ���������ڿհ״���
____KIO3��___KI��___H2SO4��___K2SO4��___I2��___H2O
��2��������Ӧ���ɵ�I2�������Ȼ�̼���顣�������Ȼ�̼��Һ�м���Na2SO3ϡ��Һ����I2��ԭ���Ի������Ȼ�̼��
��Na2SO3ϡ��Һ��I2��Ӧ�����ӷ���ʽ��_________________________________��
��ijѧ����ƻ������Ȼ�̼�IJ�������Ϊ��
a.��������Ȼ�̼��Һ���ڷ�Һ©���У�
b.��������Na2SO3ϡ��Һ��
c.������²�Һ�塣
�����������©�IJ����������������е�λ����______________________��
��3����֪��I2��2S2O32����2I����S4O62����ijѧ���ⶨʳ�þ����εĵ⺬�����䲽��Ϊ��
a. ȷ��ȡwgʳ�Σ�����������ˮʹ����ȫ�ܽ⣻
b.��ϡ�����ữ������Һ����������KI��Һ��ʹKIO3��KI��Ӧ��ȫ��
c.�Ե���Ϊָʾ������μ������ʵ���Ũ��Ϊ2.0��10��3mol��L��1��Na2S2O3��Һ10.0mL��ǡ�÷�Ӧ��ȫ��
���ж�c�з�Ӧǡ����ȫ���ݵ�������______________________��
��b�з�Ӧ��������I2�����ʵ�����___________mol��
����������ʵ��Ͱ�װ��˵�������⾫���εĵ⺬���ǣ��Ժ�w�Ĵ���ʽ��ʾ��
_______________________mg/kg��
���𰸡�1 5 3 3 3 3 I2��SO32����H2O![]() 2I����SO42����2H�� �ڲ���b�����Ӳ���������Һ©��������� ��Һ����ɫǡ�ñ�Ϊ��ɫ 1.0��10��5 4.2 ��102/w
2I����SO42����2H�� �ڲ���b�����Ӳ���������Һ©��������� ��Һ����ɫǡ�ñ�Ϊ��ɫ 1.0��10��5 4.2 ��102/w
��������
��1���÷�Ӧ�У�KIO3��IԪ�ػ��ϼ���+5�۱�Ϊ0�ۡ�KI��IԪ�ػ��ϼ���-1�۱�Ϊ0�ۣ�����ת�Ƶ��������ƽ����ʽ��
��2����I2���������ԣ��ܽ�SO32-����ΪSO42-����������ԭΪI-��
������������߷�Ӧ����֣�
��3���ٶ���ǡ�÷�Ӧʱ����Һ����ɫǡ�ñ�Ϊ��ɫ��
�ڸ���I2+2S2O32-=2I-+S4O62-�е�����������֮��Ĺ�ϵʽ���㵫�����ʵ�����
�۸��ݵ��ʳ������֮�Ƚ��м��㡣
��1���÷�Ӧ�У�KIO3��IԪ�ػ��ϼ���+5�۱�Ϊ0�ۡ�KI��IԪ�ػ��ϼ���-1�۱�Ϊ0�ۣ�ת�Ƶ�������Ϊ5���ٽ��ԭ���غ���ƽ����ʽΪKIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O���ʴ�Ϊ��1��5��3��3��3��3��
��2����I2���������ԣ��ܽ�SO32-����ΪSO42-����������ԭΪI-�����ӷ���ʽΪI2+SO32-+H2O=2I-+SO42-+2H+���ʴ�Ϊ��I2+SO32-+H2O=2I-+SO42-+2H+��
������������߷�Ӧ����֣������ڲ���b�����Ӳ���������Һ©��������ã��ʴ�Ϊ���ڲ���b�����Ӳ���������Һ©��������ã�
��3���ٵ���������Һ����ɫ���������ȫ��Ӧ������Һ������ɫת��Ϊ��ɫ�����Ե���Һ����ɫת��Ϊ��ɫʱ˵����Ӧ��ȫ���ʴ�Ϊ����Һ����ɫǡ�ñ�Ϊ��ɫ��
���������ʵ���Ϊx��
I2+2S2O32-=2I-+S4O62-
1mol 2mol
x 1.00��10-3molL-1��0.024L
1mol��2mol=x����1.00��10-3molL-1��0.024L��
x=![]()
=1.2��10-5mol��
�ʴ�Ϊ��1.2��10-5��
�۸���KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O��![]() n��I2��=��KIO3��=4��10-6mol��������е������=4��10-6mol��127g/mol=0.508mg��
n��I2��=��KIO3��=4��10-6mol�������������=4��10-6mol��127g/mol=0.508mg��
��ÿkgʳ���е������Ϊy��
��y��1000g=0.508mg��wg��
y=![]() =
=![]() mg��
mg��![]() mg��
mg��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. �����ܱ������н��еķ�Ӧ��A��s����3B��g��![]() 2C��g����D��g������������ܶȱ��ֲ��䣬˵����Ӧ�Ѿ��ﵽƽ��
2C��g����D��g������������ܶȱ��ֲ��䣬˵����Ӧ�Ѿ��ﵽƽ��
B. C ( s) + H2O (g) ![]() CO ( g) + H2 (g)�������������䣬��С��������������ʼ�С������������
CO ( g) + H2 (g)�������������䣬��С��������������ʼ�С������������
C. N2(g) + 3H2(g)![]() 2NH3(g) ��H=��93kJ��mol��1���������ܱ������г���0.4 molN2(g)��2 mol H2(g)�ﵽƽ��ʱ�����Էų�37.2 kJ������
2NH3(g) ��H=��93kJ��mol��1���������ܱ������г���0.4 molN2(g)��2 mol H2(g)�ﵽƽ��ʱ�����Էų�37.2 kJ������
D. A(g)+ 3B (g) ![]() 2C (g) + D (g)�������ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ����
2C (g) + D (g)�������ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ����![]() ����
����![]() ����ǰ�߱Ⱥ��߿�
����ǰ�߱Ⱥ��߿�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���2 L�ܱ������У�A��B��C������������ʵ�����ʱ��仯��������ͼ��ʾ������˵����ȷ����
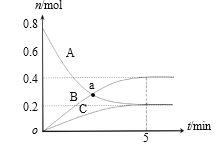
A.a��ʱ����(A) =��(B)
B.��Ӧ��ʼ��5min��B�����ʵ���������0.2 mol
C.��Ӧ�Ļ�ѧ����ʽΪ��3A![]() 2B��C
2B��C
D.��Ӧ��ʼ��5min����(C) =0.04 mol/(L��min)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й���ѧԺ�����Ŷ��о��������ڳ��³�ѹ�Ϳɼ����£�����![]() ��һ�ֹ���������ϳ�
��һ�ֹ���������ϳ�![]() ��ԭ��ʾ��ͼ���¡��Իش��������⣺
��ԭ��ʾ��ͼ���¡��Իش��������⣺
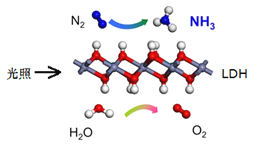
��1��������ת���ĽǶȣ��ù��̽�______ת����Ϊ__________��
��2���÷�Ӧ�Ļ�ѧ����ʽΪ��________________���������뻹ԭ�������ʵ���֮��Ϊ__________��
��3�����ڸ÷�Ӧ��˵������ȷ����_______
A������������ѧ��Ӧ���ʣ����̷�Ӧʱ�䣬�Ӷ���߲���Ч��
B���÷�Ӧ�������漰���Լ��ͷǼ��Լ��Ķ��Ѻ��γ�
C������ͨ������Һ̬�����ķ�����õ���
D������![]() �ϳ�
�ϳ�![]() �Ĺ��������˹��̵�
�Ĺ��������˹��̵�
��4���ִ���ҵ�����Ȼ��ơ�������̼�Ͱ���Ϊԭ���Ʊ��������ԭ�ϵ�˳���ǣ����Ȼ�����Һ��ͨ��_________�����ͣ���ͨ��������_________���Ƶ�![]() ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��R��W��X��Y��M��ԭ�����������������������Ԫ�ء�R���ͬλ�ص�ԭ�Ӻ��в������ӡ�W��X���γ������ȶ��Ļ����WX��WX2����ҵ��������������ʹ�õĻ�ʯȼ����ȼ�չ����н�����WX2�����������һ���̶ȵ��µ������ƽ���¶����ߡ�Y��X��ͬһ�����Ԫ�أ�����Ԫ�����ڱ�����X���ڡ�
��1��W��ԭ�ӽṹʾ��ͼ��__________________________��
��2��WX2�ĵ���ʽ��_______________________��
��3��R2X��R2Y�У��ȶ��Խϸߵ���____���ѧʽ�������ԭ�ӽṹ�ĽǶȽ�����ԭ��_____��
��4��Se��Y��ͬһ�����Ԫ�أ�����Ԫ�����ڱ�����Y���ڡ�
�ٸ���Ԫ�������ɣ������ƶ���ȷ����________������ĸ��ţ���
a��Se����������ϼ�Ϊ+7��
b��H2Se�Ļ�ԭ�Ա�H2Yǿ
c��H2SeO3�����Ա�H2YO4ǿ
d��SeO2��һ�������¿���NaOH��Һ��Ӧ
����������SeO2������洵��NH3���ɵõ����ֵ��ʺ�H2O���÷�Ӧ�Ļ�ѧ����ʽΪ_____________��
��5��������Ա�ӿ�ʯ�з����һ���������ѧʽ�ɱ�ʾΪM2O3��Ϊȷ��MԪ�ص����࣬������һϵ��ʵ�飬������£�
��M�����ԭ����������K��Rb��﨣�֮�䣻
��0.01 mol M2O3�ڼ�����Һ����Zn��ַ�Ӧ�ɵõ�M�ļ��⻯���Ӧ��ȫʱ����M2O3������ZnΪ0.06 mol��
�ۺ�������Ϣ�ƶϣ�M����λ��Ԫ�����ڱ���_________________�塣
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ұ�����������Ϊ98%,�ܶ�Ϊ1.84 g��cm-3������,�ݴ�����˵��������� (����)
A. ����������ʵ���Ũ��Ϊ18.4 mol��L-1
B. ������50 mL��������ͭ��Ӧ�ɵõ���״����SO2 0.46 mol
C. ijͬѧ�ø���������ϡ����ʱ,δϴ���ձ��Ͳ�����,������������Ƶ�ϡ����Ũ��ƫ��
D. ��������ˮ���������������Һ�����ʵ���Ũ��С��9.2 mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��Q��R��T��W��Ԫ�����ڱ��е�λ����ͼ��ʾ������T��������������������������ȣ����������������
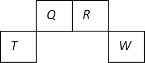
A. T������������Ӧ
B. Ԫ�صķǽ����ԣ�Qǿ��W
C. W�ĵ��ʹ���ʱ������������������ˮ����Ũ��Һ��Ӧ
D. ԭ��������R��1��Ԫ�ص�һ���⻯���ֽܷ�Ϊ������һ���⻯��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ж�ͼ���������ȷ����
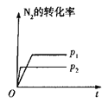
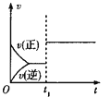

�� �� �� ��
A.ͼ�ɱ�ʾѹǿ�Է�Ӧ��![]()
![]() ��Ӱ��
��Ӱ��
B.ͼ���У�![]() ʱ�̸ı������һ���Ǽ����˴���
ʱ�̸ı������һ���Ǽ����˴���
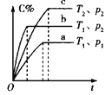
C.��ͼ����ʾ��Ӧ��![]() ����
����![]() ��
��![]()
D.ͼ����ʾˮ��![]() ��
��![]() �Ĺ�ϵ��ABC������������
�Ĺ�ϵ��ABC������������![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�����CO2�ŷ���һ����Ҫ���⡣CO2��������������ɵ�̼�л����Ҫ�����·�Ӧ��
��Ӧ����CO2(g)��3H2(g) ![]() CH3OH(g)��H2O(g) ��H1����49.6 kJ/mol
CH3OH(g)��H2O(g) ��H1����49.6 kJ/mol
��Ӧ����CH3OCH3(g)��H2O(g) ![]() 2CH3OH(g) ��H2����23.4 kJ/mol
2CH3OH(g) ��H2����23.4 kJ/mol
��Ӧ����2CO2(g)��6H2(g) ![]() CH3OCH3(g)��3H2O(g) ��H3
CH3OCH3(g)��3H2O(g) ��H3
��1����H3��________kJ/mol��
��2�����º��������£����ܱ�������ͨ������ʵ�����CO2��H2��������ӦI������������˵����ӦI�ﵽƽ��״̬����_______������ţ���
A����Ӧ��ϵ��ѹǿ���ֲ���
B�������ڵĻ��������ܶȱ��ֲ���
C��ˮ�����ж���2NA��H-O����ͬʱ������ж���3NA��H-H��
D��CH3OH��H2O��Ũ��֮�ȱ��ֲ���
��3����ӦII��ij�¶��µ�ƽ�ⳣ��Ϊ0.25�����¶��£����ܱ������м�������ʵ�����CH3OCH3(g)��H2O(g)����Ӧ��ijʱ�̲�ø����Ũ�����£�
���� | CH3OCH3(g) | H2O(g) | CH3OH(g) |
Ũ��/mol��L��1 | 1.8 | 1.8 | 0.4 |
��ʱv��___v������������������������������������Ӧ�ﵽƽ��״̬ʱ�����������CH3OH�������(CH3OH)% ��___%��
��4����ijѹǿ�£���ӦIII�ڲ�ͬ�¶ȡ���ͬͶ�ϱ�ʱ��CO2��ƽ��ת������ͼ��ʾ��T1�¶��£���6mol CO2��12mol H2����2 L���ܱ������У�5min��Ӧ�ﵽƽ��״̬����0��5min�ڵ�ƽ����Ӧ����v(CH3OCH3)��____��KA��KB��KC����֮��Ĵ�С��ϵΪ____��
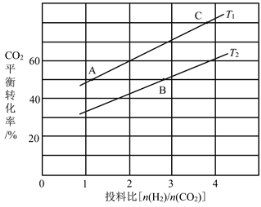
��5����ѹ�½�CO2��H2�������1��3��ϣ��ڲ�ͬ���������·�����ӦI�ͷ�ӦIII������ͬ��ʱ�����CH3OH��ѡ���ԺͲ������¶ȵı仯��ͼ�����У�CH3OH��ѡ���ԣ�![]() ��100%
��100%

�����������ºϳɼ״��Ĺ�ҵ������____��
A��210�� B��230�� C������CZT D������CZ(Zr��1)T
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com