
| A. | Cl-、HCO3-、Na+、K+ | B. | NO3-、Ba2+、K+、Cl- | ||
| C. | Fe3+、NO3-、K+、H+ | D. | Al3+、SO42-、NH4+、Cl- |
分析 由水电离出的c(OH-)=1×10-13 mol•L-1的溶液呈酸性或碱性,无色溶液说明不含有色离子,如Fe3+、Fe2+、Cu2+等,离子之间不反应的能大量共存,据此分析解答.
解答 解:A.HCO3-和氢离子或氢氧根离子都反应,所以强酸性或强碱性条件下都不能大量共存,故A错误;
B.这几种离子之间不反应,且和氢离子或氢氧根离子也不反应,且无色,所以能大量共存,故B正确;
C.Fe3+呈黄色,不符合无色条件,且Fe3+、H+和氢离子反应,Fe3+、OH-反应生成沉淀,所以不能大量共存,故C错误;
D.碱性条件下Al3+、NH4+不能大量共存,故D错误;
故选B.
点评 本题考查离子共存,为高频考点,正确判断溶液酸碱性是解本题关键,明确离子反应条件及离子性质,注意题干中限制性条件“无色”“一定”,题目难度中等.


科目:高中化学 来源: 题型:解答题
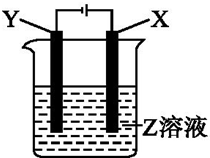 根据如图所示装置回答:
根据如图所示装置回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用试管加热碳酸氢钠固体时使试管口竖直向上 | |
| B. | 金属钠着火时使用泡沫灭火器灭火 | |
| C. | 验证氯气能否与水反应的实验时,用氢氧化钠溶液处理尾气 | |
| D. | 浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属氧化物一定是酸性氧化物 | B. | 碱性氧化物一定是金属氧化物 | ||
| C. | 碱性氧化物都能与水化合生成碱 | D. | 酸性氧化物都能与水化合生成酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+6H+═3I2+3H2O | |
| B. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 石灰乳与Na2CO3溶液混合:Ca2++CO32-═CaCO3↓ | |
| D. | 用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 品红溶液褪色---漂白性 | B. | 高锰酸钾溶液褪色---漂白性 | ||
| C. | 导致酸雨---酸性氧化物 | D. | 通入H2S溶液中变浑浊---氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 基态碳原子核外电子排布图是: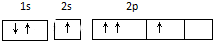 | |
| B. |  和 和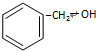 是同系物,性质相似 是同系物,性质相似 | |
| C. | 过氧化钠的电子式: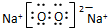 | |
| D. | 常见的化学键有:离子键、共价键、金属键、氢键等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 福尔马林(蚁酸):加入足量饱和碳酸钠溶液充分振荡,蒸馏,收集馏出物 | |
| B. | 甘油(水):用分液漏斗分离 | |
| C. | 苯(苯酚):加NaOH溶液,充分振荡,分液 | |
| D. | 乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com