
有机物A可用作果实催熟剂,某同学欲以A为主要原符合成乙酸已酯,其合成路线如图所示.
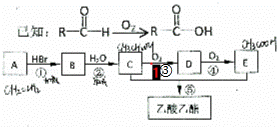
请回答:
(1)E的结构简式是 ,B分子中含有的官能团名称是 .
(2)反应①~⑤中反应类型与 相同的是 (填序号),B转化成A的反应条件是 .
(3)由A可以直接转化为C,其反应的化学方程式是 .
(4)反应③的化学方程式是 .
考点:有机物的推断.
分析:有机物A可用作果实催熟剂,A为CH2=CH2,A和HBr发生加成反应生成B为CH3CH2Br,溴乙烷发生取代反应生成C为CH3CH2OH,乙醇被氧化生成D为CH3CHO,乙醛进一步被氧化生成E为CH3COOH,乙醇与乙酸发生酯化反应生成乙酸乙酯,据此解答.
解答: 解:有机物A可用作果实催熟剂,A为CH2=CH2,A和HBr发生加成反应生成B为CH3CH2Br,溴乙烷发生取代反应生成C为CH3CH2OH,乙醇被氧化生成D为CH3CHO,乙醛进一步被氧化生成E为CH3COOH,乙醇与乙酸发生酯化反应生成乙酸乙酯.
(1)E的结构简式是CH3COOH,B为CH3CH2Br,含有的官能团名称是溴原子,故答案为:CH3COOH;溴原子;
(2)反应①~⑤中反应②⑤均属于取代反应,B转化成A发生卤代烃的水解反应,反应条件是:氢氧化钠醇溶液、加热,故答案为:⑤;氢氧化钠醇溶液、加热;
(3)乙烯与水发生加成反应可以直接转化为乙醇,反应的化学方程式是:CH2=CH2+H2O CH3CH2OH,故答案为:CH2=CH2+H2O
CH3CH2OH,故答案为:CH2=CH2+H2O CH3CH2OH;
CH3CH2OH;
(4)反应③的化学方程式是2CH3CH2OH+O2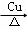 2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O,故答案为:2CH3CH2OH+O2 2CH3CHO+2H2O.
2CH3CHO+2H2O.
点评:本题考查有机物推断,涉及烯烃、卤代烃、醇、醛、羧酸和酯之间的转化,比较基础,注意对基础知识的理解掌握.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
24、(9分)A、B、C、D为前四周期元素。A元素的原子价电子排布为ns2np2,B元素的最外层电子数是其电子层数的3倍,C元素原子的M电子层的p亚层中有3个未成对电子,D元素原子核外的M层中只有2对成对电子。
 (1)当n=2时,AB2属于________分子(填“极性”或“非极性”),分子中有________个σ键,________个π键。
(1)当n=2时,AB2属于________分子(填“极性”或“非极性”),分子中有________个σ键,________个π键。
(2)当n=3时,A与B形成的晶体属于________晶体。
(3)若A元素的原子价电子排布为3s23p2,A、C、D三种元素的第一电离能由大到小的顺序是________________________(用元素符号表示)。
(4)已知某红紫色络合物的组成为[Co(NH3)5(H2O)]Cl3。该络合物中的中心离子钴离子在基态时核外电子排布式为________,作为配位体之一的NH3分子的空间构型为____________________。其中Co3+与NH3之间的作用力为 。
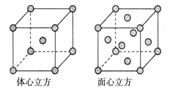
(5)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如下图所示。体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义。
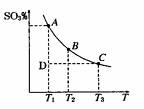 (1)硫酸生产过程中2SO2(g)+O2(g)
(1)硫酸生产过程中2SO2(g)+O2(g)  2SO3(g),平衡混合体系中SO3
2SO3(g),平衡混合体系中SO3
的百分含量和温度的关系如右图所示,根据右图回答下列问题:
①2SO2(g)+O2(g)  2SO3(g)的△H__________0(填“>”或“<”),
2SO3(g)的△H__________0(填“>”或“<”),
②一定条件下,将SO2与O2以体积比2:1置于一体积不变的密闭容器中
发生以上反应,能说明该反应已达到平衡的是 。
a.体系的密度不发生变化
b.SO2与SO3的体积比保持不变
c.体系中硫元素的质量百分含量不再变化
d.单位时间内转移4 mol 电子,同时消耗2 mol SO3
e.容器内的气体分子总数不再变化
(2)一定的条件下,合成氨反应为:N2(g)+3H2(g)  2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
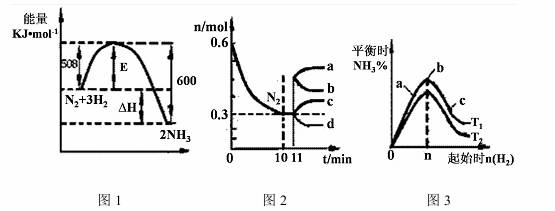
①该反应的平衡常数表达式为 ,升高温度,平衡常数 (填“增大”或“减小”或“不变”)。
②由图2信息,计算0~10min内该反应的平均速率v(H2)= ,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为 (填“a”或“b”或“c”或“d”)
③图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是 点,温度T1 T2(填“>”或“=”或“<”)
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物具有广泛的用途.下列说法不正确的是( )
A.能用于制作烈性炸药TNT的是甲苯
B.可用于杀菌消毒、制造阿司匹林的是苯酚
C.可用于食品调味剂的是乙酸
D.常用来焊接或切割金属的是苯
查看答案和解析>>
科目:高中化学 来源: 题型:
已知: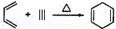 ,如果要合成
,如果要合成 ,所用的起始原料可以是( )
,所用的起始原料可以是( )
A.2﹣甲基﹣1,3﹣丁二烯和1﹣丁炔
B.1,3﹣戊二烯和2﹣丁炔
C.2,3﹣二甲基﹣1,3戊二烯和乙炔
D.2,3﹣二甲基﹣1,3﹣丁二烯和丙炔
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质间的转化关系中不能全部通过一步反应完成的是( )
A. Na→NaOH→Na2CO3→NaCl B. Mg→MgCl2→MgCO3→Mg(OH)2
C. Al→Al2O3→Al(OH)3→AlCl3 D. Fe→FeCl3→Fe(OH)3→Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
某校学生化学实验小组,为验证非金属元素氯的氧化性强于硫和氮,设计了一套实验装置:(部分夹持装置已略去)
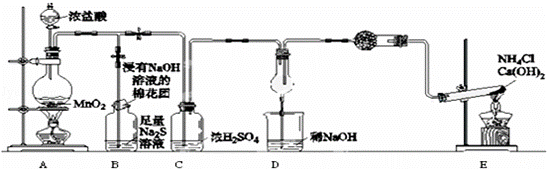
(1)写出A中反应的离子方程式 .
(2)B中出现黄色浑浊现象,产生此现象的离子方程式 .
(3)浸有NaOH溶液的棉花团的作用是 .
(4)D中干燥管中出现的明显现象及化学方程式是 ; 8NH3+3Cl2=6NH4Cl+N2 .
(5)有同学认为D中的现象并不能说明氯的氧化性大于氮,需要在C之前加装洗气装置,该洗气装置中盛装 试剂.
(6)还有什么方法能证明氧化性Cl2>S,(用化学方程式表示) .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com