
【题目】某班学生对BeCl2是离子化合物还是共价化合物进行集体探究,从经验看铍是金属元素,易失去电子,氯元素易得到电子,请回答以下问题:
(1)Be的电负性是1.5,Cl的电负性是3.0,则BeCl2应为_________化合物。
(2)工业上制取BeCl2方法是:将得到的BeCl2溶液在HCl气流中蒸干灼烧,防止BeCl2水解,请写出BeCl2水解的化学方程式__________________。
(3)经实验验证,熔融的BeCl2不能导电,说明它是_______化合物;BeCl2能溶于水,水溶液能导电,因它在溶液中能电离,写出它的电离方程式_________。
(4)在周期表中,铍元素和铝元素恰好处于对角线位置,根据对角线法则,判断BeCl2应与_____(填MgCl2或AlCl3)化学性质更相似。
(5)0.1mol氢氧化铍恰好能和100mL0.2mol/L的氢氧化钠溶液发生反应,写出反应的化学方程式_________________。
【答案】共价 BeCl2+2H2O![]() 2HCl+Be(OH)2(没有写可逆号给1分) 共价 BeCl2=Be2+ + 2Cl— AlCl3 Be(OH)2+2NaOH=Na2BeO2+2H2O
2HCl+Be(OH)2(没有写可逆号给1分) 共价 BeCl2=Be2+ + 2Cl— AlCl3 Be(OH)2+2NaOH=Na2BeO2+2H2O
【解析】
(1)Be的电负性为1.57,Cl元素的电负性3.0,差值小于1.7,Be和Cl形成共价键,BeCl2应为共价化合物
(2)BeCl2属于强酸弱碱盐水解生成氢氧化铍,BeCl2水解的化学方程式:BeCl2+2H2O![]() 2HCl+Be(OH)2;
2HCl+Be(OH)2;
(3)熔融的BeCl2不能导电,BeCl2含的化学键是共价键,不含离子键,所以是共价化合物;BeCl2在水分子作用下断裂共价键电离产生Be2+和Cl-电离方程式为:BeCl2═Be2++2Cl-,
(4)周期表中,铍元素和铝元素恰好处于对角线位置,根据对角线法则,BeCl2应与AlCl3性质更相似;
(5)依据对角线规则,氢氧化铍性质与氢氧化铝性质,氢氧化铝与强碱反应生成偏铝酸钠,所以氢氧化铍与氢氧化钠反应的化学方程式为:Be(OH)2+2NaOH═Na2BeO2+2H2O


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案科目:高中化学 来源: 题型:
【题目】烃A的产量能衡量一个国家石油化工发展水平,F的碳原子数为D的两倍,以A为原料合成F,其合成路线如图所示:

(1)写出决定B、D性质的重要原子团的名称:
B________、D________。
(2)A的结构式为____________。
(3)写出下列反应的化学方程式并注明反应类型:
①______________________,反应类型:_______;
②_________________,反应类型:________。
(4)实验室怎样区分B和D?___________。
(5)除去F中少量B和D的最好试剂是________(填字母)。
A 饱和碳酸钠溶液 B 氢氧化钠溶液 C 苯 D 水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得0.5 mol·L1CH3COONa溶液、0.5 mol·L1 CuSO4溶液以及H2O的pH随温度变化的曲线如图所示。下列说法正确的是

A. 随温度升高,纯水中c(H+)>c(OH)
B. 随温度升高,CH3COONa溶液的c(OH)减小
C. 随温度升高,CuSO4溶液的pH变化是Kw改变与水解平衡移动共同作用的结果
D. 随温度升高,CH3COONa溶液和CuSO4溶液的pH均降低,是因为CH3COO、Cu2+水解平衡移动方向不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是:
A.1 L 0.1 mol·L-1亚硫酸钠溶液含有的SO32-数目为0.1NA
B.标准状况下,5.6L O2和O3的混合气体含有的氧原子数为0.5NA
C.向FeI2溶液中通入适量Cl2,当有1 mol Fe2+被氧化时,转移电子的总数为NA
D.30g甲醛中含共用电子对总数为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
实验装置 | 部分实验现象 |
| a极质量减小,b极质量增加 |
| b极有气体产生,c极无变化 |
| d极溶解,c极有气体产生 |
| 电流计指示在导线中电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>dB.b>c>d>aC.d>a>b>cD.a>b>d>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应原理在科研和生产中有广泛应用。
(1)难挥发性TaS2可采用如下装置提纯:将不纯的TaS2粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中,反应如下:TaS2(s)+2I2(g)![]() TaI4(g)+S2(g),△H>0,下列说法正确的是:_____
TaI4(g)+S2(g),△H>0,下列说法正确的是:_____

A 在提纯过程中,I2的作用是将TaS2从高温区转移到低温区
B 改变压强,平衡不发生移动,所以反应放出的热量不变
C 加入催化剂,改变了反应的途径,反应的△H也随之改变
D 向容器中加入更多的TaS2(s)可以提高I2(g)的转化率
(2)在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中曲线所示。
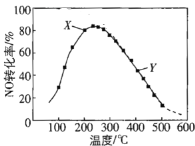
①下列说法不正确的是_____________。
A 反应2NO(g)+O2(g)![]() 2NO2(g),温度升高NO转化率增大说明正反应为吸热反应
2NO2(g),温度升高NO转化率增大说明正反应为吸热反应
B 图中X点所示条件下,延长反应时间能提高NO转化率
C 图中Y点所示条件下,增加O2的浓度能提高NO转化率
D 3800C下,C起始(O2)=5.0×10-4 mol·L-1,NO平衡转化率为50%,则平衡常数K<2000
②请在上图中画出不同温度下NO转化为NO2的平衡曲线_____。
(3)电解NO可制备NH4NO3,其工作原理如下图所示,为使电解产物全部转化为NH4NO3,需补充物质A,A是_________,写出电解过程的总反应化学方程式________。
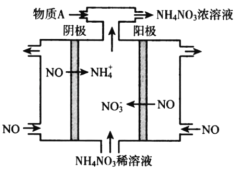
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四中某学习小组依据氧化还原反应原理:2Ag++Cu=Cu2++2Ag设计成的原电池如右图所示。
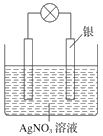
(1) 从能量转化角度分析,上述原电池将化学能转化为_________ ;
(2) 负极的电极材料为_____________;
(3) 正极发生的电极反应__________________________________;
(4) 假设反应初两电极质量相等,当反应进行到一段时间后(AgNO3溶液足量),取出两电极洗净干燥后称量,测得两电极质量差为11.2 g,则该时间内原电池反应转移的电子数为_____________。(设NA表示阿伏加德罗常数的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用如图所示装置进行实验,下列说法错误的是
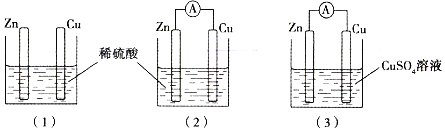
A. 若使图(1)装置中的Zn棒和Cu棒直接接触,则Cu棒上能看到有气体产生
B. 图(2)装置中SO42-向着Zn棒移动
C. 若将图(2)装置中Zn改为Mg,则Cu棒上产生气体的速率加快
D. 当图(2)装置与图(3)装置中正极生成物的质量比为1∶16时,两装置中Zn棒减轻的质量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
2Z(g) ΔH<0,一段时间后达到平衡。反应过程中测定的数据如下表:
下列说法正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A. 反应前2 min的平均速率v(Z)=2.0×10-3 mol·(L·min)-1
B. 其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C. 该温度下此反应的平衡常数K=1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com