
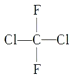
 (商品名称为氟里昂-12,一种限制使用的制冷剂,类似于甲烷的结构)的叙述正确的是( )
(商品名称为氟里昂-12,一种限制使用的制冷剂,类似于甲烷的结构)的叙述正确的是( )| A. | 有两种同分异构体 | B. | 是烷烃 | ||
| C. | 只有一种结构 | D. | 有四种同分异构体 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
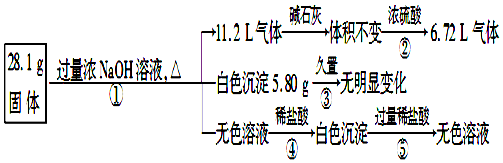
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
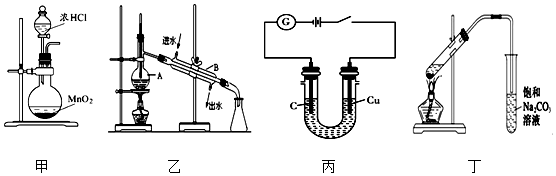
| A. | 利用装置甲制取氯气 | |
| B. | 利用装置乙分离乙酸(沸点:118℃)与乙酸乙酯(沸点:77.1℃) | |
| C. | 利用装置丙可电解食盐水制氯气和氢气 | |
| D. | 利用装置丁制取乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①⑤ | B. | ② | C. | ①④ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 现 象 | 解释或结论 | |
| A | SO2使酸性高锰酸钾溶液褪色 | SO2表现漂白性 |
| B | 向某溶液中加入BaCl2溶液和稀HNO3,若有白色沉淀生成 | 原溶液中含SO42- |
| C | 用铂丝蘸取某溶液在酒精灯火焰上灼烧直接观察火焰颜色,未见紫色 | 原溶液中不含K+ |
| D | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色. | Fe3+的氧化性比I2的强 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
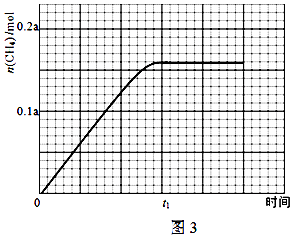
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
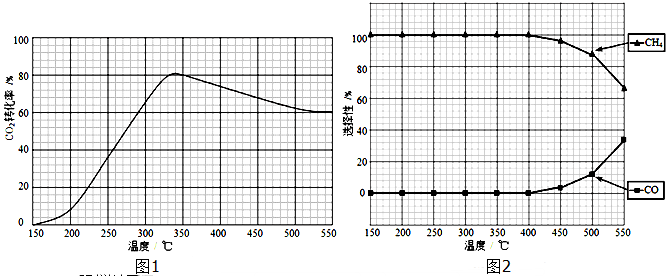
一定条件下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应:Fe(s) + CO2(g) FeO(s) + CO(g) ΔH>0。反应过程中CO2气体和CO气体的浓度与时间的关系如下图所示:
FeO(s) + CO(g) ΔH>0。反应过程中CO2气体和CO气体的浓度与时间的关系如下图所示:
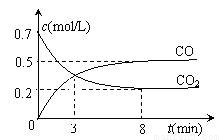
下列说法不正确的是
A.该反应的平衡常数表达式为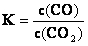
B.升高温度后达新平衡时,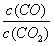 增大
增大
C.3分钟时,CO和CO2的浓度相等,反应达到平衡状态
D.8分钟内CO的平均反应速率v(CO)= 0.0625 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上教学质检化学试卷(解析版) 题型:选择题
瑞典皇家科学院曾将诺贝尔化学奖授予“手性碳原子的催化氢化、氧化反应”研究领域作出贡献的美、日三位科学家。下列分子中含有“手性碳原子”的是
A.CBr2F2 B.CH3CH(OH)COOH C.CH3CH2CH3 D.CH3CH2OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com