
【题目】下列措施一定能使化学反应速率降低的是( )
A.增大反应物的浓度
B.使用催化剂
C.降低温度
D.将块状固体变成粉末
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
【题目】燃料电池是将化学能转化为电能的装置,能量利用率高,环境友好.是未来能源领域发展的方向. 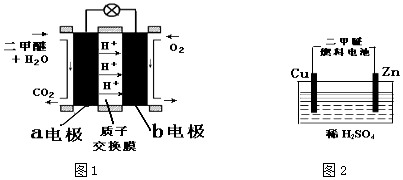
(1)图1左为绿色电源“二甲醚【(CH3)2O】燃料电池”的工作原理示意图.电池工作时,电子流动方向是 极经外电路到极((填a或b)),a电极上发生反应的电极反应式为 .
(2)连接图2装置的电源为(1)问中的二甲醚燃料电池.接通电源一段时间后,观察到装置中电解质溶液颜色由无色变为蓝色,并逐渐加深.则该装置中的Cu电极应与二甲醚燃料电池中 电极(填a或b)相连.通电时发生反应的总的离子反应方程式为:;若将电极材料都改为石墨,电解质溶液改为MnSO4溶液可以制备MnO2;则阳极反应式为;如二甲醚消耗23克,则理论上产生MnO2的质量为 克.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.催化剂是化工技术的核心,绝大多数的化工生产需采用催化工艺。
(1)新的研究表明,可以将CO2转化为炭黑进行回收利用,反应原理如图所示。
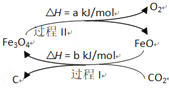
整个过程中Fe3O4的作用是________________________________。
(2)已知反应N2(g)+3H2(g)![]() 2NH3(g) ΔH<0。按n(N2)∶n(H2) = 1∶3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示:
2NH3(g) ΔH<0。按n(N2)∶n(H2) = 1∶3向反应容器中投料,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示:
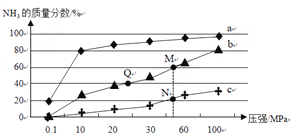
①下列说法正确的是__________。(填字母)
a.曲线a、b、c对应的温度是由低到高
b.加入催化剂能加快化学反应速率和提高H2的转化率
c.图中Q、M、N点的平衡常数:K(N)>K(Q)=K(M)
②M点对应H2的转化率是__________。
③2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如下:
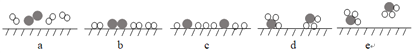
![]() 、
、![]() 和
和![]() 分别表示N2、H2和NH3。e表示生成的NH3离开催化剂表面,b和c的含义分别是____________和______________。
分别表示N2、H2和NH3。e表示生成的NH3离开催化剂表面,b和c的含义分别是____________和______________。
(3)有机反应中也常用到催化剂。某反应原理可以用下图表示,写出此反应的化学方程式_____________________________。
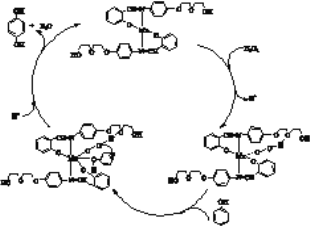
Ⅱ.过二硫酸钾(K2S2O8)在科研与工业上有重要用途。
(4)某厂采用湿法K2S2O8氧化脱硝和氨法脱硫工艺综合处理燃煤锅炉烟气,提高了烟气处理效率,处理液还可以用作城市植被绿化的肥料。一定条件下,NO去除率随温度变化的关系如图所示。80℃时,若NO初始浓度为450 mg·m-3,t min达到最大去除率,NO去除的平均反应速率:v(NO)=__________mol·L-1·Min-1(列代数式,不必计算结果)
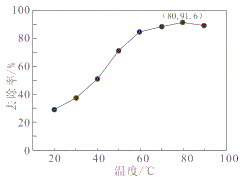
(5)过二硫酸钾可通过“电解→转化→提纯”方法制得,电解装置示意图如图所示。
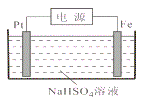
常温下,电解液中含硫微粒的主要存在形式与pH的关系如下图所示。
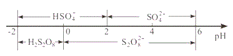
在阳极放电的离子主要是HSO4,阳极区电解质溶液的pH范围为___________,阳极的电极反应式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A. 原子最外层电子数为2的元素一定处于周期表第ⅡA族
B. 主族元素X、Y能形成XY2型化合物,则X与Y的原子序数之差可能为2或5
C. 氯化氢的沸点比氟化氢的沸点高
D. 同主族元素形成的氧化物的晶体类型均相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里……月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影……”月光穿过薄雾形成的种种美景本质原因是
A.雾是一种胶体B.空气中的小水滴颗粒的布朗运动
C.发生丁达尔现象D.空气中的小水滴颗粒直径大小约为1~100 nm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的密闭容器中,能判断反应X(s)+2Y(g) ![]() M(g)+N(g)达到最大限度的是( )
M(g)+N(g)达到最大限度的是( )
A. 压强不变
B. 生成M与N的物质的量之比为1:1
C. 生成1molM同时消耗2molY
D. 生成M的速率和消耗N的速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着材料科学的发展,金属钒及其化合物得到了越来越广泛的应用,并被誉为“合金维生素”。工业上回收废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,回收率达91.7%以上。该工艺的主要流程如图所示:
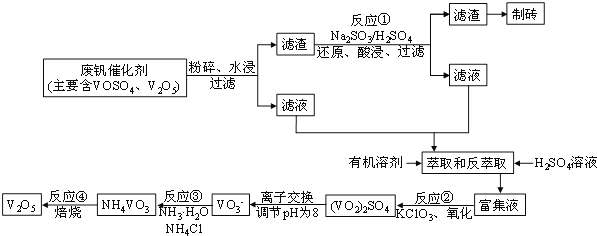
已知部分含钒物质在水中的溶解性如下表所示:
物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
请问答下列问题:
(1)工业上由V2O5冶炼金属钒常用铝热剂法,其化学方程式可表示为____。
(2)滤液中含钒的主要成分________(写化学式)。反应①的离子方程式___________________。
(3)萃取和反萃取过程中所需的主要玻璃仪器为_____________。若反萃取使用硫酸用量过大,进一步处理会增加_______(填化学式)的用量,造成成本增大。
(4)该工艺反应③的沉淀率(又称沉钒率)是回收钒的关键之一,写出该步发生反应的离子方程式___________________。“沉淀”过程中,沉钒率受温度、氯化铵系数(NH4Cl的质量与调节pH之后的料液中VO3-的质量比)等的影响,其中温度与沉钒率的关系如图所示,温度高于80℃沉钒率降低的可能原因是___________________________。

(5)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
结合上表,在实际生产中,③中加入氨水,调节溶液的最佳pH值为____。若矾沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)<_____。(已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39)
(6)废钒催化剂中V2O5的质量分数为6%(原料中的所有钒已换算成V2O5)。取100g此废钒催化剂按上述流程进行实验,当加入105mL 0.1molL-1的KClO3溶液时,溶液中的钒恰好被完全处理,假设以后各步钒没有损失,则该工业生产中钒的回收率是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨氮废水中的氮元素多以NH4+和NH3H2O的形式存在,在一定条件下,NH4+经过两步反应被氧化成NO3﹣ , 两步反应的能量变化示意图如图所示: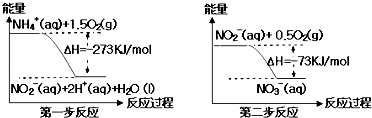
下列说法合理的是( )
A.该反应的催化剂是NO2﹣
B.升高温度,两步反应速率均加快,有利于NH4+ 转化成NO3﹣
C.在第一步反应中,当溶液中水的电离程度不变时,该反应即达平衡状态
D.1 mol NH4+在第一步反应中与1 mol NO2﹣在第二步反应中失电子数之比为1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物 ,在一定条件下可以相互转化。下列说法正确的是
,在一定条件下可以相互转化。下列说法正确的是
A. ①分子中的所有原子可以处于同一平面内
B. ①的同分异构体只有②和③
C. ①②③均能与H2发生加成反应
D. ③的一氯取代物和二氯取代物均只有2种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com