Fe和Al是两种常见的金属,将它们按一定的质量比组成混合物.
(1)取一定质量的该混合物,向其中加入足量NaOH溶液,生成气体在标准情况下的体积为aL,则反应的离子方程式为______;混合物中Al的物质的量为______(用含字母的数学式表示).
(2)另取相同质量的混合物,向其中加入足量稀硫酸,固体全部溶解,生成气体在标准状况下的体积为bL,则反应中转移电子的物质的量为______;混合物中Fe的质量为______(用含字母的数学式表示).
【答案】
分析:(1)铁和氢氧化钠不反应,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,根据氢气和铝之间的关系式计算铝的物质的量;
(2)该反应中稀硫酸作氧化剂,根据氢气和转移电子之间的关系式计算转移电子的物质的量,相同质量的铝与足量稀硫酸或氢氧化钠反应生成的氢气体积相同,再根据铁和氢气之间的关系式计算铁的质量.
解答:解:(1)铁和氢氧化钠不反应,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,离子反应方程式为2Al+2OH
-+2H
2O=2AlO
2-+3H
2↑,
设铝的物质的量为x,
2Al+2OH
-+2H
2O=2AlO
2-+3H
2↑
2mol 67.2L
x aL
x=
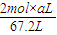
=
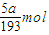
混合物中Al的物质的量为
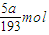
,
故答案为:2Al+2OH
-+2H
2O=2AlO
2-+3H
2↑;
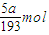
;
(2)该反应中转移电子数等于氢离子得到的电子数=
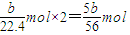
,相同质量的铝与足量稀硫酸或氢氧化钠反应生成的氢气体积相同,所以等质量的铝和稀硫酸反应生成氢气的体积是aL,则铁与稀硫酸反应生成氢气的体积=(b-a)L,
设铁的质量是y,
Fe+H
2SO
4=FeSO
4+H
2↑
56g 22.4L
y (b-a)L
y=
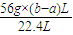
=2.5(b-a)g,
即转移电子的物质的量是
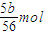
,铁的质量是2.5(b-a)g,
故答案为:
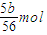
;2.5(b-a)g.
点评:本题考查化合物的有关计算、离子方程式的书写,注意铝和氢氧化钠溶液的反应中水参加反应,为易错点.

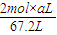 =
=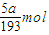
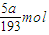 ,
,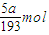 ;
;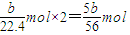 ,相同质量的铝与足量稀硫酸或氢氧化钠反应生成的氢气体积相同,所以等质量的铝和稀硫酸反应生成氢气的体积是aL,则铁与稀硫酸反应生成氢气的体积=(b-a)L,
,相同质量的铝与足量稀硫酸或氢氧化钠反应生成的氢气体积相同,所以等质量的铝和稀硫酸反应生成氢气的体积是aL,则铁与稀硫酸反应生成氢气的体积=(b-a)L,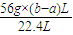 =2.5(b-a)g,
=2.5(b-a)g,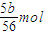 ,铁的质量是2.5(b-a)g,
,铁的质量是2.5(b-a)g,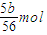 ;2.5(b-a)g.
;2.5(b-a)g.



