
����Ŀ����ҵ��ұ����ͭ��mCu2OnFeS���ɵõ���ͭ����ͭ���ᷴӦ�����������⣨��ͼ1�������������գ� 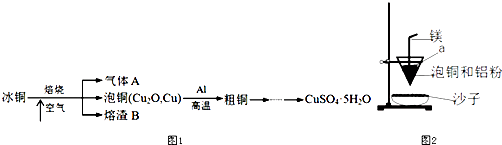
��1������A�еĴ�����Ⱦ���ѡ�������Լ��е�������ţ����գ�
a��ŨH2SO4 b��ŨHNO3 c��NaOH��Һ d����ˮ
��2��ʵ���ҿ�����ͼ2��װ�������ͭұ����ͭ�ķ�Ӧ��
����ͭұ����ͭ�Ļ�ѧ����ʽ����
��װ����þ������������
����ͭ�����ۻ������渲��������ɫ����a��a����
��3����H2S��O2���ܱ������е�ȼ����ַ�Ӧ��ָ���ԭ�����¶Ⱥ�ѹǿ��120�桢101kPa���������������30%����ԭ�����������H2S��������� �� ��������H2S�������ֽ⣩��֪����������ʱ��2H2S+O2 ![]() 2S+2H2O ��������ʱ��2H2S+3O2�T2SO2+2H2O��
2S+2H2O ��������ʱ��2H2S+3O2�T2SO2+2H2O��
��4����֪��SiCl4��s��+H2��g���TSiHCl3��s��+HCl��g����H1=47kJ/mol
SiHCl3��s��+H2��g���TSi��s��+3HCl��g����H2=189kJ/mol
����SiCl4�Ʊ�����Ȼ�ѧ����ʽΪ ��
���𰸡�
��1��cd
��2��3Cu2O+2Al ![]() 6Cu+Al2O3��ȼ�շų��������ȣ�������»���������ȼ����������أ���KClO3��
6Cu+Al2O3��ȼ�շų��������ȣ�������»���������ȼ����������أ���KClO3��
��3��0.6��0.7
��4��SiCl4��s��+2H2��g��=Si��s��+4HCl��g����H=+236kJ/mol
���������⣺��1.������AΪSO2 �� ���ü�Һ���գ���Ӧ��NaOH��ˮ�����Դ��ǣ�cd��
��2.����3Cu2O��Al�ڸ����·�Ӧ����Cu��Al2O3 �� ��Ӧ�ķ���ʽΪ3Cu2O+2Al ![]() 6Cu+Al2O3 ��
6Cu+Al2O3 ��
���Դ��ǣ�3Cu2O+2Al ![]() 6Cu+Al2O3��
6Cu+Al2O3��
��þ������ȼ���ã�ȼ�շų��������ȣ�������»����������������ȼ��������������������þ��ȼ�գ�
���Դ��ǣ�ȼ�շų��������ȣ�������»���������ȼ������
�۰�ɫ����Ϊ����أ���KClO3�������Դ��ǣ�����أ���KClO3����
��3.��2H2S+O2=2S+2H2O��a�� 2H2S+3O2=2SO2+2H2O��b����
�ɷ�Ӧ֪����H2S��O2��2��1ʱ������a�����У�����������ܼ���30%��
��2��1��H2S��O2��2��3ʱ���з�Ӧ��a�����з�Ӧ��b��������������ܼ���30%��
��ԭ���������H2S��O2�ֱ�Ϊx��yL��
2H2S | + | O2 | = | 2S | + | 2H2O | ����������� |
2y | y | 2y | y |
�� ![]() =0.3
=0.3 ![]() =
= ![]()
�� ![]() =0.7��
=0.7��
xH2S + yO2=��y�� ![]() ��SO2+��1.5x��y��S+xH2O �����������
��SO2+��1.5x��y��S+xH2O �����������
x y ��y�� ![]() ��
�� ![]()
�� ![]() =0.3
=0.3 ![]() =
= ![]()
�� ![]() =0.6
=0.6
���Դ��ǣ�0.6��0.7��
��4.����SiCl4��s��+H2��g���TSiHCl3��s��+HCl��g����H1=47kJ/mol
��SiHCl3��s��+H2��g���TSi��s��+3HCl��g����H2=189kJ/mol
�ɸ�˹���ɿ�֪��+�ڵõ�SiCl4��s��+2H2��g��=Si��s��+4HCl��g������H�T+236kJ/mol��
����SiCl4�Ʊ�����Ȼ�ѧ����ʽΪSiCl4��s��+2H2��g��=Si��s��+4HCl��g����H=+236kJ/mol��
���Դ��ǣ�SiCl4��s��+2H2��g��=Si��s��+4HCl��g����H=+236kJ/mol��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������þ���Ͻ�������������������Һ��Ӧ����3.36L�����������������ĸúϽ���ȫ����ϡ���ᣬ��Ӧ�����ᱻ��ԭֻ����4.48L��NO�����������������㵽��״�������ڷ�Ӧ�����Һ�У���������������������Һ�����ɳ���������Ϊ�� ��
A.11.4g
B.16.5g
C.9.7g
D.8.7g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ҫ֤��ij��Һ�в���Fe3+�����ܺ���Fe2+��������ʵ�����ʱ���˳��Ϊ ( )
�ټ���������ˮ �ڼ�������KMnO4��Һ �ۼ�������NH4SCN��Һ
A.�ۢ�B.�ۢ�C.�٢�D.�٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ij�л�����ӵļ������ģ�ͣ����л����к�C��H��O��N����Ԫ�أ����й��ڸ��л����˵���д�����ǣ� �� 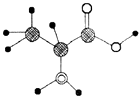
A.����ʽΪC3H7O2N
B.�ܷ���ȡ����Ӧ
C.��ͨ���ۺϷ�Ӧ���ɸ߷��ӻ�����
D.���л����ܸ�NaOH��Һ��Ӧ�������ܺ����ᷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�������CO2������ȼ�ϼ״����ȼ��ٶ�����̼���壬�ֵõ��������Դ���ʣ�Ϊ��̽����Ӧԭ�����ֽ�������ʵ�飺�����Ϊ1L���ܱ������У�����1molCO2��3molH2 �� ij�¶��·�����Ӧ��CO2��g��+3H2��g���TCH3OH��g��+H2O��g����H=��49.0KJ/mol�����CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ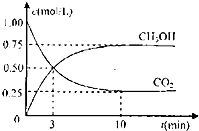
��1���÷�Ӧ���¶��£���ѧƽ�ⳣ����ֵΪ
��2������˵��������Ϊ��Ӧ�ﵽƽ��״̬��־����������ĸ����
A.������ѹǿ���ٷ����仯
B.ƽ����Է����������ٱ仯
C.c��CO2����c��H2��֮�ȵ���1��3
D.��ͬʱ����ÿ����3molH��H����ͬʱ����3molO��H��
��3�����д�ʩ����ʹ ![]() ��С����
������
A.�ٳ���1molCO2��3molH2
B.��H2O��g������ϵ�з���
C.����He��g����ʹ��ϵѹǿ����
D.�����¶ȣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й��������ʵıȽϣ��������
A.�۵㣺���� > ����B.�ܶȣ������� > ˮ
C.���ȶ��ԣ�С�մ� < �մ�D.̼̼����������ϩ > ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�к���Ba2����Cu2����Ag��������NaOH��Һ�������Na2SO4��Һ��������������һ�������롣������ͼ��ͼ����

(1)�����Ļ�ѧʽ������1________������2________������3___ ____��
(2)д�����Һ��A�����ӷ���ʽ________________����Һ��B�����ӷ���ʽ__________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йر�ʾ��ȷ���ǣ� ��
A.�������ƣ�CaO2���ĵ���ʽ�� ![]()
B.ij���Ľṹʾ���ͼΪ ![]() �����Ԫ�������ڱ���λ�ڵ������ڡ�VIA��
�����Ԫ�������ڱ���λ�ڵ������ڡ�VIA��
C.H2CO3�ĵ��뷽��ʽ��H2CO32H++CO32��
D.�����ǵĽṹ��ʽ��C6H12O6
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com