
下列说法正确的是:
A. 分子中一定存在共价键
B. 在共价化合物分子中一定存在σ键
C. Na3[AlF6]、Na2[SiF6]和[Cu(NH3)4]Cl2的配位数都是6
D. 共价键键长越短,键能一定越大
科目:高中化学 来源:2017届山东省济南市高三第一次模拟考试理科综合化学试卷(解析版) 题型:选择题
25℃时,向20mL 0.1mol/LH2R(二元弱酸)溶液中滴加0.1mol/LNaOH溶液,溶液pH与加入NaOH溶液体积的关系如图所示。下列有关说法正确的是

A. a点所示溶液中:c (H2R) + c (HR-)+ c (R2-)=0.lmol/L
B. b点所示溶液中:c (Na+) >c(HR-)> c (H2R)>c(R2-)
C. 对应溶液的导电性:b > c
D. a、b、c、d中,d点所示溶液中水的电离程度最大
查看答案和解析>>
科目:高中化学 来源:宁夏勤行校区2016-2017学年高二下学期第一次(3月)月考化学试卷 题型:选择题
已知具有相同价电子数和相同原子数的分子或离子具有相同的结构,这一原理称为“等电子原理”。根据等电子原理,下列各组粒子结构不相似的是( )
A. BCl3和PH3 B. NH4+和CH4 C. NO3-和CO32- D. CO2和N2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省大同市高二3月月考化学试卷(解析版) 题型:选择题
当向蓝色的硫酸铜中逐滴加入氨水,观察到溶液呈深蓝色时,再通入SO2气体,生成了白色沉淀。将白色沉淀加入稀硫酸中,又生成了红色粉末状固体和SO2气体,同时溶液呈蓝色。根据上述实验现象分析推测,下列描述正确的是
A. Cu2+和Ag+相似,能与NH3结合生成铜氨配离子
B. 白色沉淀为+2价铜的某种亚硫酸盐,溶于H2SO4发生复分解反应
C. 白色沉淀为+1价铜的某种硫酸盐,在酸性条件下发生了自身氧化还原反应
D. 反应过程中消耗的SO2与生成的SO2的物质的量相等
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省大同市高二3月月考化学试卷(解析版) 题型:选择题
下列物质中不存在氢键的是( )
A.冰醋酸中醋酸分子之间
B.液态氟化氢中氟化氢分子之间
C.一水合氨分子中的氨分子与水分子之间
D.可燃冰(CH4·8H2O)中甲烷分子与水分子之间
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省大同市高二3月月考化学试卷(解析版) 题型:选择题
已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是
A. 质子数c>d,离子的还原性Y2->Z-
B. 氢化物的稳定性H2Y>HZ
C. 原子半径X<W,第一电离能X<W
D. 电负性Z>Y>W>X
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆第二外国语学校高一下学期3月份月考化学试卷(解析版) 题型:选择题
下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是( )
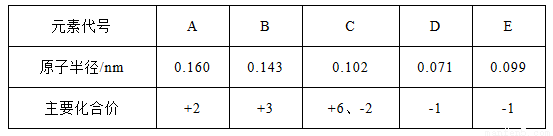
A. 简单离子半径大小关系为B3+>A2+
B. 气态氢化物的稳定性HD<H2C
C. 形成的简单离子的还原性E->D-
D. 最高价氧化物对应的水化物的酸性H2CO4>HEO4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南师范大学附属中学高一下学期第一次阶段性测试化学试卷(解析版) 题型:填空题
下图是元素周期表的一部分(1~36号元素),试回答下列问题:

(1)D的元素符号是_______;H代表的元素在周期表中的位置是________。
(2)F、G、I、K、M对应的简单离子的半径由大到小的顺序是________(用离子符号表示)。
(3)请写出MY2的电子式:______。
(4)常温常压下,上表中的元素对应的单质为有色且是气态的有_________。
(5)X的非金属性_____于J(填“强”或“弱”),请用化学方程式证明上述结论______。
(6)元素B和L形成的化合物的水溶液与元素K的单质反应的离子方程式为_________,反应后,向溶液中加人X、K形成的化合物溶液,现象为:____________。
查看答案和解析>>
科目:高中化学 来源:2017届贵州省凯里市高三3月联考理综化学试卷(解析版) 题型:简答题
磷存在于人体所有细胞中,是维持骨骼和牙齿的必要物质,几乎参与所有生理上的化学反应。回答下列问题:
(1)基态P原子的核外电子排布式为__________,有______个未成对电子。写出磷及其同周期相邻元素第一电离能的大小顺序_________。
(2)磷的一种同素异形体——白磷(P4)的其键角为_________,推测其在CS2中的溶解度___________(填“大于”或“小于”)在水中的溶解度
(3)两种三角锥形气态氢化物膦(PH3)和氮(NH3)的键角分别为93.6°和107°,试分析PH3、的键角小于NH3的原因_________。写出一种与互为等电子体的阳离子_________。
(4)PCl3中心原子杂化轨道类型为________,VSEPR 模型为_______。
(5)磷化硼(BP)是一种超硬耐磨涂层材料,下图为其立方体晶胞,其中的每个原子均满足8电子稳定结构,试判断其熔点______(填“高于”或“低于”)金刚石熔点。
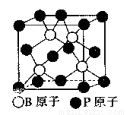
已知其B-P键长均为x cm,则其密度为_____g/cm3(列出计算式即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com