
在密闭容器中,充入SO2和18O原子组成的氧气,在一定条件下开始反应,在达到平衡后,18O存在于( )
A.只存在于氧气中 B.只存在于SO3中
C.只存在于SO2和SO3中 D.SO2、SO3、O2中都存在
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
某化学兴趣小组对电化学问题进行了实验研究。
(1)利用下图装置探究金属的电化学腐蚀,接通电路发现灵敏电流计指针发生偏转,盐桥中K+向______槽(填“a”或“b”或“c”)移动。写出正极的电极反应_________________________。
(2)如何检验a槽中生成的阳离子________________________________________。
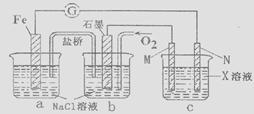
(3)在c槽中欲实现Cu+2H2O=Cu (OH)2+H2↑的反应,则电极_________(填"M"或“N")一定是铜电极。c槽中电解质X可以是下列_________________物质(填选项)
A. H2SO4 B. NaNO3 C. MgCl2 D. KOH
查看答案和解析>>
科目:高中化学 来源: 题型:
右图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系。该溶液的成分可能是 ( )

A.NH4Al(SO4)2 B.KAl(SO4)2
C.Al2(SO4)3 D.NaAlO2
查看答案和解析>>
科目:高中化学 来源: 题型:
烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝溶液,并用于烟气脱硫。
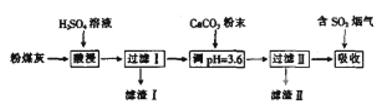
(1) (“能”或“不能”)用NaOH溶液代替H2SO4溶液。
(2)酸浸时反应的离子方程式为
(3)加CaCO3调节溶液的pH至3.6,其目的是 。Al2(SO4)x(OH)6-2x______(填“易”或“难”)于水。
(4)已知粉煤灰中Al2O3的质量分数为40.8%,制得的碱式硫酸铝【Al2(SO4)x(OH) 6-2x】中x=1.5.某实验小组取80.0g粉煤灰进行上述实验,假设在整个过程中铝的损耗率为10%,则可制得碱式硫酸铝的质量为__________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
1)反应aA(g)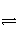
 bB(g)+cC(g)在一容积不变的容器内进行,反应达到平衡后(以下填“增大”、“减小”或“不变”):
bB(g)+cC(g)在一容积不变的容器内进行,反应达到平衡后(以下填“增大”、“减小”或“不变”):
①若a=b+c,增大A的浓度,A的转化率________。
②若a>b+c,增大A的浓度,A的转化率________。
(2)若反应aA(g)+bB(g)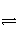
 cC(g)+dD(g),容器体积固定不变,且起始时A与B的物质的量之比为a∶b。
cC(g)+dD(g),容器体积固定不变,且起始时A与B的物质的量之比为a∶b。
①平衡时A与B的转化率之比是________。
②若增大A的浓度,则A的转化率________。
③若同时同等倍数地增大A、B的浓度,则a+b与c+d满足什么关系时,A与B的转化率同时增大?a+b______c+d(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家预言超级原子的发现将会重建周期表,2005年1月美国科学家在《Science》上发表论文,宣布发现了A1的超原子结构A113和A114,并在质谱仪检测到稳定的A113I一等,Al13、Al14的性质很像现行周期表中的某主族元素,己知这类超原子当具有40个价电子时最稳定(例Al原子具有3个价电子)。下列说法不正确的是
A. Al14有42个价电子,且与IIA族元素性质相似
B. Al13有39个价电子,且与卤素性质类似
C. Al13在气相中与HI反应可生成H Al13I,且化学
方程式为 AI13+HI=H AI13I
D. Al13原子中A1原子间是通过离子键结合的
查看答案和解析>>
科目:高中化学 来源: 题型:
CO和H2的混合气体俗称合成气,是一种重要的工业原料气,工业上利用天
然气(主要成分为CH4)与水进行高温重整制备合成气。
⑴ 已知:CH4、H2和CO的燃烧热(△H)分别为-890.3kJ/mol、-285.8kJ/mol和
-283.0kJ/mol,且1mol液态水汽化时的能量变化为44.0kJ。用1 m3(标准状况)的
甲烷与水蒸气在高温下反应制取合成气所需的热量为 (保留整数)。
⑵ 在一定温度下,向体积为2L的密闭容器中充入0.40mol CH4和0.60mol H2O(g),测得
CH4(g)和H2(g)的物质的量浓度随时间变化如下表所示:
|

 | 0 | 1 | 2 | 3 | 4 | ||||||
| CH4 | 0.2mol·L-1 | 0.13 mol·L-1 | 0.1 mol·L-1 | 0.1 mol·L-1 | 0.09 mol·L-1 | ||||||
| H2 | 0 mol·L-1 | 0.2 mol·L-1 | 0.3 mol·L-1 | 0.3 mol·L-1 | 0.33 mol·L-1 |
①计算该反应第一次达平衡时的平衡常数K 。
②3min时改变的反应条件是 (只填一种条件的改变即可)。
⑶ 已知温度、压强、投料比X对该反应的影响如图所示。
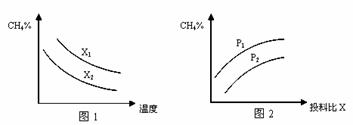
①图1中的两条曲线所示投料比的关系X1 X2(填“=”、“>”或“<”下同)。
②图2中两条曲线所示的压强比的关系:P1 P2。
⑷ 以天然气(设杂质不参与反应)、KOH溶液为原料可设计成燃料电池:
①放电时,负极的电极反应式为 。
②设装置中盛有100.0mL 3.0mol/L KOH溶液,放电时参与反应的氧气在标准状况下
的体积为8.96L,放电过程中没有气体逸出,则放电完毕后,所得溶液中各离子浓度由大到小的关系为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨工艺的一个重要工序是铜洗,其目的是用铜液[醋酸二氨合铜(I)、氨水]吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应是放热反应,其反应方程式为: Cu(NH3)2Ac+CO+NH3 [Cu(NH3)3CO]Ac 。完成下列填空:
[Cu(NH3)3CO]Ac 。完成下列填空:
(1)如果要提高上述反应的反应速率,可以采取的措施是 。(选填编号)
a.减压 b.增加NH3的浓度 c.升温 d.及时移走产物
(2)铜液中的氨可吸收二氧化碳,写出该反应的化学方程式_____________________
(3)铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为__________________。通过比较_____________________________可判断氮、磷两种非金属元素的非金属性强弱。
(4)已知CS2与CO2分子结构相似,CS2的电子式是_________________。CS2熔点高于CO2,其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com