
【题目】锶有“金属味精”之称。以天青石(主要含有SrSO4和少量CaCO3、MgO杂质)生产氢氧化锶的工艺如下:

已知氢氧化锶在水中的溶解度:
温度(℃) | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
溶解度(g/100mL) | 0.91 | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(1)隔绝空气焙烧时SrSO4只被还原成SrS,化学方程式为____。
(2)“除杂”方法:将溶液升温至95℃,加NaOH溶液调节pH为12。
①95℃时水的离子积KW=1.0×10-12,Ksp[Mg(OH)2]=1.2×10-10,则溶液中c(Mg2+)=____。
②若pH过大,将导致氢氧化锶的产率降低,请解释原因____。
(3)“趁热过滤”的目的是____,“滤渣”的主要成分为___。
(4)从趁热过滤后的滤液中得到Sr(OH)2产品的步骤为____、过滤、洗涤、干燥。
(5)“脱硫”方法:用FeCl3溶液吸收酸浸产生的气体,吸收时的氧化产物为___(填化学式);再用石墨电极电解吸收液,电解后可在“脱硫”中循环利用的物质是__。
【答案】 SrSO4+ 4C![]() SrS + 4CO↑ 1.2×10-10 molL-1 OH-对氢氧化锶的溶解起抑制作用,OH-浓度过大,将使氢氧化锶沉淀析出 防止温度降低使氢氧化锶析出而造成损失 Ca(OH)2、Mg(OH)2 降温结晶 S FeCl3
SrS + 4CO↑ 1.2×10-10 molL-1 OH-对氢氧化锶的溶解起抑制作用,OH-浓度过大,将使氢氧化锶沉淀析出 防止温度降低使氢氧化锶析出而造成损失 Ca(OH)2、Mg(OH)2 降温结晶 S FeCl3
【解析】(1)根据图中信息,隔绝空气焙烧时SrSO4只被碳还原成SrS,同时生成一氧化碳,反应的化学方程式为:SrSO4+ 4C![]() SrS + 4CO↑;(2)①95℃时水的离子积KW=1.0×10-12,pH为12,c(H+)=10-12mol/L,
SrS + 4CO↑;(2)①95℃时水的离子积KW=1.0×10-12,pH为12,c(H+)=10-12mol/L,
c(OH-)=![]() =1mol/L,c(Mg2+)=
=1mol/L,c(Mg2+)=![]() =
=![]() =1.2×10-10 molL-1;②OH-对氢氧化锶的溶解起抑制作用,OH-浓度过大,将使氢氧化锶沉淀析出,导致氢氧化锶的产率降低;(3)“趁热过滤”的目的是防止温度降低使氢氧化锶析出而造成损失,“滤渣”的主要成分为在碱性条件下沉淀下来的Mg(OH)2和微溶物Ca(OH)2;(4)从趁热过滤后的滤液中得到Sr(OH)2产品的步骤为降温结晶、过滤、洗涤、干燥;(5)“脱硫”方法:用FeCl3溶液吸收酸浸产生的气体,铁离子将硫离子氧化为硫单质,吸收时的氧化产物为S;再用石墨电极电解吸收液,电解过程将氯化亚铁氧化为氯化铁,故电解后可在“脱硫”中循环利用的物质是FeCl3。
=1.2×10-10 molL-1;②OH-对氢氧化锶的溶解起抑制作用,OH-浓度过大,将使氢氧化锶沉淀析出,导致氢氧化锶的产率降低;(3)“趁热过滤”的目的是防止温度降低使氢氧化锶析出而造成损失,“滤渣”的主要成分为在碱性条件下沉淀下来的Mg(OH)2和微溶物Ca(OH)2;(4)从趁热过滤后的滤液中得到Sr(OH)2产品的步骤为降温结晶、过滤、洗涤、干燥;(5)“脱硫”方法:用FeCl3溶液吸收酸浸产生的气体,铁离子将硫离子氧化为硫单质,吸收时的氧化产物为S;再用石墨电极电解吸收液,电解过程将氯化亚铁氧化为氯化铁,故电解后可在“脱硫”中循环利用的物质是FeCl3。


科目:高中化学 来源: 题型:
【题目】在实验室里可用如图所示装置来制取氯酸钠、次氯酸钠和探究氯水的性质. 图中:
①为氯气发生装置;
②的试管里盛有15mL30%NaOH溶液来制取氯酸钠,并置于热水浴中;
③的试管里盛有15mL8%NaOH溶液来制取次氯酸钠,并置于冰水浴中;
④的试管里加有紫色石蕊试液;
⑤为尾气吸收装置.
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过(仪器名称)向烧瓶中加入适量的浓盐酸.实验室制Cl2的化学方程式为; 实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有(填写下列编号字母)的净化装置.
A.碱石灰 B.氢氧化钠溶液 C.饱和食盐水 D.浓硫酸
(2)如果将过量二氧化锰与20mL12molL﹣1的浓盐酸混合加热,充分反应后生成的氯气0.06mol.(填“大于”“小于”或“等于”),若有17.4g的MnO2被还原,则被氧化的HCl的物质的量为 .
(3)写出装置②中发生反应的化学方程式 .
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白.
实验现象 | 原因 |
溶液最初从紫色逐渐变为红色 | 氯气与水反应生成的H+使石蕊变色 |
随后溶液逐渐变为无色 | |
然后溶液从无色逐渐变为色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素周期表的叙述,错误的是
A. 镁是第IIA族元素
B. 第IA族元素全部是金属元素
C. 氧族中含金属元素
D. 第3周期中既有金属元素又有非金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原子结构的叙述正确的是
A. 所有的原子核都是由质子和中子组成的
B. 原子的最外层电子数可以超过8个
C. 稀有气体的最外层电子数均为8
D. 所有主族元素的最外层电子数都等于其主族序数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO | H2SO3 |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 | K1=1.5×10-2 K2=1.1×10-7 |
请回答下列问题:
(1)写出碳酸的第一级电离平衡常数表达式:K1=_______________________。
(2)CH3COOH、H2CO3、HClO、H2SO3的酸性由强到弱的顺序为____________________。
(3)室温下,向10mL0.1mol/L醋酸溶液中加水稀释后,下列说法正确的是(_______)。
A.溶液中导电粒子的数目减少
B.再加入CH3COONa固体能促进醋酸的电离
C.醋酸的电离程度增大,H+的数目亦増大
D.溶液中![]() 不变
不变
E.再加入10 mL c(OH-)=10-1 mol·L-1的NaOH溶液,醋酸与NaOH恰好中和
(4)物质的量浓度相同的四种溶液CH3COONab.Na2SO3c.NaClOd.NaHCO3
pH由小到大排列的顺序是_______________(用编号填写)
(5)物质的量浓度相同的四种溶液a.CH3COONH4,b.NH4HCO3,c.(NH4)2CO3,d.NH4HSO3,C(NH4+)由小到大的顺序是_______________(用编号填写)
(6)写出向NaClO溶液中通入少量CO2的化学方程式____________________________________。
(7)下列化学方程式一定错误的有(_______)
A.2NaHCO3+SO2=Na2SO3+CO2
B.CH3COOH+Na2SO3=CH3COONa+NaHSO3
C.NaClO+SO2+H2O=HClO+NaHSO3
D.CH3COOH+Na2CO3=CH3COONa+NaHCO3
(8)室温下,对于c(ClO-)=0.1 mol·L-1的Ca(ClO)2溶液,下列判断中正确的是(____)。
A. 加水稀释后,溶液中![]() 增大
增大
B. 溶液中c(ClO-)>c(HClO)>c(OH-)>c(H+)
C. 溶液中c(Ca2+)+c(H+)=c(ClO-)+c(OH-)
D. 若溶液的pH=12,则ClO-的水解百分率为10%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在CH3COOH溶液中存在如下平衡:CH3COOHCH3COO-+H+。加入少量下列物质或采取下述方法,能使平衡逆向移动的是( )
A. 加水 B. 升温
C. CH3COONa固体 D. NaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O.如图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好.下表中由实验现象得出的结论完全正确的是( )
选项 | 实验现象 | 结论 |
A | 滴有KSCN的FeCl2溶液变红 | Cl2具有还原性 |
B | 滴有酚酞的NaOH溶液褪色 | Cl2具有酸性 |
C | 石蕊试液先变红后褪色 | Cl2具有漂白性 |
D | KI淀粉溶液变蓝 | Cl2具有氧化性 |

A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气及其相关产品是基本化工原料,在化工领域中具有重要的作用。
(1)以铁为催化剂,0.6mol氮气和1.8mol氢气在恒温、容积恒定为1L的密闭容器中反应生成氨气,20min后达到平衡,氮气的物质的量为0.3mol。
①在第25min时,保持温度不变,将容器体积迅速增大至2L并保持恒容,体系达到平衡时N2的总转化率为38.2%,请画出从第25min起H2的物质的量浓度随时间变化的曲线_____。
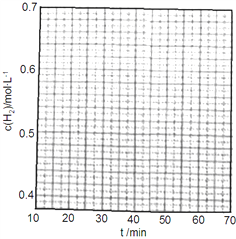
②该反应体系未达到平衡时,催化剂对逆反应速率的影响是_____(填增大、减少或不变)。
(2)①N2H4是一种高能燃料,有强还原性,可通过NH3和NaClO反应制得,写出该制备反应的化学方程式______________________。
②N2H4的水溶液呈弱碱性,室温下其电离常数K1=1.0×10-6,则0.01 mol·L-1 N2H4水溶液的pH等于__________(忽略N2H4的二级电离和H2O的电离)。
③已知298K和101KPa条件下:
N2(g)+3H2(g)=2NH3(g) ΔH1
2H2(g)+O2(g)=2H2O(l) ΔH2
2H2(g)+O2(g)=2H2O(g) ΔH3
4NH3(g)+O2(g)=2N2H4(l)+2H2O(I) ΔH4
则N2H4(l)的标准燃烧热ΔH=_______。
(3)科学家改进了NO2转化为HNO3的工艺(如虚框所示),在较高的操作压力下,提高N2O4/H2O的质量比和O2的用量,能制备出高浓度的硝酸。
![]()
实际操作中,应控制N2O4/H2O质量比高于5.11,对此请给出合理解释______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com