
| A. | 乙烯分子中碳碳键的键能是乙烷分子中碳碳键的2倍,因而乙烯比乙烷稳定 | |
| B. | 石油裂化的目的是为了将直链烃转化为芳香烃 | |
| C. | 分子式为C4H8O2的有机物,存在含有六元环的同分异构体 | |
| D. | 有机物  不能发生氧化反应,但可以发生消去反应、取代反应和加成反应 不能发生氧化反应,但可以发生消去反应、取代反应和加成反应 |
分析 A.烯分子中碳碳双键的键能小于乙烷分子中碳碳单键键能的两倍,碳碳双键易断裂;
B.石油裂化的目的是为了提高轻质液体燃料的产量和质量;
C.可为环状化合物;
D.含有酚羟基,可被氧化.
解答 解:A.烯分子中碳碳双键的键能小于乙烷分子中碳碳单键键能的两倍,不稳定,易断裂,故A错误;
B.石油裂化的目的是为了提高轻质液体燃料的产量和质量,得到短链烃,不能得到芳香烃,故B错误;
C.存在分子中含有六元环的同分异构体: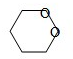 ,故C正确;
,故C正确;
D.含有酚羟基,可被氧化,故D错误.
故选C.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 硅晶体是良好的半导体,可用于制造光导纤维 | |
| B. | 高压钠灯发出的黄光透雾能力强,可用于道路和广场照明 | |
| C. | 生石灰能与水反应,可用于除去HC1气体中少量的水蒸气 | |
| D. | 氢氧化钠具有强碱性,可用于制胃酸中和剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫化锌(ZnS)晶体用作分析试剂、荧光体、光导体材,久置湿空气中易被氧化为ZnSO4.回答下列问题:
硫化锌(ZnS)晶体用作分析试剂、荧光体、光导体材,久置湿空气中易被氧化为ZnSO4.回答下列问题:| ZnF2 | ZnCl2 | ZnBr2 | ZnI2 | |
| 熔点/℃ | 872 | 275 | 394 | 446 |
| 在乙醇、乙醚中溶解性 | 不溶 | 溶解 | 溶解 | 溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
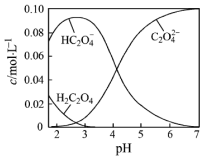 H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定不正确的是( )
H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定不正确的是( )| A. | pH=7的溶液中:c(Na+)>2c(C2O42-) | |
| B. | c(Na+)=0.100 mol•L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+c(C2O42-) | |
| C. | c(HC2O4-)=c(C2O42-)的溶液中:c(Na+)>0.100 mol•L-1+c(HC2O4-) | |
| D. | c(HC2O4-)=c(C2O42-)的点的坐标为(4.3,0.5),则Na2C2O4的水解平衡常数为Kh=1×10-9.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 羽绒服中的鸭绒和羽绒棉的主要成分都是蛋白质 | |
| B. | 在食品袋中放入装有生石灰和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| C. | 含氮、磷的污水是很好的肥料,可直接排放到自然界水体中用于灌溉庄稼 | |
| D. | 煤燃烧排放的废气中含大量CO2、SO2,是形成“硫酸型”酸雨的主要原因 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 事实或现象 | 结论 |
| A | 某钾盐中滴加盐酸,产生使澄清石灰水变浑浊的无色气体 | 该钾盐是K2CO3或KHCO3 |
| B | 加热蒸干MgSO4溶液能得到MgSO4固体;加热蒸干MgCl2溶液得不到MgCl2固体 | H2SO4不易挥发,HCl易挥发 |
| C | 常温下,向相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中的铝片先溶解完 | 反应物的浓度越大,反应速率越快 |
| D | NH3沸点低于PH3 | 结构和组成相似的物质,沸点随相对分子质量增大而升高 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
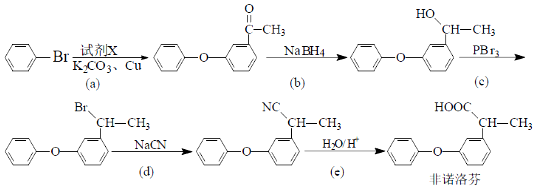
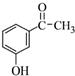 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火 | |
| B. | 为准确配制一定物质的量浓度的溶液,定容过程中向容量瓶内加蒸馏水至接近刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至刻度线 | |
| C. | 蒸馏完毕后,应先停止加热,待装置冷却后,停止通水,再拆卸蒸馏装置 | |
| D. | 探究温度对硫代硫酸钠与硫酸反应速率的影响时,若先将两种溶液混合并计时,再用水浴加热至设定温度,则测得的反应速率偏高 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com