
 ��������ҽԺ���õ�����������������ǿ�ҵĸ�ʴ���ã��ܸ�ʴƤ�������ܣ���ʹ�����ʱ��ԣ����Ա���С��ʹ�ã���ѧ��ѧ����Ũ��ˮ���鱽�ӣ���д���÷�Ӧ�Ļ�ѧ����ʽ
��������ҽԺ���õ�����������������ǿ�ҵĸ�ʴ���ã��ܸ�ʴƤ�������ܣ���ʹ�����ʱ��ԣ����Ա���С��ʹ�ã���ѧ��ѧ����Ũ��ˮ���鱽�ӣ���д���÷�Ӧ�Ļ�ѧ����ʽ ��
������ ��ϩ���Ӽ䷢���ӳɾۺϷ�Ӧ���ɸ߷��ӻ��������ϩ��
��������ˮ��Ӧ���DZ��ӷ������ǻ��Ա���Ӱ�죬�ڶ�λ��ԭ�ӻ��ã�����ȡ����
����������ȩ������ͬ�Ĺ�����ȩ����ȩ���Ļ�ԭ�Ա�������������Ϊ�������ᣬ������������Ӧ��
��� �⣺��ϩ���Ӽ䷢���ӳɾۺϷ�Ӧ���ɸ߷��ӻ��������ϩ����Ӧ�Ļ�ѧ����ʽΪ�� ��
��
������Ũ��ˮ��Ӧ���DZ��ӷ������ǻ��Ա���Ӱ�죬�ڶ�λ��ԭ�ӻ��ã�����ȡ����Ӧ�Ļ�ѧ����ʽΪ�� ��
��
����������ȩ������ͬ�Ĺ�����ȩ��������������Ӧ����ȩ���Ļ�ԭ�Ա�������������Ϊ�������ᣬ������������Ӧ����Ӧ�Ļ�ѧ����ʽΪ��CH2OH��CHOH��4CHO+2Ag��NH3��2OH$\stackrel{ˮԡ}{��}$CH2OH��CHOH��4COONH4+2Ag��+3NH3+H2O��
�ʴ�Ϊ�� ��
�� ��CH2OH��CHOH��4CHO+2Ag��NH3��2OH$\stackrel{ˮԡ}{��}$CH2OH��CHOH��4COONH4+2Ag��+3NH3+H2O��
��CH2OH��CHOH��4CHO+2Ag��NH3��2OH$\stackrel{ˮԡ}{��}$CH2OH��CHOH��4COONH4+2Ag��+3NH3+H2O��
���� ���⿼���˷���ʽ����д�����ݷ�Ӧ�������ͷ�Ӧ������д����ʽ����ȷ�����Ļ�ѧ��Ӧԭ���ǽ����Ĺؼ���ע�ⳣ���л�������ʣ���Ŀ�Ѷ��еȣ�


 53������ϵ�д�
53������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C2H4��C3H4 | B�� | C2H6��C4H10 | C�� | CH2O2��C2H4O2 | D�� | C2H2��C6H6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| 0.01mol•L-1KIO3������Һ�������ۣ������/mL | 0.01mol•L-1 Na2SO3��Һ�����/mL | H2O���� ��/mL | ʵ���� ��/�� | ��Һ������ɫʱ����ʱ��/s | |
| ʵ��1 | 5 | V1 | 35 | 25 | t 1 |
| ʵ��2 | 5 | 5 | 40 | 25 | t 2 |
| ʵ��3 | 5 | 5 | V2 | 0 | t 3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �¶ȼ� | B�� | ������ | C�� | ������ | D�� | �ƾ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ͭ | B�� | Ӳ�� | C�� | ����� | D�� | ���ʯ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
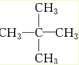 ������Ϊ2��2-�������飨�����飩��
������Ϊ2��2-�������飨�����飩��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com