
取一定量的NaOH溶液通入CO2后,再继续向该溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,下列有关说法正确的是( )
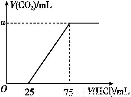
A.原溶液中NaOH的物质的量为0.75 mol
B.通入CO2后所得的溶液溶质成分为NaOH和Na2CO3
C.通入CO2后所得的溶液中含有2.5×10-3 mol NaHCO3
D.纵坐标中a的数值为224
C
【解析】由于盐酸逐滴滴入到碳酸盐中的反应为:Na2CO3+HCl NaHCO3+NaCl;NaHCO3+HCl
NaHCO3+NaCl;NaHCO3+HCl NaCl+CO2↑+H2O,从图像中分析可以发现0~25 mL段消耗的酸体积小于生成气体的体积段消耗酸的体积,所以可以得到溶质的成分是NaHCO3和Na2CO3的混合物,且根据0~25 mL段消耗酸的体积可以判断出Na2CO3的物质的量为2.5×10-3 mol,由25~75 mL段知消耗酸25 mL时,NaHCO3总共(75-25)×10-4 mol=5×10-3 mol,其中由Na2CO3转化过来的NaHCO3是:2.5×10-3 mol,则通入CO2后所得溶液中NaHCO3为:5×10-3 mol-2.5×10-3 mol=2.5×10-3 mol,C正确;其中纵坐标a的数值为112。
NaCl+CO2↑+H2O,从图像中分析可以发现0~25 mL段消耗的酸体积小于生成气体的体积段消耗酸的体积,所以可以得到溶质的成分是NaHCO3和Na2CO3的混合物,且根据0~25 mL段消耗酸的体积可以判断出Na2CO3的物质的量为2.5×10-3 mol,由25~75 mL段知消耗酸25 mL时,NaHCO3总共(75-25)×10-4 mol=5×10-3 mol,其中由Na2CO3转化过来的NaHCO3是:2.5×10-3 mol,则通入CO2后所得溶液中NaHCO3为:5×10-3 mol-2.5×10-3 mol=2.5×10-3 mol,C正确;其中纵坐标a的数值为112。


科目:高中化学 来源:2014高考化学名师知识点精编 专题1物质的分类分散系练习卷(解析版) 题型:选择题
在物质分类中,前者包括后者的是( )
A.氧化物、化合物 B.溶液、分散系 C.溶液、胶体 D.化合物、电解质
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题17氮及其化合物练习卷(解析版) 题型:选择题
往100 mL,pH=0的硫酸和硝酸的混合液中投入3.84 g铜粉,充分反应后,生成NO气体,标准状况下为448 mL,则反应前的混合液中HNO3的物质的量是( )
A.0.02 mol B.0.08 mol
C.0.10 mol D.0.16 mol
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题15富集在海水的元素-氯溴碘练习卷(解析版) 题型:选择题
从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是( )
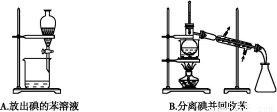
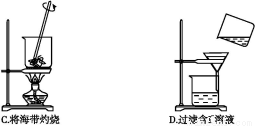
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题14无机非金属材料-碳和硅练习卷(解析版) 题型:选择题
下列根据实验操作和现象所得出的结论正确的是( )
选项实验操作实验现象结 论
A将少量Fe(NO3)2试样加水溶解,滴加稀H2SO4酸化,再滴加KSCN溶液溶液变成红色Fe(NO3)2试样已变质
B将少量某无色气体通入澄清石灰水出现白色沉淀该气体一定是CO2
C分别测定常温下0.1 mol·L-1 Na2SiO3溶液和Na2CO3溶液的pHpH:
Na2SiO3
>Na2CO3非金属性:
Si>C
D向浓度均为0.1 mol·L-1 NaCl和NaI混合溶液中,滴加少量AgNO3溶液出现黄色沉淀Ksp(AgCl)
>Ksp(AgI)
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题13铁、铜及其重要化合物练习卷(解析版) 题型:填空题
硫铁矿烧渣是一种重要的化工生产中间产物,主要成分是Fe3O4、Fe2O3、FeO和二氧化硅等。下面是以硫铁矿烧渣制备高效净水剂聚合硫酸铁的流程图:
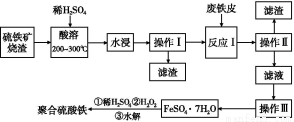
(1)实验室实现“操作Ⅰ”所用的玻璃仪器有 、玻璃棒和烧杯。“操作Ⅲ”系列操作名称依次为 、 、过滤和洗涤。
(2)“酸溶”过程中Fe3O4溶解的化学反应方程式为 。
(3)硫铁矿烧渣在“酸溶”前要粉碎的主要目的是 。
(4)实验室检验“反应Ⅰ”已经完全的试剂是 ,现象是 。
(5)加入适量H2O2的目的是氧化Fe2+,写出H2O2氧化Fe2+为Fe3+的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题13铁、铜及其重要化合物练习卷(解析版) 题型:选择题
FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是( )
A.加入KSCN溶液一定不变红色
B.溶液中一定含Fe2+
C.溶液中一定含Cu2+
D.剩余固体中一定含Cu
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题11电化学练习卷(解析版) 题型:选择题
用如图装置,完成很多电化学实验。下列有关此装置的叙述中,不正确的
是( )
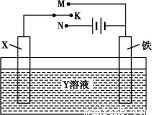
A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阳离子向铁电极移动
C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题9电化学原理练习卷A(解析版) 题型:选择题
肼(N2H4)—空气燃料电池是一种环保型碱性燃料电池,电解质为20%~30%的KOH溶液,电池总反应为N2H4+O2=N2+2H2O。下列关于该电池工作时说法中正确的是( )
A.正极的电极反应式:O2+4H++4e-=2H2O
B.溶液中的阴离子向正极移动
C.负极的电极反应式:N2H4+4OH--4e-=4H2O+N2
D.溶液的pH保持不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com