
【题目】某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了O元素的非金属性比S强的实验研究。
回答下列问题:
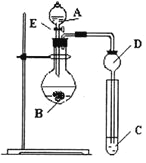
(1)图中D装置名称是 。
(2)从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO3溶液②稀盐酸③碳酸钙④Na2SiO3溶液⑤SiO2
试剂A为_________;试剂C为_________(填序号)。
(3)乙同学设计的实验所用到试剂A为________;试剂C为________。
【答案】(1)长颈漏斗(2)①;④(3)双氧水;氢硫酸或硫化钠溶液。
【解析】试题分析:(1)由装置图可知,装置图中D的名称长颈漏斗,故答案为:长颈漏斗;
(2)通过比较酸性强弱来判断非金属性强弱,装置中为强酸制备弱酸,所以A中试剂为稀硝酸,B中为碳酸钙,C中为Na2SiO3溶液,试管C中为二氧化碳与硅酸钠溶液的反应,其离子方程式为:SiO32-+CO2+H2O═H2SiO3↓+CO32-;故答案为:①;④;
(3)完成了O元素的非金属性比S强的实验研究,通过比较单质的氧化性来判断非金属性,所以用二氧化锰作催化剂使双氧水分解生成氧气,氧气通过氢硫酸或硫化钠溶液会生成硫单质,其反应的方程式为:2H2S+O2=2S↓+2H2O;故答案为:双氧水;氢硫酸。


科目:高中化学 来源: 题型:
【题目】下表中物质的分类组合完全正确的是
编 号 | A | B | C | D |
强电解质 | KNO3 | H2SO4 | Ba(OH)2 | BaSO4 |
弱电解质 | CH3COOH | CaCO3 | H2S | NH3·H2O |
非电解质 | SO2 | CO2 | Cl2 | C2H5OH溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质溶液的正确判断的是
A.在pH=12的溶液中,Al3+、Cl-、HCO3-、Na+可以大量共存
B.在pH=0的溶液中,Na+、NO3-、SO32-、K+可以大量共存
C.由0.1 mol/L —元碱BOH溶液的pH=10,可推知BOH溶液存在BOH![]() B++OH-
B++OH-
D.pH =2的一元酸和pH =12的一元强碱等体积混后溶液一定存在:c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池电解饱和食盐水的装置如图所示 (a、b为石墨电极)。下列说法中,正确的是
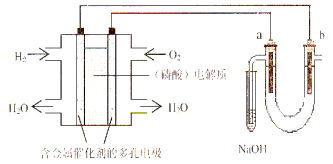
A.电池工作时,正极反应式为:O2 +2 H2O + 4e-= 4OH-
B.电解时,a 电极周围首先放电的是Cl—
C.电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
D.忽略能量损耗,当电池中消耗0.2g H2 时,b极周围会产生2.24L H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表列出了部分元素在周期表中的位置,请用具体的元素完成下列填空。
族 周期 | ⅠA | 0 | ||||||||||||
1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||||||||
2 | X | Y | G | |||||||||||
3 | Z | …… | H | W | E | Q | ||||||||
(1)上述元素的原子中,得电子能力最强的是______________(填元素名称)。
2)化学性质最不活泼的是___________(填元素符号)。
(3)G对应离子的半径______________Z对应离子的半径(填“<”或“>”)。
(4)写出H与Z的最高价氧化物的水化物溶液反应的离子方程式:________________。
(5)元素X的最高价氧化物的电子式________________,元素W的最高价氧化物为
_______________(填晶体类型)。
(6)为比较元素X和W的非金属性强弱,用下图所示装置进行实验(夹持仪器已略去,装置气密性良好)。溶液B的作用是________________,能说明X和W非金属性强弱的化学方程式是_________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示溶液中c(H+)和c(OH-)的关系,下列判断错误的是:
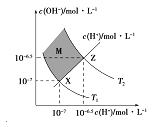
A. 两条曲线间任意点均有c(H+)×c(OH-)=KW
B. M区域内任意点均有c(H+)<c(OH-)
C. 图中T1<T2
D. XZ线上任意点均有pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【江西省师大附中、临川一中2017届高三1月联考理综】等体积浓度均为0.1mol/L的三种溶液:①CH3COOH溶液、②HSCN溶液、③NaHCO3溶液混合,①、②分别与③混合,实验测得产生的CO2气体体积(V)随时间(t)的变化如图所示,下列说法正确的是( )
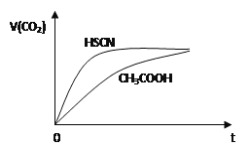
A. 三种溶液pH的比较③>②>①
B. 反应结束后所得两溶液中,c(CH3COO-)>c(SCN-)
C. 上述三种溶液中水电离的电离度:NaHCO3>CH3COOH>HSCN
D. ①与③反应所得的溶液中:c(CH3COO-) + c(CH3COOH) = 0.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液氨和水类似,也能电离:NH3+NH3![]() NH4++NH2﹣,25℃时,其离子积K=1.0×10﹣30mol2L﹣2.现将2.3g金属钠投入1.0L液氨中,钠完全反应,有NaNH2和H2产生,则所得溶液中粒子关系不正确的是(设温度保持不变,溶液体积为1L)
NH4++NH2﹣,25℃时,其离子积K=1.0×10﹣30mol2L﹣2.现将2.3g金属钠投入1.0L液氨中,钠完全反应,有NaNH2和H2产生,则所得溶液中粒子关系不正确的是(设温度保持不变,溶液体积为1L)
A.c(Na+)=c(NH2﹣) B.c(NH4+)=1.0×10﹣29molL﹣1
C.c(NH2﹣)>c(NH4+) D.c(NH4+) c(NH2﹣)=1.0×10﹣30 mol2L﹣2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com