
【题目】国庆70周年阅兵式,大量新式武器新鲜出炉且都为中国制造,制造这些“国之重器”的材料多为合金。下列关于合金的说法不正确的是
A.合金在工业上的用途比纯金属更广
B.合金的硬度一般比它的成分金属大
C.合金的熔点一般比它的成分金属高
D.合金与各成分金属相比,具有许多优良的物理、化学或机械性能
科目:高中化学 来源: 题型:
【题目】生活中常常碰到涉及化学知识的某些问题,下列叙述正确的是( ) ①人的皮肤在强紫外线的照射下将会失去生理活性
②用甲醛溶液浸泡海产品保鲜
③变质的油脂有难闻的特殊气味,是由于油脂发生了水解反应
④厨房用到的食盐、醋和糖均可以防腐.
A.①④
B.②③
C.①②④
D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对滴有酚酞试液的下列溶液,操作后颜色变深的是( )
A.明矾溶液加热
B.CH3COONa溶液加热
C.氨水中加入少量NH4Cl固体
D.小苏打溶液中加入少量NaCl固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种常见物质的转化关系如图所示(部分反应物及产物略去),其中Q、M、N含有某种相同的元素。下列说法不正确的是
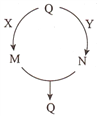
A. 若Q为N2,则X可能为氢气 B. 若Q为A1(OH)3,则Y可能为稀硫酸
C. 若Q为Fe,则Y可能为稀硝酸 D. 若Q为NaHCO3,则X可能为氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中有一瓶含有一定量杂质的烧碱样品,某学生用中和滴定法测定烧碱的纯度,若烧碱中含有与酸不反应的杂质,请根据实验回答:
(1)将准确称取的4.3g烧碱样品配成250mL待测液,需要的主要仪器除量筒、烧杯、玻璃棒、托盘天平外,还必须用到的仪器有:、 .
(2)取10.00mL待测液,选择下图中(填A或B)来移取.![]()
(3)用0.2000标准盐酸滴定待测烧碱溶液,以酚酞为指示剂.滴定时左手旋转滴定管玻璃活塞,右手不停地摇动锥形瓶,两眼注视 , 直到滴定终点.滴定达到终点的标志是: .
(4)根据下列数据,烧碱的纯度为:(精确到小数点后一位)
滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 10.00 | 0.50 | 20.40 |
第二次 | 10.00 | 4.00 | 24.10 |
(5)判断下列操作引起的误差(填“偏大”、“偏小”或“无影响”)①滴定前读数正确,滴定终点读数时仰视. .
②未用标准液润洗滴定管. .
③滴定终点时发现滴定管尖嘴处悬挂着一滴溶液. .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】出土的古代铜制品上往往覆盖着一层铜绿〔主要成分是Cu2(OH)2CO3〕,下列关于铜及其化合物的说法不正确的是
A.铜盐溶液有毒
B.Cu2(OH)2CO3中铜的化合价为+1
C.硫酸铜常用来配制农药,如波尔多液
D.铜属于重金属,它的化学性质不活泼,所以使用铜器皿比较安全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素的原子结构决定其性质和在周期表中的位置.下列叙述正确的是( )
A.多电子原子中,在离核较近的区域内运动的电子能量较高
B.原子核外电子的数目越多,电子的运动状态就越多
C.轨道表示式,是对原子核外电子运动状态最完美的描述
D.所有元素原子的最外层电子数都等于该元素的最高化合价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6LH2;E的阳离子与A的阴离子核外电子层结构完全相同. 
回答下列问题:
(1)B的元素名称为 , D在周期表中的位置 .
(2)A,C,D对应的离子半径由大到小顺序为 , (用化学符号表示)
(3)D的单质与水反应的离子方程式为 .
(4)向D与E形成的化合物的水溶液中滴入过量烧碱溶液,用离子方程式表述 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数.下列说法中,正确的是( )
A.1.8g重水(D2O)中含有的质子数为1.0 NA
B.500℃、30MPa下:N2(g)+3H2(g)2NH3(g);△H=﹣38.6kJmol﹣1;将1.5NA的H2和过量N2在此条件下充分反应,放出热量19.3kJ
C.标准状况下,11.2 L Cl2通入足量的石灰乳中制备漂白粉,转移的电子数为0.5NA
D.60 g石英晶体中含有的Si﹣O键数目为2NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com