
下列说法正确的是
A.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强
B.KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质
C.根据是否有丁达尔效应将分散系分为溶液、胶体和浊液
D.使用静电除尘器除去空气中的飘尘利用了胶体的性质
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:
设计实验证明酸性强弱顺序:HCl>H2CO3>H2SiO3。
(1)写出实验原理的化学反应方程式________________。
(2)设计本实验所依据的化学原理是________________。
(3)实验中必须用到的药品有________________,所需的实验仪器有________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为
A.两种分子的中心原子杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。
B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。
C.氨气分子是极性分子而甲烷是非极性分子。
D.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。
查看答案和解析>>
科目:高中化学 来源: 题型:
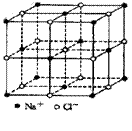
食盐晶体如图所示。在晶体中,· 表示Na+,o 表示Cl-。已知食盐的密度为r g / cm3,NaCl摩尔质量M g / mol,阿伏加德罗常数为N,则在食盐晶体里Na+和Cl-的间距大约是
 |
A. 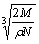 cm B.
cm B. 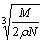 cm
cm
C. 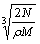 cm D.
cm D. 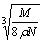 cm
cm
查看答案和解析>>
科目:高中化学 来源: 题型:
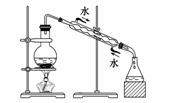
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是
 |
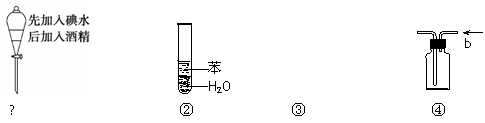 |
A.溶液上层无色,下层紫红色
B.装置②可用于吸收HCl气体,并防止倒吸
 C.装置③可用于制取蒸馏水
C.装置③可用于制取蒸馏水
D.装置④ b口进气可收集H2、CO2等气体
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列化学方程式中,能够用离子方程式H+ + OH-= H2O表示的是
A.醋酸溶液与氢氧化钠溶液反应
B.盐酸与氨水反应
C.硫酸氢钠溶液与氢氧化钾溶液反应
D.氢氧化铁与硫酸溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.食盐是日常生活的必需品,也是重要的化工原料。粗食盐常含有少量Ca2+、Mg2+、SO42-等杂质离子,实验室提纯NaCl的流程如下:
 |
提供的试剂:
饱和Na2CO3溶液、 饱和K2CO3溶液 、NaOH溶液 、BaCl2溶液、Ba(NO3)2溶液
(1)欲除去溶液I中的Ca2+、Mg2+、SO42-离子,选出A所代表的试剂,按滴加顺序依次为 _______________________________________(只填化学式)。
(2)操作Ⅲ的名称是_________,所需用到的仪器主要有铁架台、酒精灯、铁圈、______________________ (填仪器名称)。
(3)加盐酸的目的是(用离子方程式表示) 、 。
Ⅱ.一份无色溶液中可能含有Na+ 、Fe3+、H+ 、Mg2+、CO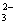 、OH-、HCO
、OH-、HCO 、Cl-、SO42-等离子中的若干种。为了确定溶液的组成,进行了如下操作:
、Cl-、SO42-等离子中的若干种。为了确定溶液的组成,进行了如下操作:
① 向溶液中滴加酚酞试液,溶液显红色;
② 取2 mL溶液,先加足量稀硝酸酸化,有气体产生,再加氯化钡溶液进行检验,没有明显现象;
(4)原溶液中一定存在的离子是 , 一定不存在的离子是 。
(5)经过上述操作后,还不能肯定是否存在的离子是 。对可能含有的离子,如何进行实验以进一步检验。 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法中,不正确的是:
A.a mol/L的HCN溶液与b mol/L的NaOH溶液等体积混合,所得溶液中
c(Na+)>c(CN-),则a一定小于b
B.常温下,CH3COONa溶液的pH=8,则c(Na+) -c(CH3COO-)=9.9×10-7mol/L
C.常温下,0.1mol/L的某酸溶液中,若c(OH-)/c(H+) =1×10-8,则溶液中由水电离出的
c(H+) =1×10-11mol/L
D.在0.1 mol/L Na2SO3溶液中加入少量NaOH固体,c(SO32-)与c(Na+)均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
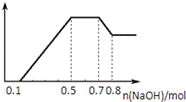
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种。①若加入锌粒,产生
无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如右图所示。则下列说法正确的是( )
A.溶液中一定不含CO32-,可能含有SO42-和NO3-
B.溶液中的阳离子只有H+、Mg2+、Al3+
C.溶液中n(NH4+)=0.2mol
D.n(H+)∶n(Al3+)∶n(Mg2+) = 1∶1∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com