
| ŠņŗÅ | Ba£ØOH£©2ČÜŅŗĢå»ż/mL | ŃĪĖįĢå»ż/mL | »ģŗĻŅŗpH |
| 1 | 22.00 | 0 | 10 |
| 2 | 22.00 | 22.00 | 8 |
| 3 | 22.00 | 18.00 | n |
| A£® | 4”¢9 | B£® | 4”¢7 | C£® | 6”¢9 | D£® | 6”¢7 |
·ÖĪö ŌŚt”ꏱ£¬Ä³Ba£ØOH£©2µÄĻ”ČÜŅŗÖŠc£ØH+£©=10-x mol/L£¬c£ØOH-£©=10-y mol/L£¬Ōņkw=c£ØH+£©”Įc£ØOH-£©=10-x”Į10-y=10-£Øx+y£©£¬x+y=16£¬ŌņKw=1”Į10-16£¬ÖŠŠŌČÜŅŗpH=8£¬ĖµĆ÷ĪĀ¶ČµĶÓŚ³£ĪĀĻĀ£»Ć»ÓŠ¼ÓŃĪĖįŹ±ČÜŅŗµÄpH=10£¬æÉŅŌĒó³öĒāŃõ»Æ±µÖŠĒāŃõøłĄė×ÓÅØ¶Č£¬ŌŁøł¾ŻŃĪĖįĪŖ22mLŹ±£¬ČÜŅŗĻŌÖŠŠŌ£¬æÉŅŌĒó³öĻūŗĵÄŃĪĖįµÄÅØ¶Č£»
µ±¼ÓČėµÄHClĪŖ18mLŹ±£¬ĒāŃõøłĄė×Ó¹żĮ棬æÉŅŌ»ģŗĻŗóČÜŅŗÖŠc£ØOH-£©£¬ŌŁĒó³öpH£®
½ā“š ½ā£ŗŌŚt”ꏱ£¬Ä³Ba£ØOH£©2µÄĻ”ČÜŅŗÖŠc£ØH+£©=10-x mol/L£¬c£ØOH-£©=10-y mol/L£¬Ōņkw=c£ØH+£©”Įc£ØOH-£©=10-x”Į10-y=10-£Øx+y£©£¬x+y=16£¬ŌņKw=1”Į10-16£¬ÖŠŠŌČÜŅŗpH=8£»
ƻӊ¼ÓŃĪĖįŹ±ČÜŅŗµÄpH=10£¬Ōņc£ØOH-£©=10-6mol/L£¬
µ±Ē”ŗĆĶźČ«ÖŠŗĶŹ±£¬ČÜŅŗµÄpH=8£¬¼“¼ÓŃĪĖįµÄĢå»żĪŖ22.00 mLŹ±£¬Ē”ŗĆĶźČ«ÖŠŗĶ£¬
øł¾Żc£ØH+£©”Į22.00 mL=c£ØOH-£©”Į22.00 mL£¬ÓÖŅņĪŖc£ØOH-£©=10-6mol/L£¬
ŌņŃĪĖįc£ØH+£©=10-6mol/L£¬pH=6£¬¼“m=6£»
µ±¼ÓČėµÄHClĪŖ18mLŹ±£¬»ģŗĻŗóČÜŅŗÖŠc£ØOH-£©=$\frac{22.00mL”Į1{0}^{-6}mol/L-18mL”Į1{0}^{-6}mol/L}{40mL}$=10-7mol/L£¬ĖłŅŌc£ØH+£©=10-9mol/L£¬pH=9£¬¼“n=9£®
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĖį¼ī»ģŗĻµÄ¶ØŠŌÅŠ¶ĻŗĶ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬ÅŠ¶ĻøĆĪĀ¶ČĻĀµÄKwĪŖ½ā“šøĆĢāµÄ¹Ų¼ü£¬×¢Ņāµ±pH=8Ź±£¬Ėį¼īĒ”ŗĆÖŠŗĶ£¬²ąÖŲÓŚæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ¼ĘĖćÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
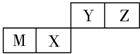
| A£® | Ō×Ó°ė¾¶Z£¼M | |
| B£® | YµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌ±ČXµÄČõ | |
| C£® | XµÄ×ī¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄČČĪČ¶ØŠŌ±ČZµÄČõ | |
| D£® | ZĪ»ÓŚŌŖĖŲÖÜĘŚ±ķÖŠµŚ2ÖÜĘŚ”¢µŚ¢öA×å |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | XŗĶY¶¼ŹĒŠŌÖŹ»īĘƵÄŌŖĖŲ£¬ŌŚ×ŌČ»½ēÖŠÖ»ÄÜŅŌ»ÆŗĻĢ¬“ęŌŚ | |
| B£® | XŗĶYŠĪ³ÉµÄ»ÆŗĻĪļµÄ»ÆѧŹ½Ö»ÄÜĪŖY2X2 | |
| C£® | XµÄ»ÆŗĻĪļÖÖĄą±ČYµÄ»ÆŗĻĪļÖÖĄą¶ą | |
| D£® | YÄÜÖĆ»»ĖįÖŠĒā·Å³öĒāĘų£¬µ«²»ÄÜÖĆ»»ŃĪÖŠµÄ½šŹō |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆ HNO2ČÜŅŗ×÷µ¼µēŠŌŹµŃ飬µĘ¹ā½Ļ°µ£¬ĖµĆ÷ HNO2ŹĒČõµē½āÖŹ | |
| B£® | NaCl ČÜŅŗŗĶ CH3COONH4ČÜŅŗ¾łĻŌÖŠŠŌ£¬Į½ČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶ČĻąĶ¬ | |
| C£® | 25”ꏱ£¬ÓĆ“×ĖįČÜŅŗÖŠŗĶµČÅØ¶Č NaOH ČÜŅŗÖĮ pH=7£¬VCH3COOH£¼VNaOH | |
| D£® | AgCl Ņ××Ŗ»ÆĪŖ AgI ³ĮµķĒŅ Ksp£ØAgX£©=[Ag+]•[X-]£¬¹Ź Ksp£ØAgI£©£¼Ksp£ØAgCl£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŗ¬“óĮæFe3+µÄČÜŅŗÖŠ£ŗNa+”¢Mg2+”¢SO42-”¢SCN- | |
| B£® | Ź¹¼×»ł³Č³ŹŗģÉ«µÄČÜŅŗ£ŗNO3-”¢Ba2+”¢AlO2-”¢Cl- | |
| C£® | ÓėĀĮ·“Ó¦²śÉś“óĮæĒāĘųµÄČÜŅŗ£ŗNa+”¢K+”¢CO32-”¢NO3- | |
| D£® | pH=12µÄČÜŅŗ£ŗCO32-”¢Cl-”¢K+”¢F- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
 £»
£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
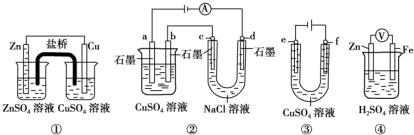
| A£® | ×°ÖĆ¢ŁÖŠ£¬ŃĪĒÅÖŠµÄK+ŅĘĻņCuSO4ČÜŅŗ | |
| B£® | ×°ÖĆ¢ŚÖŠb¼«Īö³ö6.4 g¹ĢĢåŹ±£¬d¼«²śÉś2.24 L H2 | |
| C£® | ÓĆ×°ÖĆ¢Ū¾«Į¶ĶŹ±£¬f¼«ĪŖ“ÖĶ | |
| D£® | ×°ÖĆ¢ÜÖŠµē×ÓŃŲµ¼ĻßÓÉZnĮ÷ĻņFe£¬Fe¼«ÉĻÓŠ“óĮæĘųÅŻÉś³É |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µŚČżÖÜĘŚµŚ¢õA×å | B£® | µŚ¶žÖÜĘŚµŚ¢õA×å | C£® | µŚČżÖÜĘŚµŚ¢ōA×å | D£® | µŚČżÖÜĘŚµŚ¢õA×å |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com