
下列说法中,正确的是( )
A.铁是人类在生产、生活中最早使用的金属
B.金、银、铜是应用最广泛的金属材料
C.钛被誉为“21世纪的金属”,应用前景很广阔
D.铜是导电性、导热性最好的有色金属
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列化学用语的表述正确的是( )
A.离子结构示意图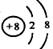 :可以表示16O2-,也可以表示18O2-
:可以表示16O2-,也可以表示18O2-
B.比例模型  :可以表示甲烷分子,也可以表示四氯化碳分子
:可以表示甲烷分子,也可以表示四氯化碳分子
C.氯化铵的电子式为: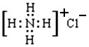
D.CO2的结构式为: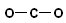
查看答案和解析>>
科目:高中化学 来源: 题型:
主链为5个碳原子的C7H16的同分异构体中,其中一种同分异构体A的核磁共振氢谱有3个峰且面积比为1︰1︰6,则A的一氯代物的同分异构体的数目为( )
A.2 B.3  C.4
C.4  D.5
D.5
查看答案和解析>>
科目:高中化学 来源: 题型:
向一定量的下列物质中逐滴加入氢氧化钠溶液,先生成白色沉淀,后沉淀逐渐溶解。这种物质是( )
A.MgSO4 B.Na[Al(OH)4]
C.AlCl3 D.FeCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
查阅有关资料知:金属铝与氢氧化钠溶液反应实际是分以下两步进行:
第一步:2Al+6H2O===2Al(OH)3+3H2↑
第二步:Al(OH)3+NaOH===Na[Al(OH)4]
试回答下列问题:
(1)书写金属铝与氢氧化钠溶液反应的离子方程式:____________________________。
(2)判断两步反应的反应类型:第一步属________,第二步属________(用四种基本反应类型答题)。
(3)请分析,金属铝与氢氧化钠溶液的反应中氧化剂是________,还原剂是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学研究性学习小组为了解Cu的常见化合物性质,运用类比的思想提出如下问题,并进行探究。
提出问题 ①通常情况下,+2价Fe不如+3价Fe稳定,+1价Cu也不如+2价Cu稳定吗?
②CuO能被H2、CO等还原,也能被NH3还原吗?
实验方案 (1)解决问题①的实验步骤和现象如下:取98 g Cu(OH)2固体,加热至80 ℃~100 ℃时,得到黑色固体粉末,继续加热到1 000 ℃以上,黑色粉末全部变成红色粉末A。冷却后称量,A的质量为72 g。向A中加入适量的稀硫酸,得到蓝色溶液,同时观察到容器内还有红色固体存在。据此可推得A的化学式为____________。
(2)如图所示为常见气体的制备、干燥和性质验证的部分仪器装置(部分夹持装置及尾气处理装置未画出),请从中选择合适的药品和仪器装置回答问题。
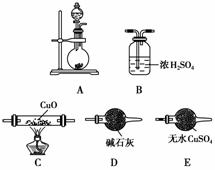
①制取干燥的NH3并还原CuO,所选仪器装置的正确连接顺序是________。
②制取NH3可选用下列药品中的________。
A.NH4Cl和Ca(OH)2 B.NH4HCO3
C.浓氨水和生石灰 D.浓氨水和固体烧碱
③若CuO能被NH3还原,实验中观察到的现象是________________________,该反应的化学方程式为__________________________。
实验结论 根据“实验方案(1)”,得出的+1价Cu和+2价Cu稳定性大小的结论是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
采用右图装置(实验前已除尽装置内的空气)制取Na2S2O 5。装置II中有Na2S2O5晶体析出,发生的反应为:Na2SO3+SO2=Na2S2O5
5。装置II中有Na2S2O5晶体析出,发生的反应为:Na2SO3+SO2=Na2S2O5
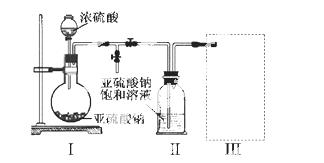
(1)装置I中产生气体的化学方程式为 。
(2)要从装置II中获得已析出的晶体,可采取的分离方法是 。
(3)装置III用于处理尾气,可选用的最合理装置(夹持仪器已略去)为 (填序号)。
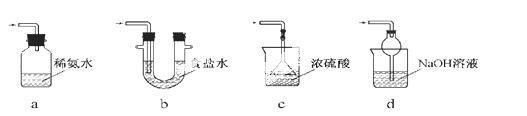
实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)证明NaHSO3溶液中HSO3- 的电离程度大于水解程度,可采用的实验方法是 (填序号)。
a.测定溶液的pH b.加入Ba(OH)2溶液 c.加入盐酸
d.加入品红溶液 e.用蓝色石蕊试纸检测
(5)检验Na2S2O5晶体在空气中已被氧化的实验方案是 。
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为 g·L-1。
②在上述实验过程中,若有部分HI被空气氧化,则测得结果 (填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在10 L密闭容器中,1 mol A和3 mol B在一定条件下反应:A(g)+xB(g)  2C(g),
2C(g),
2 min后达到平衡,生成0.4 mol C,测得混合气体共3.4 mol,则下列结果正确的是
A.平衡时,物质的量之比n(A)∶n(B)∶n(C)=2∶11∶4
B.x值等于3
C.A的转化率为20%
D.B的平均反应速率为0.4 mol/(L·min)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com