
【题目】Ⅰ:二氧化碳的回收利用是环保领域研究的热点课题。
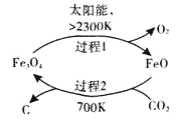
(1)以CO2为原料制取炭黑的流程如图所其总反应的化学方程式为________,
(2)CO2经过催化氢化合成低碳烯烃。其合成乙烯的反应为2CO2(g)+6H2(g)![]() CH2=CH2(g)+4H2O(g) ΔH几种物质的能量(在标准状况下,规定单质的能量为 0,测得其他物质在生成时所放出或吸收的热量)如下表所示:
CH2=CH2(g)+4H2O(g) ΔH几种物质的能量(在标准状况下,规定单质的能量为 0,测得其他物质在生成时所放出或吸收的热量)如下表所示:
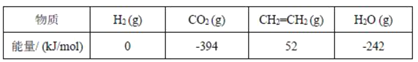
则ΔH=____。
Ⅱ:已知:①2C(s)+O2(g)=2CO(g) ΔH=-220kJ·mol-1;②氢气燃烧的能量变化示意图:
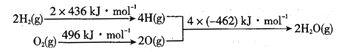
请写出碳和水蒸气反应,生成 CO和H2的热化学方程式:_______
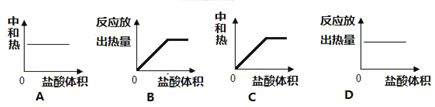
Ⅲ:向100mL0.1mol·L-1 稀 NaOH溶液中加入稀盐酸,“中和热”或“反应放出热量”与所加入的盐酸体积的关系图正确的是(________)
【答案】CO2![]() C+O2 -128kJ/mol C(s)+H2O(g)=CO(g)+H2(g) △H=+130kJ/mol AB
C+O2 -128kJ/mol C(s)+H2O(g)=CO(g)+H2(g) △H=+130kJ/mol AB
【解析】
I.(1)在700K条件下,CO2和FeO发生反应生成C和Fe3O4,过程1中Fe3O4分解生成FeO和O2,所以整个反应过程中FeO作催化剂,根据反应物和生成物及反应条件书写方程式;
(2)焓变等于生成物总能量减去反应物总能量;
II.根据盖斯定律,睛已知的热化学方程式叠加,可得待求反应的热化学方程式;
III.中和热是强酸强碱发生中和反应产生1mol水时放出的热量;反应放出的热量与反应的物质的多少有关。
(1)在700K条件下,CO2和FeO发生反应生成C和Fe3O4,过程1中Fe3O4分解生成FeO和O2,所以整个反应过程中FeO作催化剂,根据反应物和生成物及反应条件书写方程式为CO2![]() C+O2;
C+O2;
(2)焓变等于生成物总能量减去反应物总能量,则该反应的焓变=[52+(-242)×4-(-392)×2-0]kJ/mol=-128kJ/mol;
II.①2C(s)+O2(g)=2CO(g) ΔH=-220kJ·mol-1;②根据图示可得H2(g)+![]() O2(g)=H2O(g) ΔH=436kJmol+
O2(g)=H2O(g) ΔH=436kJmol+![]() kJ/mol -2(-462)kJ/mol=-240kJ/mol;根据盖斯定律将
kJ/mol -2(-462)kJ/mol=-240kJ/mol;根据盖斯定律将![]() ①-②,整理可得C(s)+H2O(g)=CO(g)+H2(g) △H=+130kJ/mol;
①-②,整理可得C(s)+H2O(g)=CO(g)+H2(g) △H=+130kJ/mol;
III.中和热是强酸强碱发生中和反应产生1mol水时放出的热量,由于水的物质的量是1mol,所以中和热不会发生变化,是一个定值,选项A正确,C错误;
在容器中含有的NaOH的物质的一定,随着HCl的加入,反应产生的H2O的物质的量逐渐增多,反应放出的热量也逐渐增多,当NaOH恰好反应完全时,放出的热量达到最大值,此后再加入盐酸,不能在反应,反应放出的热量也不再发生变化,则选项B正确、D错误;
所以合理选项是AB。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】化学与生产、生活紧密相关,下列有关物质应用的说法不正确的是![]()
![]()
![]() 古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金
古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金
![]() 制造新版人民币所使用的棉花、优质针叶木、羊毛、蚕丝都属于天然纤维
制造新版人民币所使用的棉花、优质针叶木、羊毛、蚕丝都属于天然纤维
![]() 为了增强漂白粉的使用效果,在使用漂白粉时和盐酸混合使用
为了增强漂白粉的使用效果,在使用漂白粉时和盐酸混合使用
![]() 天津港爆炸案中对剧毒的氰化钠
天津港爆炸案中对剧毒的氰化钠![]() 喷洒双氧水消毒,是利用了双氧水的还原性
喷洒双氧水消毒,是利用了双氧水的还原性
![]() 碳酸钙分解、氢氧化钡晶体和氯化铵固体反应、高温下铝与氧化铁反应都是吸热反应
碳酸钙分解、氢氧化钡晶体和氯化铵固体反应、高温下铝与氧化铁反应都是吸热反应
![]() 玛瑙的主要成分是二氧化硅,陶瓷的主要成分是硅酸盐
玛瑙的主要成分是二氧化硅,陶瓷的主要成分是硅酸盐
![]() 豆浆制豆腐、纳米材料、塑料、橡胶及合成纤维等制造过程都会用到胶体的性质
豆浆制豆腐、纳米材料、塑料、橡胶及合成纤维等制造过程都会用到胶体的性质
![]() “青蒿一握,以水二升渍,绞取汁”,该过程对青蒿素的提取属于物理变化
“青蒿一握,以水二升渍,绞取汁”,该过程对青蒿素的提取属于物理变化
A.5个B.4个C.3个D.2个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是
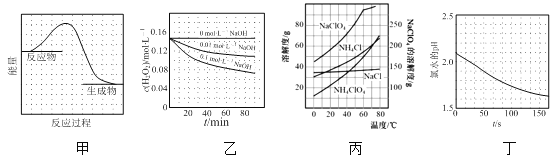
A.图甲表示某反应过程中的能量变化曲线,可推知该反应是吸热反应
B.图乙表示70℃时不同碱性条件下H2O2的浓度随时间变化的曲线,可推知溶液碱性越强,H2O2分解速率越慢
C.图丙表示部分物质的溶解度随温度变化的曲线,可推知20℃时向含a mol NaClO4的饱和溶液中加入a mol NH4Cl固体会有NH4ClO4固体析出
D.图丁表示光照下氯水的pH随时间的变化曲线,可推知光照后溶液中Cl2浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图甲、乙分别表示反应 CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH>0 在 t1 时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况,下列说法正确的是
CO(g)+H2O(g) ΔH>0 在 t1 时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况,下列说法正确的是
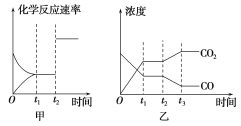
A.图甲中t2时刻发生改变的条件一定是同比增大 CO2和H2的浓度
B.图甲中t2时刻发生改变的条件一定是加入催化剂
C.图乙中t2时刻发生改变的条件可能是降低温度
D.图乙中t2时刻发生改变的条件可能是增大CO2的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃,c(HCN)+c(CN-)=0.1 mol·L-1的一组HCN和NaCN的混合溶液,溶液中 c(HCN)、c(CN-)与pH的关系如图所示。下列有关离子浓度关系叙述正确的是( )
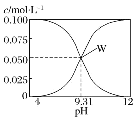
A.将 0.1 mol·L-1 的 HCN 溶液和 0.1 mol·L-1NaCN溶液等体积混合(忽略溶液体积变化):c(Na+)>c(HCN)>c(CN-)>c(OH-)>c(H+)
B.W 点表示溶液中:c(Na+)=c(HCN)+c(CN-)
C.pH=8的溶液中:c(Na+)+c(H+)+c(HCN)=0.1 mol·L-1+c(OH-)
D.将0.3 mol·L-1 HCN溶液和0.2 mol·L-1NaOH溶液等体积混合(忽略溶液体积变化):c(CN-)+3c(OH-)=c(HCN)+3c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一个2L的密闭容器中,加入4molX和2molY进行如下反应:3X(g)+2Y(g)![]() 4Z(s)+2W(g),反应一段时间后达到平衡,测得生成1.6molZ,则下列说法正确的是( )
4Z(s)+2W(g),反应一段时间后达到平衡,测得生成1.6molZ,则下列说法正确的是( )
A.该反应的化学平衡常数表达式是K=![]()
B.此时,Y的平衡转化率是40%
C.增大该体系的压强,化学平衡常数增大
D.增加Y,Y的平衡转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空。
(1)按系统命名法给下列有机物命名:
①(CH3)2CHCH(Cl)CH3:___。
②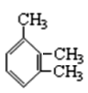 :___。
:___。
(2)羟基的电子式是:___。
(3)2-甲基-1-丁烯的键线式:___。
(4)相对分子质量最小的有机物空间构型是___。
(5)3-甲基戊烷的一氯代产物有___种(考虑立体异构)。
(6)高分子化合物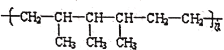 的单体分别是___。
的单体分别是___。
(7)写出下列有机反应的方程式:
①2-溴丙烷的水解反应:___。
②3-甲基-2-丁醇的催化氧化反应:___。
③实验室制乙烯:___。
④对苯二甲酸和乙二醇的缩聚反应:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
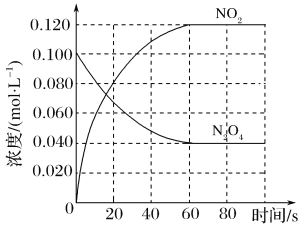
该反应ΔH______0(填“>”、“<”或“=”),在0~60 s时段,反应速率v(N2O4)为________mol·L-1·s-1。平衡常数K=________________(请书写单位)。在温度不变的情况下向平衡体系中再充入N2O4 0.01mol·L-1和NO20.03mol·L-1此时v(正)___________v(逆)(填“>”、“<”或“=”)。有利于提高反应N2O4(g) ![]() 2NO2(g)平衡转化率的条件是________(填标号)。
2NO2(g)平衡转化率的条件是________(填标号)。
A.高温低压 B.低温高压
C.高温高压 D.低温低压
(2)在一定温度下,向a L密闭容器中加入1 molN2O4(g)发生如下反应:N2O4(g) ![]() 2NO2(g),不能说明该反应一定达平衡的是__________。
2NO2(g),不能说明该反应一定达平衡的是__________。
A.容器内压强不随时间变化
B.容器内各物质的浓度不随时间变化
C.容器内O2、NO、NO2的浓度之比为1:2:2
D.单位时间内生成1 mol N2O4(g),同时生成2 mol NO2
E.混合气体的密度不随时间变化
F.混合气体的颜色不随时间变化
(3)在体积都为1 L,pH都等于2的盐酸和醋酸溶液中,投入0.65 g锌粒,则如图所示符合客观事实的是__________
A. 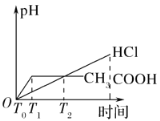 B.
B. 
C. 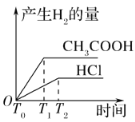 D.
D. 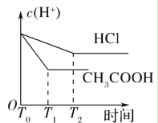
(4)25 ℃时,一元弱酸HA溶液Kal=4.3×10-4 ,一元弱酸HB溶液Ka2=5.6×10-4则酸性HA____________HB(填“>”、“<”或“=”)。
(5)常温下0.001mol·L-1的H2SO4溶液与0.004mol·L-1的NaOH溶液1:1体积比混合,混合后溶液的pH=_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列各化合物:
A.CH3CH2CH2CHO与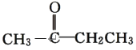
B.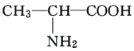 与
与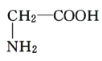
C. ![]() 与
与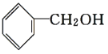
D.CH3CH≡CH与CH2=CH—CH=CH2
E. 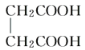 与
与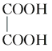
F.戊烯与环戊烷
(1)上述各组化合物中属于同系物的是________,属于同分异构体的是________(填字母)。
(2)上述A中两化合物的含氧官能团是__________和 __________(写名称)。
(3)根据官能团的特点可将C中两种化合物划分为________类和________类。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com