
”¾ĢāÄæ”æĻĀĮŠŹōÓŚµē½āÖŹµÄŹĒ
A. ÕįĢĒ B. ŃĪĖį C. ¾Ę¾« D. ĒāŃõ»ÆÄĘ

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼×“¼ŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬Ņ²ŹĒŅ»ÖÖÓÅÖŹµÄČ¼ĮĻ”£
¢ń.¼×“¼ĶŃĒāÖĘČ”¼×Č©µÄŌĄķĪŖCH3OH(g)![]() HCHO(g) +H2(g)”£Ä³æĘŃŠŠ”×éŌŚ2 LĆܱÕČŻĘ÷ÖŠ³äČė1 mol CH3OH£¬¶ŌøĆ·“Ó¦½ųŠŠĮĖŅ»ĻµĮŠµÄŃŠ¾æ£¬µĆµ½¼×“¼µÄĘ½ŗā×Ŗ»ÆĀŹĖęĪĀ¶ČµÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾”£
HCHO(g) +H2(g)”£Ä³æĘŃŠŠ”×éŌŚ2 LĆܱÕČŻĘ÷ÖŠ³äČė1 mol CH3OH£¬¶ŌøĆ·“Ó¦½ųŠŠĮĖŅ»ĻµĮŠµÄŃŠ¾æ£¬µĆµ½¼×“¼µÄĘ½ŗā×Ŗ»ÆĀŹĖęĪĀ¶ČµÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾”£
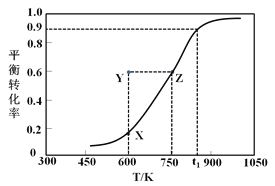
£Ø1£©ĻĀĮŠŃ”ĻīÖŠ£¬ÄÜĖµĆ÷øĆ·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄŹĒ__________£»
a£®v(CH3OH) =v(HCHO) b£®H2µÄĢå»ż·ÖŹż²»ŌŁ±ä»Æ
c£®¼×Č©µÄÖŹĮæ·ÖŹż²»ŌŁøıä d£®»ģŗĻĘųĢåĆÜ¶Č²»±ä
£Ø2£©ŌŚt1Ź±£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżĪŖK=________________£¬“ĖĪĀ¶ČĻĀ£¬“Ó·“Ó¦æŖŹ¼µ½Ę½ŗāĖł¾¹żµÄŹ±¼äĪŖ5 s£¬Ōņv(HCHO)ĪŖ_______mol/(L”¤min)”£Ļņ“ĖČŻĘ÷ÖŠŌŁĶØČė1.1 mol CH3OHŗĶ1.1 mol H2£¬ŌņĘ½ŗāĻņ_________£ØĢī”°Õż·“Ó¦”±»ņ”°Äę·“Ó¦”±£©·½ĻņŅĘ¶Æ£»
£Ø3£©600 KŹ±£¬Yµć¼×“¼µÄv(Õż)_______v(Äę) (Ģī”°>”±”¢”°<”±»ņ”°=”±)£¬ĄķÓÉŹĒ_____________________£»
¢ņ.ŅŃÖŖ£ŗCH3OH(g) +CuO(s)=HCHO(g) +Cu(s)+H2O(g) ¦¤H1=£a kJ/mol£»
2Cu(s)+O2(g)=2CuO(s) ¦¤H2=£b kJ/mol£»
£Ø4£©ŌņŌŚĶ×÷“߻ƼĮŹ±£ŗ2CH3OH(g)+O2(g)=2HCHO(g)+2H2O(g) ¦¤H3=______kJ/mol£ØÓĆŗ¬a£¬bµÄ“śŹżŹ½±ķŹ¾£©£»
¢ó.ČēĶ¼ĖłŹ¾ŹĒŅŌNaOHČÜŅŗĪŖµē½āÖŹČÜŅŗµÄ¼×“¼Č¼ĮĻµē³Ų£ŗ

£Ø5£©a¼«µē¼«·“Ó¦Ź½ĪŖ__________________________£¬ČōøōĤĪŖŅõĄė×Ó½»»»Ä¤£¬Ōņµē³Ų¹¤×÷Ņ»¶Īŗ󣬵ē³Ųøŗ¼«ĒųČÜŅŗÖŠn(OH£)_____£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø11·Ö£©ŌŚ2LĆܱÕČŻĘ÷ÄŚ£¬800”ꏱ·“Ó¦£ŗ2NO(g)+O2(g) ![]() 2NO2(g)ĢåĻµÖŠ£¬n(NO)Ėꏱ¼äµÄ±ä»ÆČē±ķ£ŗ
2NO2(g)ĢåĻµÖŠ£¬n(NO)Ėꏱ¼äµÄ±ä»ÆČē±ķ£ŗ
Ź±¼ä(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
£Ø1£©“ļĘ½ŗāµÄŹ±¼äŹĒ £¬ĄķÓÉŹĒ ”£
£Ø2£©ÓŅĶ¼ÖŠ±ķŹ¾NO2µÄ±ä»ÆµÄĒśĻߏĒ ”£ÓĆO2±ķŹ¾“Ó0~2 sÄŚøĆ·“Ó¦µÄĘ½¾łĖŁĀŹv= ”£
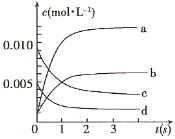
£Ø3£©ÄÜĖµĆ÷øĆ·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬µÄŹĒ ”£
a£®v(NO2) = 2v(O2) b£®ČŻĘ÷ÄŚø÷ĪļÖŹµÄÅØ¶Č±£³Ö²»±ä
c£®vÄę(NO) = 2vÕż(O2) d£®“ļµ½»ÆŃ§Ę½ŗāŹ±£¬NO½«ĶźČ«×Ŗ»ÆĪŖNO2
£Ø4£©ÄÜŌö“óøĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹŹĒ ”£
a£®¼°Ź±·ÖĄė³żNO2ĘųĢå b£®ŹŹµ±ÉżøßĪĀ¶Č
c£®Ōö“óO2µÄÅØ¶Č d£®Ń”Ōńøߊ§“߻ƼĮ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¾ŪŗĻĀČ»ÆĀĮŹĒŅ»ÖÖŠĀŠĶ¾»Ė®¼Į£¬ĘäÖŠĀĮµÄ×ÜÅضČ(ÓĆc±ķŹ¾£©°üĄØČżĄą£ŗÖ÷ŅŖĪŖA l3+µÄµ„ĢåŠĪĢ¬ĀĮ£ØÓĆAla±ķŹ¾£©×ÜÅØ¶Č£¬Ö÷ŅŖĪŖÖ÷ŅŖĪŖ[AlO4 Al12(OH)24(H2O)12 ]7+µÄÖŠµČ¾ŪŗĻŠĪĢ¬ĀĮ×ÜÅضČ(ÓĆAlb ±ķŹ¾)ŗĶAl(OH)3½ŗĢåŠĪĢ¬ĀĮ(ÓĆA1c±ķŹ¾)×ÜÅØ¶Č”£
£Ø1£©ÕęæÕĢ¼ČČ»¹ŌŅ»Ńõ»Æ·ØæÉŹµĻÖÓÉĀĮĶĮæóÖʱø½šŹōĀĮ£¬Ļą¹Ų·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ČēĻĀ£ŗ
¢ŁAl2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g)”÷H1=akJ”¤mol-1
¢Ś3AlCl(g)= 2Al(s)+AlCl3(g) ”÷H2=bkJ”¤mol-1
Ōņ·“Ó¦Al2O3(s)+33C(s)= 2Al(s)+ 3CO(g)”÷H=______kJ”¤mol-1£ØÓĆŗ¬a”¢bµÄ“śŹżŹ½±ķ¶ū£©”£ ·“Ó¦¢ŁŌŚ³£Ń¹”¢1900 ”ę µÄøßĪĀĻĀ²ÅÄܽųŠŠ£¬ĖµĆ÷”÷H______( Ģī”°>”±”°=”±»ņ”°<”±£©”£
£Ø1£©ÓĆĤÕōĮó£Ø¼ņ³ĘMD£©ÅØĖõ¼¼Źõ½«¾ŪŗĻĀČ»ÆĀĮČÜŅŗ½ųŠŠÅØĖõ£¬ŹµŃé¹ż³ĢÖŠ²»Ķ¬ÅØ¶Č¾ŪŗĻĀČ»ÆĀĮČÜŅŗÖŠĀĮŠĪĢ¬·Ö²¼£Ø°Ł·ÖŹż£©ČēĻĀ±ķ£ŗ
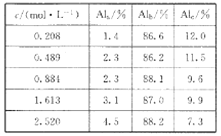
¢ŁŌŚŅ»¶ØĪĀ¶ČĻĀ£¬cŌ½“ó,Al(OH)3½ŗĢåµÄ°Ł·Öŗ¬Įæ______(Ģī”°Ō½“ó”±”°Ō½Š””±»ņ”°²»±ä”±)”£
¢ŚČō½«c=2.520mol/LµÄ¾ŪŗĻĀČ»ÆĀĮČÜŅŗ¼ÓĖ®Ļ”ŹĶ£¬ŌņĻ”ŹĶ¹ż³ĢÖŠ·¢ÉśµÄÖ÷ŅŖ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_____________”£
£Ø3£©Ņ»¶ØĢõ¼žĻĀ£¬Ļņ1.0mol/LµÄAlCl3ČÜŅŗÖŠ¼ÓČė0.6 mol/LµÄNaOHČÜŅŗ£¬æÉÖʵĆAlbŗ¬ĮæŌ¼ĪŖ86 % µÄ¾ŪŗĻĀČ»ÆĀĮČÜŅŗ”£Š“³öÉś³É[AlO4 Al12(OH)24(H2O)12 ]7+µÄĄė×Ó·½³ĢŹ½£ŗ_______”£
£Ø4£©ŅŃÖŖAl3++4X=2![]() £¬X±ķŹ¾ĻŌÉ«¼Į£¬
£¬X±ķŹ¾ĻŌÉ«¼Į£¬ ![]() ±ķŹ¾ÓŠÉ«ĪļÖŹ£¬Ķعż±ČÉ«·ÖĪöµĆµ½25 ”ꏱAl3+ÅضČĖꏱ¼äµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø³õŹ¼Ź±XµÄÅضČĪŖ0.194mol”¤L-1£©”£
±ķŹ¾ÓŠÉ«ĪļÖŹ£¬Ķعż±ČÉ«·ÖĪöµĆµ½25 ”ꏱAl3+ÅضČĖꏱ¼äµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø³õŹ¼Ź±XµÄÅضČĪŖ0.194mol”¤L-1£©”£

¢Ł1minŹ±, ![]() µÄÅضČĪŖ___________”£
µÄÅضČĪŖ___________”£
¢Ś0”«3minÄŚøĆ·“Ó¦µÄĖŁĀŹvx£½________”£
¢ŪµŚ9minŹ±£¬·“Ó¦“ļµ½Ę½ŗā£¬K=__________(ÓĆ“śŹżŹ½±ķŹ¾£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŌNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£Źż£¬Ōņ¹ŲÓŚČČ»Æѧ·½³ĢŹ½£ŗ
C2H2(g)£«![]() O2(g)===2CO2(g)£«H2O(l) ¦¤H£½£1300 kJ/molµÄĖµ·ØÖŠ£¬ÕżČ·µÄŹĒ( )
O2(g)===2CO2(g)£«H2O(l) ¦¤H£½£1300 kJ/molµÄĖµ·ØÖŠ£¬ÕżČ·µÄŹĒ( )
A. µ±ÓŠ6 NAøöµē×Ó×ŖŅĘŹ±£¬øĆ·“Ó¦·Å³ö1300 kJµÄÄÜĮæ
B. µ±ÓŠ1NAøöĖ®·Ö×ÓÉś³ÉĒŅĪŖŅŗĢåŹ±£¬ĪüŹÕ1300 kJµÄÄÜĮæ
C. µ±ÓŠ4NAøöĢ¼Ńõ¹²ÓƵē×Ó¶ŌÉś³ÉŹ±£¬·Å³ö1300 kJµÄÄÜĮæ
D. µ±ÓŠ8NAøöĢ¼Ńõ¹²ÓƵē×Ó¶ŌÉś³ÉŹ±£¬·Å³ö1300 kJµÄÄÜĮæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ[»Æѧ”Ŗ”ŖŃ”ŠŽ3£ŗĪļÖŹ½į¹¹ÓėŠŌÖŹ]Ēā»ÆĀĮÄĘ£ØNaAlH4£©ŹĒŅ»ÖÖŠĀŠĶĒįÖŹ“¢Ēā²ÄĮĻ£¬²ōČėÉŁĮæTiµÄNaAlH4ŌŚ150”ꏱŹĶĒā£¬ŌŚ170”ę”¢15.2MPaĢõ¼žĻĀÓÖÖŲø“ĪüĒā”£NaAlH4æÉÓÉAlCl3ŗĶNaHŌŚŹŹµ±Ģõ¼žĻĀŗĻ³É”£NaAlH4µÄ¾§°ū½į¹¹ČēÓŅĻĀĶ¼ĖłŹ¾”£

£Ø1£©»łĢ¬TiŌ×ӵļŪµē×Ó¹ģµĄ±ķŹ¾Ź½ĪŖ ”£
£Ø2£©NaHµÄČŪµćĪŖ800”ę£¬²»ČÜÓŚÓŠ»śČܼĮ”£NaHŹōÓŚ ¾§Ģ壬Ęäµē×ÓŹ½ĪŖ ”£
£Ø3£©AlCl3ŌŚ178”ꏱɿ»Ŗ£¬ĘäÕōĘųµÄĻą¶Ō·Ö×ÓÖŹĮæŌ¼ĪŖ267£¬ÕōĘų·Ö×ӵĽį¹¹Ź½ĪŖ £Ø±źĆ÷ÅäĪ»¼ü£©”£
£Ø4£©AlH4£ÖŠ£¬AlµÄ¹ģµĄŌӻƷ½Ź½ĪŖ £»Ąż¾ŁÓėAlH4£æռ乹ŠĶĻąĶ¬µÄĮ½ÖÖĄė×Ó £ØĢī»ÆѧŹ½£©”£
£Ø5£©NaAlH4¾§ĢåÖŠ£¬ÓėNa+½ōĮŚĒŅµČ¾ąµÄAlH4£ÓŠ øö£»NaAlH4¾§ĢåµÄĆܶČĪŖ g”¤cm£3£ØÓĆŗ¬aµÄ“śŹżŹ½±ķŹ¾£©”£ČōNaAlH4¾§°ūµ×ŠÄ“¦µÄNa+±»Li+Č”“ś£¬µĆµ½µÄ¾§ĢåĪŖ £ØĢī»ÆѧŹ½£©”£
£Ø6£©NaAlH4µÄŹĶĒā»śĄķĪŖ£ŗĆæ3øöAlH4£ÖŠ£¬ÓŠ2øö·Ö±šŹĶ·Å³ö3øöHŌ×ÓŗĶ1øöAlŌ×Ó£¬Ķ¬Ź±ÓėøĆAlŌ×Ó×ī½üĮŚµÄNaŌ×Ó×ŖŅʵ½±»ŹĶ·ÅµÄAlŌ×ÓĮōĻĀµÄæÕĪ»£¬ŠĪ³ÉŠĀµÄ½į¹¹”£ÕāÖÖ½į¹¹±ä»ÆÓɱķĆę²ćĄ©Õ¹µ½Õūøö¾§Ģ壬“Ó¶ųŹĶ·Å³öĒāĘų”£øĆŹĶĒā¹ż³ĢæÉÓĆ»Æѧ·½³ĢŹ½±ķŹ¾ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¹ĢĢåAµÄ»ÆѧŹ½ĪŖNH5£¬ĖüµÄĖłÓŠŌ×ÓµÄ×īĶāµē×Ó²ć½į¹¹¶¼·ūŗĻĻąÓ¦Ļ”ÓŠĘųĢåµÄ×īĶāµē×Ó²ć½į¹¹£¬ŌņĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ( )
A. 1 mol NH5ÖŠŗ¬ÓŠ5NAøöN£H¼ü(NA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄŹżÖµ)
B. NH5ÖŠ¼ČÓŠ¹²¼Ū¼üÓÖÓŠĄė×Ó¼ü
C. NH5µÄµē×ÓŹ½ĪŖ![]()
D. NH5ÓėĖ®·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖNH![]() £«H££«H2O===NH3”¤H2O£«H2”ü
£«H££«H2O===NH3”¤H2O£«H2”ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
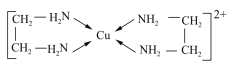
”¾ĢāÄæ”æGaN”¢GaP”¢GaAsŹĒČĖ¹¤ŗĻ³ÉµÄŅ»ĻµĮŠŠĀŠĶ°ėµ¼Ģå²ÄĮĻ£¬Ę侧Ģå½į¹¹¾łÓė½šøÕŹÆĻąĖĘ”£ĶŹĒÖŲŅŖµÄ¹ż¶ÉŌŖĖŲ£¬ÄÜŠĪ³É¶ąÖÖÅäŗĻĪļ£¬ČēCu2£«ÓėŅŅ¶ž°·£ØH2N-CH2-CH2-NH2£©æÉŠĪ³ÉČēĶ¼ĖłŹ¾ÅäĄė×Ó”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©»łĢ¬GaŌ×Ó¼Ūµē×ӵĹģµĄ±ķ“ļŹ½ĪŖ________________£»
£Ø2£©ČŪµć£ŗGaN_____GaP£ØĢī”°>”±»ņ”°<”±£©£»
£Ø3£©µŚŅ»µēĄėÄÜ£ŗAs_____Se£ØĢī”°>”±»ņ”°<”±£©£»
£Ø4£©Cu2£«ÓėŅŅ¶ž°·ĖłŠĪ³ÉµÄÅäĄė×ÓÄŚ²æ²»ŗ¬ÓŠµÄ»Æѧ¼üĄąŠĶŹĒ______£»
a£®ÅäĪ»¼ü b.¼«ŠŌ¼ü c£®Ąė×Ó¼ü d£®·Ē¼«ŠŌ¼ü
£Ø5£©ŅŅ¶ž°··Ö×ÓÖŠµŖŌ×Ó¹ģµĄµÄŌÓ»ÆĄąŠĶĪŖ________£¬ŅŅ¶ž°·ŗĶČż¼×°·[N(CH3)3]¾łŹōÓŚ°·”£µ«ŅŅ¶ž°·±ČČż¼×°·µÄ·Šµćøßŗܶą£¬ŌŅņŹĒ___________£»
£Ø6£©CuµÄijÖÖ¾§Ģ徧°ūĪŖĆęŠÄĮ¢·½½į¹¹£¬¾§°ū±ß³¤ĪŖacm£¬ĶŌ×ӵİė¾¶ĪŖrcm”£øĆ¾§ĢåÖŠĶŌ×ӵĶѻż·½Ź½ĪŖ_______ŠĶ£ØĢī”°A1”±”¢”°A2”±»ņ”°A3”±£©£¬øĆ¾§ĢåĆܶČĪŖ____g/cm3£ØÓĆŗ¬aŗĶNAµÄ“śŹżŹ½±ķ“ļ£©£¬øĆ¾§ĢåÖŠĶŌ×ÓµÄæÕ¼äĄūÓĆĀŹĪŖ______£ØÓĆŗ¬aŗĶrµÄ“śŹżŹ½±ķ“ļ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚ ¢ŁŅŅĻ© ¢Ś±½ ¢ŪŅŅ“¼ ¢ÜŅŅĖį ¢ŻĘĻĢŃĢĒµČÓŠ»śĪļµÄŠšŹö²»ÕżČ·µÄŹĒ
A£®æÉŅŌÓĆŠĀÖʵÄCu£ØOH£©2Šü×ĒŅŗ¼ų±š¢Ū¢Ü¢Ż
B£®Ö»ÓŠ¢Ł¢Ū¢ŻÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«
C£®Ö»ÓŠ¢Ś¢Ū¢ÜÄÜ·¢ÉśČ”“ś·“Ó¦
D£®Ņ»¶ØĢõ¼žĻĀ£¬¢ŻæÉŅŌ×Ŗ»ÆĪŖ¢Ū
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com