
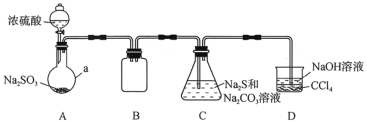
【题目】硫代硫酸钠(Na2S2O3)是一种重要的化工产品。某研究小组制备硫代硫酸钠晶体(Na2S2O3·5H2O)的实验装置如图所示(省略夹持装置):
(查阅资料)
Ⅰ.Na2S2O3·5H2O是无色晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成;
Ⅱ.向Na2CO3和Na2S混合液中通入SO2可制得Na2S2O3。
根据题意,填写下列空白。
(1)仪器a的名称是___;B的作用是___。
(2)C中反应氧化剂与还原剂的物质的量之比为___。
(3)该实验制取的产品中常含有少量Na2SO3和Na2SO4杂质。为了检验产品中是否含有这两种杂质,某小组设计了以下实验方案(所需试剂从稀硝酸、稀硫酸、稀盐酸、蒸馏水中选择),请将方案补充完整。
取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,过滤、洗涤后,向沉淀中滴加足量的___(填试剂名称),若___(填实验现象),则可以确定产品中含有Na2SO3和Na2SO4。
(4)称取样品137.5g配成500mL溶液。取50mL溶液,向其中加入足量稀硫酸,充分反应(S2O![]() +2H+=S↓+SO2↑+H2O),静置、过滤、洗涤、干燥、称量得沉淀1.6g。
+2H+=S↓+SO2↑+H2O),静置、过滤、洗涤、干燥、称量得沉淀1.6g。
准确配制500mL溶液所需仪器有:天平、药匙、烧杯、玻璃棒、___、___。经计算,样品中硫代硫酸晶体的百分含量为___。(保留三位有效数字)
【答案】圆底烧瓶 防止倒吸 2:1 稀盐酸 沉淀部分溶解,并有刺激性气味的气体产生 胶头滴管 500mL容量瓶 90.2%
【解析】
根据装置:A装置制备二氧化硫,B装置为安全瓶,C装置由二氧化硫与Na2CO3和Na2S混合液反应制得Na2S2O3,D装置吸收尾气,
(1)根据仪器a的构造可得名称,B为安全瓶;
(2)C中Na2CO3、Na2S和SO2反应制得Na2S2O3,根据化合价分析可得;
(3)根据亚硫酸钡溶解于稀盐酸并且有刺激性气味的气体产生,硫酸钡不溶解于稀盐酸来分析;
(4)配制溶液所需仪器有:天平、药匙、烧杯、玻璃棒、胶头滴管、容量瓶;沉淀1.6g为生成的S,S物质的量为0.05mol,根据反应S2O32-+2H+=S↓+SO2↑+H2O,则有:Na2S2O35H2O~S,则产品中Na2S2O35H2O的物质的量为0.05mol×![]() =0.5mol,据此计算可得。
=0.5mol,据此计算可得。
(1)仪器a为圆底烧瓶;B的作用是安全瓶,防止倒吸;故答案为:圆底烧瓶;防止倒吸;
(2)C中Na2CO3、Na2S和SO2反应制得Na2S2O3,SO2中硫元素化合价降低2价,被还原,为氧化剂,Na2S中硫元素化合价升高4价,被氧化,为还原剂,根据得失电子守恒,故氧化剂与还原剂的物质的量之比为2:1;故答案为:2:1;
(3)根据资料,硫代硫酸钠稀溶液与氯化钡溶液混合无沉淀生成,因为BaSO3难溶于水,可溶于稀盐酸并且有刺激性气味的气体产生,硫酸钡不溶解于稀盐酸,故检验产品中是否含有少量Na2SO3和Na2SO4杂质的方法为:取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,过滤、洗涤后,向沉淀中滴加足量的稀盐酸,若沉淀部分溶解,并有刺激性气味的气体产生,则可以确定产品中含有Na2SO3和Na2SO4;故答案为:稀盐酸;沉淀部分溶解,并有刺激性气味的气体产生;
(4)准确配制500mL溶液所需仪器有:天平、药匙、烧杯、玻璃棒、胶头滴管、500mL容量瓶;沉淀1.6g为生成的S,S物质的量为0.05mol,根据反应S2O32+2H+=S↓+SO2↑+H2O,则有:Na2S2O35H2OS,则产品中Na2S2O35H2O的物质的量为0.05mol×![]() =0.5mol,故样品中硫代硫酸钠晶体的百分含量为
=0.5mol,故样品中硫代硫酸钠晶体的百分含量为![]() ×100%=90.2%;故答案为:胶头滴管;500mL容量瓶;90.2%。
×100%=90.2%;故答案为:胶头滴管;500mL容量瓶;90.2%。


科目:高中化学 来源: 题型:
【题目】向Fe和Fe2O3组成的3.84 g 混合物中加入120 mL某浓度的盐酸,恰好完全反应,生成672mLH2(标准状况下),若向反应后的溶液中滴入几滴KSCN溶液,溶液不呈红色。试求:
(1)原混合物中Fe2O3和Fe的质量分别为_______、________;
(2)原盐酸的物质的量浓度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)广泛存在于以煤为原料的各种化工原料气中,能引起催化剂中毒、化学产品质量下降和大气污染。
(1)羰基硫的水解反应和氢解反应是两种常用的脱硫方法:
水解反应:COS(g)+H2O(g)![]() H2S(g)+CO2(g) △H=-34kJ/mol
H2S(g)+CO2(g) △H=-34kJ/mol
氢解反应:COS(g)+H2(g) ![]() H2S(g)+CO(g) △H=+7kJ/mol。
H2S(g)+CO(g) △H=+7kJ/mol。
已知:2H2(g)+O2(g)=2H2O(g) △H=-484kJ/mol。
写出表示CO燃烧热的热化学方程式:______________。
(2)氢解反应达到平衡后,保持体系的温度和总压强不变,通入适量的He,正反应速率____(填“增大”“减小”或“不变”,下同),COS的转化率_______。
(3)某温度下,向体积为2L的恒容密闭容器中通入2molCOS(g)和4molH2O(g),发生水解反应,5min后反应达到平衡,测得COS(g)的转化率为75%。
回答下列问题:
①反应从起始至5min内,v(H2S)=_______mol·L-1·min-1。
②该温度下,上述水解反应的平衡常数K=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
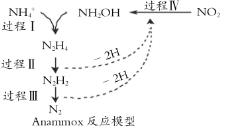
【题目】厌氧氨化法(Anammox)是一种新型的氨氮去除技术,下列说法中正确的是
A.1mol NH4+所含的质子总数为 10NA
B.联氨(N2H4)中含有离子键和非极性键
C.过程 II 属于氧化反应,过程 IV 属于还原反应
D.过程 I 中,参与反应的 NH4+ 与 NH2OH 的物质的量之比为 1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.SiO2既能和NaOH溶液反应,又能和HF反应,所以SiO2属于两性氧化物
B.因为Na2CO3+SiO2![]() Na2SiO3+CO2↑,所以H2SiO3的酸性比H2CO3强
Na2SiO3+CO2↑,所以H2SiO3的酸性比H2CO3强
C.CO2和SiO2都能与C反应
D.CO2和SiO2都是酸性氧化物,所以两者物理性质相似
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某元素的价类二维图。其中X是一种强碱,G为正盐,通常条件下Z是无色液体,D的相对原子质量比C小16,各物质转化关系如图所示。下列说法正确的是

A.E 可以是金属也可以是非金属
B.C 和 D 两种大气污染物,都能用排空气法收集
C.B 的浓溶液具有吸水性,可用来干燥气体
D.实验室制备 F 时,可以将其浓溶液滴入碱石灰中进行制取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W 四种物质有如下相互转化关系(其中 Y、Z 为化合物,未列出反应条件)。
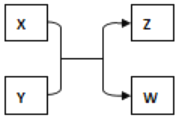
(1)若实验室经常用澄清石灰水来检验 X 的燃烧产物,W 的用途之一是计算机芯片,W 在周期表中的位置为 ___________,Y 的用途有 _________,写出Y与NaOH 溶液反应的离子方程式 _________。
(2)若 X、W 为日常生活中常见的两种金属,且 Y 常用作红色油漆和涂料,则该反应的化学方程式为___________。
(3)若 X 为淡黄色粉末,Y 为生活中常见液体,则:
①X 的电子式为 _______________,该反应的化学方程式为 ____________,生成的化合物中所含化学键类型有 ________________________。
② 若 7.8 克 X 物质完全反应,转移的电子数为 ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.纯净的水晶是由硅原子和氧原子构成的,每个原子的最外层均具有8电子稳定结构
B.Na2O是由离子构成的,其溶于水形成溶液的过程中既有离子键、共价键的断裂又有共价键的形成
C.现代科技已经能够拍到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键
D.NH5中所有原子的最外层都符合相应的稀有气体原子的最外层电子结构,是既含有离子键又含有共价键的离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲用98%的浓H2SO4(ρ=1.84g/cm3)配制成500mL 0.5mol/L的稀H2SO4
(1)填写下列操作步骤:
①所需浓H2SO4的体积为____。
②如果实验室有10mL、20mL、50mL量筒,应选用___mL量筒量取。
③将量取的浓H2SO4沿玻璃棒慢慢注入盛有约100mL水的___里,并不断搅拌,目的是___。
④立即将上述溶液沿玻璃棒注入____中,并用50mL蒸馏水洗涤烧杯2~3次,并将洗涤液注入其中,并不时轻轻振荡。
⑤加水至距刻度___处,改用__加水,使溶液的凹液面正好跟刻度相平。盖上瓶塞,上下颠倒数次,摇匀。
(2)请指出上述操作中一处明显错误:____。
(3)误差(填偏高、偏低、无影响)
①操作②中量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将___;
②问题(2)的错误操作将导致所配制溶液的浓度___;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com