
| A. | 体积相等时密度之比为2:1 | |
| B. | 原子数相等时具有的电子数之比为1:4 | |
| C. | 质量相等时具有的质子数之比为4:5 | |
| D. | 体积相等时具有的原子数之比为1:2 |
分析 A.依据ρ=$\frac{M}{Vm}$判断;
B.1个甲烷分子含有5个原子,10个电子,1个氧气分子含有2个原子,16个电子;
C.1个甲烷分子含有10个质子,1个氧气分子含有16个质子;
D.同温同压下的两种气体CH4和O2的体积相等,则具有相同的分子数,结合甲烷为5原子分子,氧气为双原子分子解答.
解答 解:A.依据ρ=$\frac{M}{Vm}$,同温同压下,密度与M成正比,所以CH4和O2密度为:16:32=1:2,故A错误;
B.CH4和O2的原子数相等,则二者物质量之比为:2:5,具有的电子数之比为:2×10:5×16=1:4,故B正确;
C.CH4和O2质量相等时,物质量之比为:$\frac{1}{16}$:$\frac{1}{32}$=2:1,具有的质子数之比为2×10:1×16=5:4,故C错误;
D.同温同压下的两种气体CH4和O2的体积相等,则具有相同的分子数,具有的原子数之比为:1×5:1×2=5:2,故D错误;
故选:B.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握相关物理量与计算公式的运用,难度不大.


科目:高中化学 来源: 题型:选择题
 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )| A. | 若Z是KCl溶液,则电解时溶液中Cl-向Y极移动 | |
| B. | 铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4 | |
| C. | 外加电流的阴极保护法中,Y是待保护金属 | |
| D. | 电解硫酸溶液一段时间后,加适量水可使溶液恢复到原溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每种烃的含氧衍生物中至少有3种元素 | |
| B. | 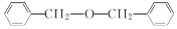 中含有的官能团为醚基 中含有的官能团为醚基 | |
| C. | 所有的有机物中都含有碳,多数含氢,其次还含有氧、氮、卤素、硫、磷等 | |
| D. | 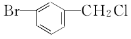 属于芳香卤代烃 属于芳香卤代烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作和现象 | 结论 |
| A | 测定等物质的量浓度的Na2CO3和Na2SO3溶液的pH,前者的pH比后者的大 | 元素非金属性:S>C |
| B | 向盛有Fe(NO3)2溶液的试管中加入0.1mol•L-1 H2SO4溶液,试管口出现红棕色气体 | 溶液中NO被Fe2+还原为NO2 |
| C | 向FeBr2溶液中加入少量氯水,再加CCl4萃取,CCl4层无色 | Fe2+的还原性强于Br- |
| D | 向溶液中滴加盐酸酸化的BaCl2溶液,产生白色沉淀 | 溶液中一定含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1 | B. | 1:2 | C. | 4:1 | D. | 1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
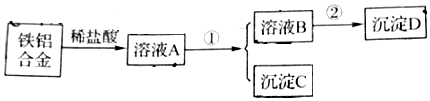
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
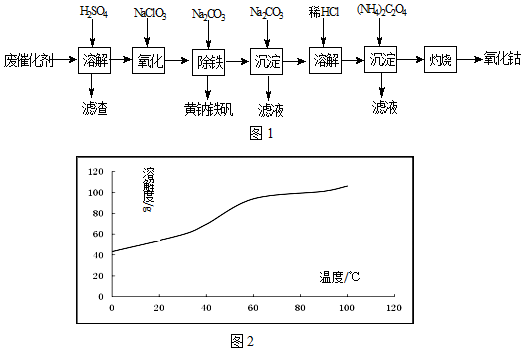
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
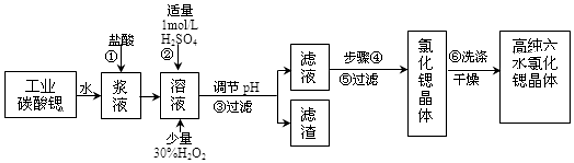
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 |
| 沉淀完全的pH | 3.7 | 9.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
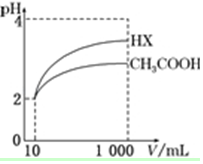 25℃时,部分物质的电离常数如表所示:
25℃时,部分物质的电离常数如表所示:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com