根据已学知识,请你回答下列问题:
(1)写出原子序数最小的第Ⅷ族元素原子的原子结构示意图为:
.
(2)写出3p轨道上有2个未成对电子的元素的符号:
Si或S
Si或S
.
(3)该元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是4s
24p
4,该元素的名称是
硒
硒
.
(4)第三主族的元素由于最外能层的p能级中有空轨道,故称为缺电子元素.硼酸的结构式可表示为
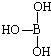
,但硼酸溶于水后,1个硼酸分子与水作用,只能产生1个H
+,请写出硼酸溶于水后溶液显酸性的离子方程式:
B(OH)3+H2O?B(OH)4-+H+
B(OH)3+H2O?B(OH)4-+H+
.
(5)写出二氧化硫和水合氢离子中硫原子,氧原子分别采用
sp2
sp2
和
sp3
sp3
杂化形式,其空间构型分别为
V形
V形
和
三角锥型
三角锥型
.
(6)已知N-N,N=N,N≡N键能之比为1.00:2.17:4.90,而C-C,C=C,C≡C键能之比为1.00:1.77:2.34.用数据分析氮分子不容易发生加成反应而乙烯和乙炔容易发生加成反应的原因
N≡N键能大于N-N键能的三倍,N=N的键能大于N-N的二倍,而C≡C键能小于C-C键能的三倍,C=C键能小于C-C键能的二倍.说明乙烯和乙炔中的π键不牢固,容易被试剂进攻,故易发生加成反应.而氮分子中N≡N非常牢固,不易发生加成反应
N≡N键能大于N-N键能的三倍,N=N的键能大于N-N的二倍,而C≡C键能小于C-C键能的三倍,C=C键能小于C-C键能的二倍.说明乙烯和乙炔中的π键不牢固,容易被试剂进攻,故易发生加成反应.而氮分子中N≡N非常牢固,不易发生加成反应
.
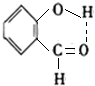
(7)用氢键表示法表示邻羟基苯甲醛分子内氢键
.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案

 ,但硼酸溶于水后,1个硼酸分子与水作用,只能产生1个H+,请写出硼酸溶于水后溶液显酸性的离子方程式:
,但硼酸溶于水后,1个硼酸分子与水作用,只能产生1个H+,请写出硼酸溶于水后溶液显酸性的离子方程式: