
关于催化剂的叙述,正确的是( )
A.催化剂在化学反应前后性质不变
B.催化剂在反应前后质量不变,故催化剂不参加化学反应
C.使用催化剂可以改变反应达到平衡的时间
D.催化剂可以提高反应物的转化率
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
已知NaNO2的化学式量为69,则500mL 1.0 mol·L-1 NaNO2溶液含有溶质质量为( )。
A.13.8g B.69g C.34.5g D.138g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )。
A.铅笔芯的主要成分是金属铅,儿童在使用是不可用嘴吮吸,以免引起铅中毒
B.CO气体有毒,在生有炉火的居室中多放几盆水,可吸收CO,防止煤气中毒
C.含氟冰箱产生的氟利昂是造成臭氧空洞的主要原因
D.油条制作中常加入明矾作膨化剂,有利于补充身体所需微量元素,是理想的早餐
查看答案和解析>>
科目:高中化学 来源: 题型:
生活中的一些问题常涉及化学知识。下列叙述中,不正确的是( )。
A.甲型H1N1流感病毒是一种油脂
B.我们所吃的豆腐中主要含有蛋白质
C.棉花和蚕丝的主要成分都是纤维素
D.糯米中的淀粉一经发生水解反应就酿造成酒
查看答案和解析>>
科目:高中化学 来源: 题型:
2007年诺贝尔化学奖得主——德国科学家格哈德·埃特尔对有关一氧化碳在金属铂表面的氧化过程的研究催生了汽车尾气净化装置。净化装置中的催化转化器可将CO、NO、NO2等转化为无害的物质。下列有关说法不正确的是( )
A.催化转化器中的铂催化剂可加快CO的氧化
B.铂表面做成蜂窝状更有利于提高催化效果
C.在铂催化下,NO、NO2可被CO还原成N2
D.使用铂催化剂,可以提高碳氢化合物被氧化的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车尾气在光照下分解时,即开始光化学烟雾的循环,它的形成过程可用下列化学方程式表示:NO2===NO+O,2NO+O2===2NO2,O2+O===O3。下列有关叙述不正确的是( )
A.此过程中,NO2是催化剂
B.在此过程中,NO是中间产物
C.此过程的总反应方程式为2O3===3O2
D.光化学烟雾能引起人的外呼吸功能严重障碍
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组在进行双氧水分解的实验时发现:大家取不同浓度的双氧水及不同质量的二氧化锰进行的实验,产生气体的速率都不相同,那么过氧化氢分解的最佳催化条件是什么呢?他们决定进行探究。
(1)用下列简图,画出实验装置(含试剂)示意图。

(2)小组经过实验,取得如下数据:
|
Z | 0.1 g | 0.3 g | 0.5 g |
| 1.5% | 223 s | 67 s | 56 s |
| 3.0% | 308 s | 109 s | 98 s |
| 4.5% | 395 s | 149 s | 116 s |
(说明:表中X是二氧化锰的质量;Y是指反应停止时的时间;Z是双氧水的质量分数)分析表中数据回答下列问题:
①相同浓度的双氧水的分解速率随着二氧化锰用量的增加而________。
②从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入________g的二氧化锰为较佳选择,理由是
________________________________________________________________________
________________________________________________________________________。
③该小组的小茂同学分析上述数据后得出“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越小,亦即其反应速率越快”的结论,你认为是否正确?________,理由是________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
以化学平衡移动原理为依据,解释以下事实。
(1)在氨水中加入氢氧化钠溶液,有氨气逸出
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)合成氨工业中将氨气液化,可以提高氨的产量
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(3)用热水溶解碳酸钠晶体(Na2CO3·10H2O),可提高去污能力
________________________________________________________________________
________________________________________________________________________。
(4)打开冰冻啤酒倒入玻璃杯,杯中立即泛起大量泡沫
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
表示下列反应的离子方程式正确的是
A.铁溶于稀盐酸:2Fe+6H+=2Fe3++3H2↑
B.氯化铝溶液中加过量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH4+
C.碳酸氢铵溶液中加足量氢氧化钠并加热:NH4++OH- H2O+NH3↑
H2O+NH3↑
D.氯气通入水中,溶液呈酸性:Cl2+H2O 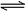 2H++Cl-+ClO-
2H++Cl-+ClO-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com