
【题目】一种离子晶体的晶胞如图,其中阳离子A以![]() 表示,阴离子B以
表示,阴离子B以![]() 表示。
表示。
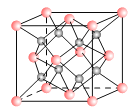
(1)每个晶胞中含A离子的数目为______,含B离子数目为_______。
(2)若A的核外电子排布与Ne相同,B的电子排布与Ar相同,则该离子化合物的化学式是___________;
(3)阳离子周围距离最近的阳离子数为_____,阳离子周围距离最近的阴离子数_____。
【答案】 4 8 MgCl2 12 8
【解析】(1)A离子位于立方体的顶点和面心位置,数目为![]() ,B离子位于立方体内部,数目为8。正确答案:4、8。(2)有A分析可知该晶体化学式为AB2,所以阳离子A为A2+,A的核外电子排布与Ne相同,所以A2+是Mg2+,阴离子B为B-,B的电子排布与Ar相同,所以B-是Cl-,该离子化合物是MgCl2。(3)如下图Ⅱ,以底面右前顶点的一个阳离子作为研究对象,图中该点对应原图的正面、侧面、底面各有一个距离最近的阳离子,由于晶胞在各方向“无隙并置”,所以三个面应当各有4个距离最近的阳离子,所以距离最近的阳离子数目为12。以正面面心的阳离子作为研究对象,距离最近的阴离子为紧贴这一侧的四个阴离子(如下图Ⅰ),由于晶胞在各方向“无隙并置”,所以对应还有4个阴离子,既距离最近的阴离子数8。正确答案:12、8。
,B离子位于立方体内部,数目为8。正确答案:4、8。(2)有A分析可知该晶体化学式为AB2,所以阳离子A为A2+,A的核外电子排布与Ne相同,所以A2+是Mg2+,阴离子B为B-,B的电子排布与Ar相同,所以B-是Cl-,该离子化合物是MgCl2。(3)如下图Ⅱ,以底面右前顶点的一个阳离子作为研究对象,图中该点对应原图的正面、侧面、底面各有一个距离最近的阳离子,由于晶胞在各方向“无隙并置”,所以三个面应当各有4个距离最近的阳离子,所以距离最近的阳离子数目为12。以正面面心的阳离子作为研究对象,距离最近的阴离子为紧贴这一侧的四个阴离子(如下图Ⅰ),由于晶胞在各方向“无隙并置”,所以对应还有4个阴离子,既距离最近的阴离子数8。正确答案:12、8。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
【题目】家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是
A. 4Fe(OH)2+2H2O+O2===4Fe(OH)3↓
B. 2Fe+2H2O+O2===2Fe(OH)2↓
C. 2H2O+O2+4e-===4OH-
D. Fe-3e-===Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A. 气体单质中,一定有σ键,可能有π键 B. σ键比π键重叠程度大,形成的共价键强
C. 两个原子间形成共价键时,最多有一个σ键 D. N2分子有一个σ键,两个π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧元素与多种元素具有亲和力,所形成化合物的种类很多。
(1)氮、氧、氟元素的第一电离能从大到小的顺序为__________。氧元素与氟元素能形成OF2分子,氧原子轨道杂化类型__________。
(2)根据等电子体原理,NO2+的空间构型是__________;1 molN O2+中含有的π键数目为__________个。
(3)氧元素和过渡元素可形成多种价态的金属氧化物,如和铬可生成Cr2O3、CrO3、CrO5等。基态铬原子外围电子排布式为__________。
(4)下列物质的分子与O3分子的结构最相似的是__________。
A.H2O B.CO2 C.SO2 D.BeCl2
(5)O3分子是否为极性分子?__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两种金属混合物3.4g,与足量的盐酸反应放出H22.24L(标况下),这两种金属可能是
A. 铜和铁 B. 镁和铝 C. 锌和铝 D. 锌和铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质,都能与Na反应放出H2,其产生H2的速率排列顺序正确的是( )
①C2H5OH ②稀盐酸 ③H2O
A.①>②>③B.②>①>③
C.③>①>②D.②>③>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列有关说法正确的是
A. 常温常压下,1.8g甲基(—CD3)中含有的中子数为NA
B. 标准状况下,11.2L乙烯和环丙烷(C3H6)的混合气体中,共用电子对的数目为3NA
C. 过量铜与含0.4 mol HNO3的浓硝酸反应,电子转移数大于0.2NA
D. 常温下,1L pH=9的CH3COONa溶液中,发生电离的水分子数为1×10-9 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知烯烃经臭氧氧化后,在Zn存在下水解,可得醛或酮.如:![]() ,现有化学式为C10H20的烯烃,它经臭氧氧化后在Zn存在下水解只生成一种有机物,符合该条件的结构共有( )种
,现有化学式为C10H20的烯烃,它经臭氧氧化后在Zn存在下水解只生成一种有机物,符合该条件的结构共有( )种
A. 4 B. 5 C. 6 D. 7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com