
| A£® | ŅŅĖįŅŅõ„”¢ŅŅ“¼”¢Ļõ»ł±½ | B£® | »·¼ŗĶ锢±½·Ó”¢¼ŗĻ© | ||
| C£® | ¼×Ėį”¢ŅŅČ©”¢ŅŅĖį | D£® | ¼ŗĶ锢ŅŅĖį”¢±½ |
·ÖĪö A£®ŅŅĖįŅŅõ„”¢Ļõ»ł±½²»ČÜÓŚĖ®£¬ĆÜ¶Č²»Ķ¬”¢ŅŅ“¼ÓėĖ®»ģČÜ£»
B£®æÉÓĆäåĖ®¼ų±š±½·Ó£¬¼ŗĻ©ÓėäåĖ®·¢Éś¼Ó³É·“Ó¦£»
C£®¼×Ėį”¢ŅŅČ©¶¼ŗ¬ÓŠČ©»ł£¬¼×Ėį”¢ŅŅĖį¶¼ŗ¬ōČ»ł£»
D£®¼ŗĶ锢±½ŠŌÖŹĪČ¶Ø£¬Ćܶȶ¼±ČĖ®Š”£®
½ā“š ½ā£ŗA£®ŅŅĖįŅŅõ„”¢Ļõ»ł±½²»ČÜÓŚĖ®£¬ŅŅĖįŅŅõ„ĆܶȱČĖ®Š”£¬Ļõ»ł±½ĆܶȱČĖ®“ó£¬ŅŅ“¼ÓėĖ®»ģČÜ£¬æɼų±š£¬¹ŹAÕżČ·£»
B£®æÉÓĆäåĖ®¼ų±š±½·Ó£¬¼ŗĻ©ÓėäåĖ®·¢Éś¼Ó³É·“Ó¦£¬»·¼ŗĶé²»·“Ó¦£¬ČÜŅŗ·Ö²ć£¬æɼų±š£¬¹ŹBÕżČ·£»
C£®¼×Ėį”¢ŅŅČ©¶¼ŗ¬ÓŠČ©»ł£¬¼×Ėį”¢ŅŅĖį¶¼ŗ¬ōČ»ł£¬æɼÓČėĒāŃõ»ÆĶ×ĒŅŗ¼ų±š£¬¼×ĶéÓėĒāŃõ»ÆĶŌŚ³£ĪĀĻĀ·¢ÉśÖŠŗĶ·“Ó¦£¬¼ÓČČŹ±·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬¶ųŅŅĖįÖ»·¢ÉśÖŠŗĶ·“Ó¦£¬ŅŅČ©Ö»·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬æɼų±š£¬¹ŹCÕżČ·£»
D£®¼ŗĶ锢±½ŠŌÖŹĪČ¶Ø£¬Ćܶȶ¼±ČĖ®Š”£¬²»Äܼų±š£¬¹ŹD“ķĪó£®
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»ÆѧŹµŃéÖŠµÄĪļÖŹµÄ¼ģŃéÖŖŹ¶£¬½ųŠŠĪļÖŹµÄ¼ģŃ鏱£¬ŅŖŅĄ¾ŻĪļÖŹµÄĢŲŹāŠŌÖŹŗĶĢŲÕ÷·“Ó¦£¬Ń”ŌńŹŹµ±µÄŹŌ¼ĮŗĶ·½·Ø£¬×¼Č·¹Ū²ģ·“Ó¦ÖŠµÄĆ÷ĻŌĻÖĻó£¬ČēŃÕÉ«µÄ±ä»Æ”¢³ĮµķµÄÉś³ÉŗĶČܽā”¢ĘųĢåµÄ²śÉśŗĶĘųĪ¶”¢»šŃęµÄŃÕÉ«µČ£¬½ųŠŠÅŠ¶Ļ”¢ĶĘĄķ£¬¼ų±šÓŠ»śĪļ³£ÓƵďŌ¼ĮÓŠ£ŗĖ®”¢äåĖ®”¢ĖįŠŌøßĆĢĖį¼Ų”¢ŠĀÖĘCu£ØOH£©2”¢FeCl3ČÜŅŗµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ńō¼« | Ņõ¼« | ČÜŅŗ¼× | ĪļÖŹŅŅ |
| A£®Pt | Pt | NaOH | NaOH¹ĢĢå |
| B£®Ķ | Ģś | CuSO4 | CuO |
| C£®C | Pt | NaCl | ŃĪĖį |
| D£®Pt | Pt | H2SO4 | H2O |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+”¢HCO3-”¢K+”¢OH- | B£® | Fe2+”¢H+”¢SO42-”¢NO3- | ||
| C£® | Fe3+”¢SCN-”¢NH4+”¢Cl- | D£® | AlO2-”¢OH-”¢Na+”¢NH4+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
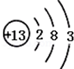 øł¾ŻČēĶ¼µÄŌ×Ó½į¹¹Ź¾ŅāĶ¼»Ų“šĻĀĮŠĪŹĢā£®
øł¾ŻČēĶ¼µÄŌ×Ó½į¹¹Ź¾ŅāĶ¼»Ų“šĻĀĮŠĪŹĢā£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £¬ĘäÓė¹żĮæµÄNaOHČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ
£¬ĘäÓė¹żĮæµÄNaOHČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ +2NaOH”ś
+2NaOH”ś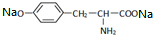 +2H2O£®ÓÉĄŅ°±ĖįÉś³É¾Ūõ„µÄ»Æѧ·½³ĢŹ½ŹĒ
+2H2O£®ÓÉĄŅ°±ĖįÉś³É¾Ūõ„µÄ»Æѧ·½³ĢŹ½ŹĒ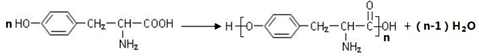 £®
£®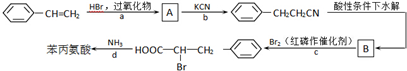
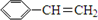 +HBr”ś
+HBr”ś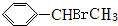 £®
£® +Br2$\stackrel{ŗģĮ×}{”ś}$
+Br2$\stackrel{ŗģĮ×}{”ś}$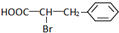 +HBr£®
+HBr£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | °±ĘųæÉÓĆÅÅĖ®·ØŹÕ¼Æ | |
| B£® | ĀČ»Æļ§¹ĢĢå¼ÓČČČŻŅ×·Ö½ā | |
| C£® | °±ĘųŗĶĖįĻąÓö¶¼ÄܲśÉś°×ŃĢ | |
| D£® | ŹµŃéŹŅÓĆĒāŃõ»ÆÄĘČÜŅŗŗĶĀČ»Æļ§ČÜŅŗ¼ÓČČÖĘNH3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com