
| A. | 一定温度和压强下,各种气态物质体积的大小,由构成气体的分子大小决定 | |
| B. | 不同的气体,若体积相同,则它们所含的分子数必相同 | |
| C. | 气体的摩尔体积是指1mol任何气体所占的体积都是22.4L | |
| D. | 恒温恒压条件下,反应前后气体的体积之比等于气体的物质的量之比 |
分析 A.一定温度和压强下,气体分子间的距离是一定的,各种气体物质体积的大小由分子数决定;
B.气体体积与温度、压强、气体分子数有关,体积相同,所含分子数不一定不同;
C.在标准状态下,1mol任何气体所占的体积约为22.4L;
D.恒温恒压条件下,气体摩尔体积相等,根据V=nVm分析解答.
解答 解:A.构成气体的分子大小相对于分子间距离忽略不计,一定温度和压强下,气体分子间的距离是一定的,各种气体物质体积的大小由由分子数决定,故A错误;
B.决定气体的体积因素是温度、压强、气体的分子数,不同气体,若体积相同,它们所含的分子数不一定不同,还受温度、压强条件的制约,故B错误;
C.气体摩尔体积指1mol任何气体所占的体积,在标准状态下1mol任何气体所占的体积约为22.4L,故C错误;
D.恒温恒压条件下,气体摩尔体积一定,根据V=nVm知,气体的体积之比等于其物质的量之比,故D正确;
故选D.
点评 本题考查了阿伏伽德罗常数的应用,主要考查了阿伏伽德罗常数概念应用,气体摩尔体积的概念和条件应用,掌握基础是解题关键,题目较简单.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
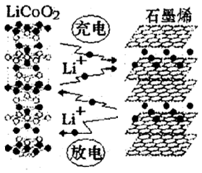 2016年12月1日,华为宣布:利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LixC6+Li1-xCoO2 $?_{充电}^{放电}$C6+LiCoO2,其工作原理如图.下列关于该电池的说法正确的是( )
2016年12月1日,华为宣布:利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LixC6+Li1-xCoO2 $?_{充电}^{放电}$C6+LiCoO2,其工作原理如图.下列关于该电池的说法正确的是( )| A. | 该电池若用隔膜可选用质子交换膜 | |
| B. | 放电时,LiCoO2极发生的电极反应为:LiCoO2-xe-═Li1-xCoO2+xLi+ | |
| C. | 石墨烯电池的优点是提高电池的储铿容量进而提高能量密度 | |
| D. | 废旧的该电池进行“放电处理”让Li+嵌入石墨烯中而有利于回收 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水放在棕色试剂瓶中,避光保存 | |
| B. | 液溴密封盛放在棕色瓶中,液面上放一层水 | |
| C. | 少量金属钠保存在四氯化碳中 | |
| D. | 水玻璃保存在带胶塞的玻璃试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 皂化反应的产物是高级脂肪酸和甘油 | |
| B. | 酯化反应和酯的水解反应均为取代反应 | |
| C. | 将苯与浓溴水混合可制取溴苯 | |
| D. | 新戊烷和2-甲基丁烷是同一种物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 的名称是2,4-二甲基戊烷,对二甲苯的结构简式是
的名称是2,4-二甲基戊烷,对二甲苯的结构简式是
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 阳离子 | Al3+、Ba2+ |
| 阴离子 | OHˉ、SO42ˉ、Clˉ |
| A. | 往甲和乙的混合溶液中加入过量的丁溶液一定会生成白色沉淀 | |
| B. | 丙和丁的水溶液混合后会生成白色沉淀 | |
| C. | 一定温度下,丙溶于水会使水的电离程度增大 | |
| D. | 一定温度下,甲溶于水会使水的电离程度减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
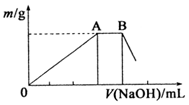 铝及其化合物在生产和生活等方面有广泛的应用.请回答下列问题:
铝及其化合物在生产和生活等方面有广泛的应用.请回答下列问题: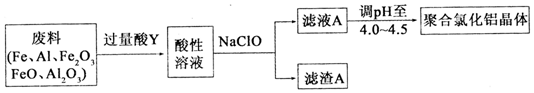
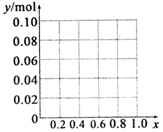
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:r(X)<r(Y)<r(Z)<r(W) | |
| B. | Y的简单气态氢化物的热稳定性比W的弱 | |
| C. | 由X、Y组成的物质与由Y、W组成的物质化合,可能发生氧化还原反应 | |
| D. | 常温下,Z的单质一定易溶于由X、Y、W三种元素组成的化合物的溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com