
有一处于平衡状态的可逆反应:X(s)+3Y(g)⇌2Z(g)(△H<0).为了使平衡向生成Z的方向移动,应选择的条件是( )
①高温 ②低温 ③高压 ④低压 ⑤加催化剂 ⑥分离出Z.
|
| A. | ①③⑤ | B. | ②③⑤ | C. | ②③⑥ | D. | ②④⑥ |
考点:
化学平衡的影响因素.
专题:
化学平衡专题.
分析:
①升高温度,平衡向吸热反应移动;
②降低温度,平衡向放热反应移动;
③压强增大,平衡向气体体积减小的方向移动;
④降低压强,平衡向气体体积增大的方向移动;
⑤加催化剂不会引起化学平衡的移动;
⑥分离出Z,即减小生成物的浓度,平衡正向移动.
解答:
解:反应X(s)+3Y(g)  2Z(g),△H<0,正反应是气体物质的量减小的放热反应,
2Z(g),△H<0,正反应是气体物质的量减小的放热反应,
①升高温度,平衡逆向移动,故①错误;
②降低温度,平衡向正反应移动,故②正确;
③压强增大,平衡向正反应移动,故③正确;
④降低压强,平衡向逆反应方向移动,故④错误;
⑤加催化剂缩短到达平衡的时间,不会引起化学平衡的移动,故⑤错误;
⑥分离出Z,即减小生成物的浓度,平衡正向移动,故⑥正确;
故选C.
点评:
本题考查化学平衡移动的影响因素等,难度中等,注意加入惰性气体对平衡的影响,恒温恒容平衡不移动,恒温恒压,体积增大,平衡向体积增大方向移动.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
把下列现象中硫酸所表现出来的性质填写在空白处
(1)把锌粒放入稀硫酸中时,有气体放出。
(2)盛有浓硫酸的烧杯敞口放置一段时间后,质量增加。
(3)用玻璃棒蘸浓硫酸滴在纸上时,纸变黑。
(4)木炭放入热的浓硫酸中时,有气体放出。
(5)常温下可以用铁或铝的容器贮存浓硫酸
(6)热的浓硫酸与铜片等金属反应
查看答案和解析>>
科目:高中化学 来源: 题型:
将amL NO、bmL NO2、xmL O2混合于同一试管中,将试管倒插入水中,待气体与水充分反应后,试管内的气体全部消失,则x对a、b的函数关系式x=f(a,b)为 ( )

查看答案和解析>>
科目:高中化学 来源: 题型:
今有如下三个热化学方程式:
H2(g)+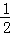 O2(g)═H2O(g)△H=a kJ•mol﹣1
O2(g)═H2O(g)△H=a kJ•mol﹣1
H2(g)+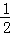 O2(g)═H2O(l)△H=b kJ•mol﹣1
O2(g)═H2O(l)△H=b kJ•mol﹣1
2H2(g)+O2(g)═2H2O(l)△H=c kJ•mol﹣1
关于它们的下列表述正确的是( )
|
| A. | 它们都是吸热反应 | B. | a、b和c均为正值 |
|
| C. | a=b | D. | 2b=c |
查看答案和解析>>
科目:高中化学 来源: 题型:
对下列过程中熵变的判断不正确的是( )
|
| A. | 溶解少量食盐于水中:△S>0 |
|
| B. | H2O(g)变成液态水:△S>0 |
|
| C. | 纯碳和氧气反应生成CO(g):△S>0 |
|
| D. | CaCO3(s)高温分解为CaO(s)和CO2(g):△S>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)原电池反应通常是放热反应,在理论上可设计成原电池的化学反应是 (填序号),理由是 该反应既 .
A.C(s)+H2O(g)═CO(g)+H2(g)△H>0
B.Ba(OH)2•8H2O(s)+2NH4Cl(s)═BaCl2(aq)+2NH3•H2O(l)+8H2O(l)△H>0
C.CaC2(s)+2H2O(l)═Ca(OH)2(s)+C2H2(g)△H<0
D.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H<0
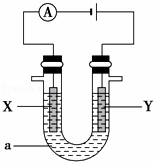
(2)电解原理在化学工业中有着广泛的应用.现将你设计的原电池通过导线与图中电解池相连,其中,a为电解液,X和Y是两块电极板,则:
①若X和Y均为惰性电极,a为饱和的NaCl溶液,则电解时,检验Y电极反应产物的方法是 .
②若X、Y分别为石墨和铁,a仍为饱和的NaCl溶液,则电解过程中生成的白色固体物质露置在空气中可观察到的现象为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)实验操作中,不慎将手指划破,这时可从急救箱中取FeCl3溶液止血,其原理是 .
(2)今有两瓶标签模糊不清,只知道分别盛有淀粉溶液和氯化钠溶液,试用2种方法对其鉴别.
① ;② .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质的性质和该性质的应用均正确的是
A.常温下浓硫酸能是铝发生钝化,可在常温下用铝制贮藏贮运浓硫酸
B.二氧化硅不与任何酸反应,可用石英制造耐酸容器
C.二氧化氯具有还原性,可用于自来水的杀菌消毒
D.铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com