
下列原子结构模型与科学家对应不正确的一项是:
A.阿伏加德罗的原子学说
B.汤姆生的“葡萄干面包式”原子结构模型
C.卢瑟福的带核原子结构模型
D.玻尔的核外电子在一定轨道上运动的观点
科目:高中化学 来源:2014-2015学年甘肃省高三11月月考化学试卷(解析版) 题型:填空题
(19分) A + B → X + Y + H2O(未配平,反应条件略去)是中学常见反应的化学方程式,请回答:
(1)若Y为黄绿色气体:
①当A、B的物质的量之比为1∶4且A为黑色固体时,该反应的离子方程式是 ;
②当A、B的物质的量之比为1∶6时,写出该反应的化学方程式,并用双线桥表示反应过程中的电子转移:__________________________________________。
③实验室处理尾气Y时常用NaOH而不用NaHSO3溶液,其原因是(用离子反应方程式表示)_____________________________________________________________。
(2)若A为单质,B为无色油状黏稠液体,当 A、B的物质的量之比为1∶2时,则A可能为______,检查其中刺激性气体产物X的方法是____________________。
(3)常温下A在B的浓溶液中会“钝化”,且A可溶于X溶液中,若A为金属单质,A和B以物质的量之比1∶4反应。
①过量的A和100mL2mol/L的B溶液充分反应后将溶液稀释至500mL后溶液中阴离子的物质的量浓度为_____________。
②含 a mol X的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量之比为1∶2时,则被还原的X是 mol。
(4)若A、B、X、Y均为化合物。向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色。则A与B按物质的量之比1:4反应后,溶液中溶质的化学式为 。
(5)若A、B、X、Y均为化合物。X为极易溶于水的气体,则盐A是_______盐,X极易溶于水的原因是:________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:选择题
下列各组物质互为同素异形体的是
A.12C和14C B.H2O和D2O C.O2和O3 D.淀粉和纤维素
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
下列溶液中,跟100mL 0.5mol/L CaCl2溶液所含的Cl-物质的量浓度相同的是
A.100mL 1mol/L MgCl2溶液 B.200mL 0.25mol/L AlCl3溶液
C.200ml 1mol/L NaCl溶液 D.200ml 0.5mol/L HCl溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高一上学期期中化学试卷(解析版) 题型:选择题
某元素Rn-核外有x个电子,该元素的某种原子质量数为A,则原子里的中子数为:
A.A-x-n B.A+x+n C.A-x+n D.A+x-n
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:填空题
(14分)2013年10月9日,2013年诺贝尔化学奖在瑞典揭晓,犹太裔美国理论化学家马丁·卡普拉斯、美国斯坦福大学生物物理学家迈克尔·莱维特和南加州大学化学家亚利耶·瓦谢尔因给复杂化学体系设计了多尺度模型而分享奖项。三位科学家的研究成果已经应用于废气净化及植物的光合作用的研究中,并可用于优化汽车催化剂、药物和太阳能电池的设计。
(1)汽车尾气净化的主要原理为:2NO(g) + 2CO(g) 2CO2(g)+ N2(g) △H<0同一条件下该反应正反应的平衡常数为K1,逆反应的表达式平衡常数为K2,K1与K2的关系式为 。
2CO2(g)+ N2(g) △H<0同一条件下该反应正反应的平衡常数为K1,逆反应的表达式平衡常数为K2,K1与K2的关系式为 。
(2)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号)。

(3)在体积为10L的密闭容器中,加入一定量的CO2和H2,在900℃时发生吸热反应并记录前5min各物质的浓度,第6min改变了条件。各物质的浓度变化如下表;
时间/min | CO2(mol·L-1) | H2(mol·L-1) | CO(mol·L-1) | H2O(mol·L-1) |
0 | 0.2000 | 0.3000 | 0 | 0 |
2 | 0.1740 | 0.2740 | 0.0260 | 0.0260 |
5 | 0.0727 | 0.1727 | 0.1273 | 0.1273 |
6 | 0.0350 | 0.1350 | 0.1650 |
①前2min,用CO表示的该化学反应的速率为 ;
②第5—6min,平衡移动的可能原因是 ;
(4)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1
2NO2(g) N2O4(g) △H=-56.9 kJ·mol-1
N2O4(g) △H=-56.9 kJ·mol-1
H2O(g) = H2O(l) △H = -44.0 kJ·mol-1
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式: 。
在一定条件下,可以用NH3处理NOx。已知NO与NH3发生反应生成N2和H2O,现有NO和NH3的混合物1mol,充分反应后得到的还原产物比氧化产物多1.4 g,则原反应混合物中NO的物质的量可能是 mol
(6)在一定条件下,也可以用H2处理CO合成甲醇和二甲醚(CH3OCH3)及许多烃类物质。当两者以物质的量1:1催化反应,其原子利用率达100%,合成的物质可能是 。
a.汽油 b.甲醇 c.甲醛 d.乙酸
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:选择题
苹果iphone5正在我国热卖,其电池为锂电池。构造如图所示,电池内部“→”表示放电时Li+的迁移方向,电池总反应可表示为:Li1-xCoO2+LixC6 LiCoO2+6C,下列说法错误的是
LiCoO2+6C,下列说法错误的是
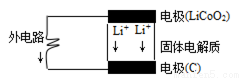
A.该电池的负极为LiCoO2
B.电池中的固体电解质可以是氯化钠、干冰等
C.充电时的阴极反应:Li1-xCoO2+xLi++xe-=LiCoO2
D.外电路上的“→”表示放电时的电子流向
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:选择题
下列有关说法中正确的是
A.合成氨中采用及时分离氨气提高反应物的转化率
B.升高温度能使吸热反应速率加快,使放热反应速率减慢
C.增大压强,化学反应速率一定加快,平衡一定发生移动
D.工业上电解饱和食盐水的阴极反应:2Cl--2e-===Cl2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津市宝坻区四校高二11月联考化学试卷(解析版) 题型:选择题
在氨水中存在下列电离平衡:NH3·H2O NH4++OH-,下列情况能引起电离平衡向正向移动的有
NH4++OH-,下列情况能引起电离平衡向正向移动的有
①加NH4Cl固体 ②加NaOH溶液 ③加HCl ④加CH3COOH溶液 ⑤加水 ⑥加压
A.①③⑤ B.①④⑥ C.③④⑤ D.①②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com