
已知常温下KClO3与HCl(浓)反应放出氯气,现按下图进行卤素的性质实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是( )
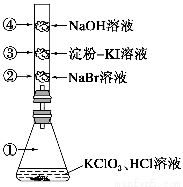
①②③④
A黄绿色橙色蓝色白色
B无色橙色紫色白色
C黄绿色橙色蓝色无色
D黄绿色无色紫色白色
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014年高一化学人教版必修二 1-3-1离子键练习卷(解析版) 题型:填空题
离子化合物AB2的阴、阳离子的电子层结构相同,1 mol AB2中含54 mol电子,且有下列反应:
①H2+B2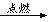 C
C
②B2+X→Y+AB2+H2O
③Y+C→AB2+Z,Z有漂白作用。
根据上述条件回答下列问题:
(1)写出下列物质的化学式:AB2__________,X________,Y________,Z________。
(2)用电子式表示AB2的形成过程:_____________________________________________。
(3)写出反应②的化学方程式:______________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-2-1原子核外电子排布练习卷(解析版) 题型:选择题
A、B为两短周期元素,A元素原子的L层比B元素原子的L层少3个电子,B原子核外电子总数比A原子核外电子总数多5,则A和B形成的化合物的化学式为( )
A.A2B3 B.BA2 C.AB4 D.B3A2
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-1-3原子结构 核素练习卷(解析版) 题型:选择题
若NA为阿伏加德罗常数,已知某元素的阴离子Rn-的原子核中,中子数为A-x+n,其中A为原子的质量数,则m g Rn-中电子总数为( )
A.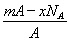 B.
B.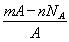
C.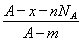 D.
D.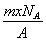
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-1-2元素性质练习卷(解析版) 题型:填空题
甲元素的原子序数是11,乙元素原子核外有两个电子层,最外电子层上有6个电子;丙是元素周期表第ⅠA族中金属性最弱的碱金属元素。由此推断:
(1)甲元素在周期表中位于第________周期;乙元素在周期表中位于第________族;丙元素的名称为________。
(2)甲的单质与水反应的离子方程式为__________________________。乙单质与丙单质反应的化学方程式为______________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-1-2元素性质练习卷(解析版) 题型:选择题
已知钡的活动性介于钠和钾之间,下列叙述正确的是( )
A.钡与水反应不如钠与水反应剧烈
B.钡可以从KCl溶液中置换出钾
C.氧化性:K+>Ba2+>Na+
D.碱性:KOH>Ba(OH)2>NaOH
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修二 1-1-1元素周期表练习卷(解析版) 题型:填空题
A、B两元素,A的原子序数为x,A、B所在周期元素的种类分别为m和n,若A、B同在第ⅠA族,当B在A的上周期时,B的原子序数为________,当B在A的下周期时,B的原子序数为________;若A、B同在第ⅦA族,当B在A的上周期时,B的原子序数为________,当B在A的下周期时,B的原子序数为________。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修2 模块水平检测2练习卷(解析版) 题型:实验题
酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、黏合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:
CH3COOH+C2H5OH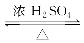 CH3COOC2H5+H2O
CH3COOC2H5+H2O
请根据要求回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有:__________、__________等。
(2)若用如图所示的装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为________、________等。
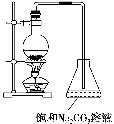
(3)此反应以浓硫酸为催化剂,可能会造成__________、__________等问题。
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)。
同一反应时间 |
| 同一反应温度 | ||||
反应温度/℃ | 转化率(%) | 选择性(%)* |
| 反应时间/h | 转化率(%) | 选择性(%)* |
40 | 77.8 | 100 |
| 2 | 80.2 | 100 |
60 | 92.3 | 100 |
| 3 | 87.8 | 100 |
80 | 92.6 | 100 |
| 4 | 92.3 | 100 |
120 | 94.5 | 98.7 |
| 6 | 93.0 | 100 |
①根据表中数据,下列________(填字母)为该反应的最佳条件。
A.120 ℃,4 h B.80 ℃,2 h
C.60 ℃,4 h D.40 ℃,3 h
②当反应温度达到120 ℃时,反应选择性降低的原因可能为________。
查看答案和解析>>
科目:高中化学 来源:2014年高一化学人教版必修2 期中测试练习卷(解析版) 题型:选择题
下列说法正确的是
A.不管什么反应使用催化剂,都可以加快反应速率
B.可逆反应A(g) B(g)+C(g),增大压强正反应速率减小,逆反应速率增大
B(g)+C(g),增大压强正反应速率减小,逆反应速率增大
C.对达到平衡的一个放热的可逆反应,若降低温度正反应速率减小,逆反应速率增大
D.参加反应物质的性质是决定化学反应速率的主要因素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com