
| A. | 核外电子排布完全相同的两种微粒,其化学性质一定相同 | |
| B. | 具有固定熔点或沸点的物质一定是纯净物 | |
| C. | 一种离子和一种分子的质子数和电子数不可能同时相等 | |
| D. | 由分子构成的物质中一定含有共价键 |
分析 A、核外电子排布完全相同的两种微粒不一定属于同种元素,化学性质不一定相同;
B、混合物没有固定熔点,纯净物有固定熔点;
C、离子带电荷,质子数一定不等于电子数;分子不带电,质子数等于电子数;
D、由分子是单原子分子,则组成的物质中不一定含有共价键;
解答 解:A、核外电子排布完全相同的两种微粒不一定属于同种元素,化学性质不一定相同,如K+与Cl-核外电子排布相同,但是二者化学性质不同,故A错误;
B、只有纯净物有固定熔沸点,故B正确;
C、离子带电荷,质子数一定不等于电子数;分子不带电,质子数等于电子数,当离子和分子的质子数相同时,他们的电子数一定不相同,故C正确;
D、由分子组成的物质中不一定含有共价键,如稀有气体,故D错误;
故选:BC.
点评 本题为综合题,考查了原子结构、物质的熔沸点、电解质的电离,综合性强,题目难度不大,侧重考查学生对基础知识的掌握.


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:解答题
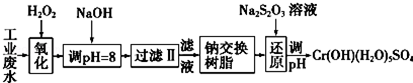
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
| pH | 3.7 | 9.6 | 11.1 | 8 | 9(>9溶解) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据酸分子中含有氢原子的个数,将酸分为一元酸、二元酸等 | |
| B. | 根据化合物在溶液中电离出的离子的类别,将化合物分为酸、碱、盐 | |
| C. | 根据化学反应中有无单质参加或生成,将化学反应分为氧化还原反应和非氧化还原反应 | |
| D. | 四种基本反应类型未能包括所有的化学反应,酸性氧化物、碱性氧化物、两性氧化物的分类包括了所有的氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4句 | B. | 5句 | C. | 6句 | D. | 7句 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在地壳中,B元素的含量位于第二位 | |
| B. | C元素的单质熔点低,在空气中加热时先熔化后燃烧 | |
| C. | A、B、D三种元素形成的化合物一定是强酸 | |
| D. | B元素与A元素形成的物质一定是纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂、纤维素、淀粉都是高分子化合物 | |
| B. | 煤的干馏、蛋白质的变性和纳米银粒子的聚焦都是化学变化 | |
| C. | 酒精、甲苯、四氯化碳都能萃取碘水中的碘单质 | |
| D. | 乙烯、乙炔都可作为合成聚合物的单体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
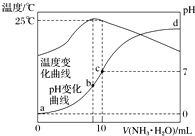 在某温度时,将n mol•L-1氨水滴入10mL 1.0mol•L-1盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示.下列有关说法正确的是( )
在某温度时,将n mol•L-1氨水滴入10mL 1.0mol•L-1盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示.下列有关说法正确的是( )| A. | n=1.0 | |
| B. | 水的电离程度:b>c>a>d | |
| C. | c点:c(NH${\;}_{4}^{+}$)=c(Cl-)=1.0 mol•L-1 | |
| D. | 25℃时,NH4Cl的水解常数(Kh)计算式为=$\frac{(\frac{n}{2}-0.5)×1{0}^{-7}}{0.5}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 和C3H8O3(甘油)以一定比例混合,测定混合物中含碳51.3%,那么氢元素的质量分数是8.7%(取2位有效数字,下同);氧元素的质量分数是40%.
和C3H8O3(甘油)以一定比例混合,测定混合物中含碳51.3%,那么氢元素的质量分数是8.7%(取2位有效数字,下同);氧元素的质量分数是40%.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com