
分析 设反应之前甲烷的物质的量为1mol,消耗的甲烷为0.4mol,根据碳原子守恒,反应后混合气体总物质的量为(1-0.4)mol+$\frac{0.4mol}{2}$=0.8mol,设得到C2H4为xmol,根据碳原子守恒,可知成C2H6为(0.2-x)mol,再根据混合气体的密度=$\frac{混合气体总质量}{混合气体总体积}$列方程计算解答.
解答 解:设反应之前甲烷的物质的量为1mol,消耗的甲烷为0.4mol,剩余甲烷为1mol-0.4mol=0.6mol,
根据碳原子守恒,反应后混合气体总物质的量为(1-0.4)mol+$\frac{0.4mol}{2}$=0.8mol,则反应后混合气体总体积为0.8mol×22.4L/mol,
设得到C2H4为xmol,根据碳原子守恒,可知成C2H6为(0.2-x)mol,则:$\frac{0.6×16+28x+30×(0.2-x)}{0.8mol×22.4L/mol}$=0.85,解得x=0.184mol,则混合气体中乙烯的体积分数为$\frac{0.184mol}{0.8mol}$×100%=23%,
答:混合气体中乙烯的体积分数为23%.
点评 本题考查混合物计算,涉及物质的量有关计算,关键是碳原子守恒应用,侧重考查学生分析计算的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 用食醋除去热水瓶中的水垢 | |
| B. | 用米汤检验加碘盐中的碘酸钾(KIO3) | |
| C. | 向Al2(SO4)3溶液中加过量NaOH溶液,制Al(OH)3 | |
| D. | 向稀H2SO4催化水解后的麦芽糖溶液中直接加入新制Cu (OH)2悬浊液,检验水解产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
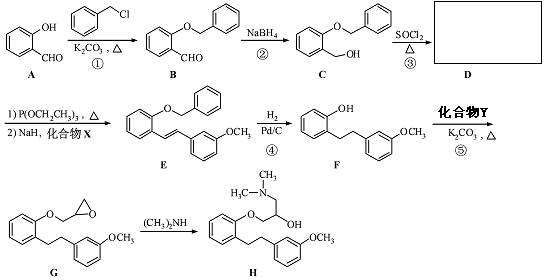

 .
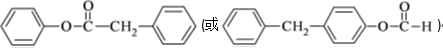
.
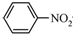 $→_{Pd/C}^{H_{2}}$
$→_{Pd/C}^{H_{2}}$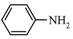 .化合物
.化合物  是合成抗癌药物美法
是合成抗癌药物美法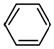 和
和 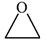 为原料制备该化合物的合成路线流程图(无机试剂任
为原料制备该化合物的合成路线流程图(无机试剂任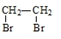
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Ca(ClO)2溶液中通入CO2至过量 | |
| B. | 向Na2SiO3溶液中滴加盐酸溶液至过量 | |
| C. | 向氢氧化铁胶体中滴加稀硫酸至过量 | |
| D. | 向Na[Al(OH)4]溶液中滴加盐酸至过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuO | B. | MnO2 | C. | Fe2O3 | D. | Fe3O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①②④ | C. | ①②③ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y形成的原子个数比为1:1的漂白性物质中既有极性共价键又有非极性共价键 | |
| B. | 上述四种元素的原子半径大小顺序为r(Z)>r(Y)>r(X)>r(W) | |
| C. | W与X形成的化合物的熔沸点高于W与Z形成的化合物的熔沸点 | |
| D. | X、Y、Z三种元素形成的化合物,其水溶液一定呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的分子式为C5H10O2 | |
| B. | X可能的结构有两种 | |
| C. | Y中含有的官能团有羧基和碳碳双键 | |
| D. | X与Y相对分子质量相差14,则X与Y互为同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com