
| A. | 2:1 | B. | 1:2 | C. | 2:3 | D. | 3:2 |
分析 气体密度等于气体质量除以容器的容积.容积固定,保证气体质量最小即可.硫化氢和二氧化硫反应,得到硫和水.温度为常温,则硫为固态;水为液态.考虑气体密度与他们无关.则需要使两者恰好反应.
解答 解:气体密度等于气体质量除以容器的容积.容积固定,容器内气体密度最小时,保证气体质量最小即可.反应的方程式为2H2S+SO2═3S+2H20,温度为常温,则硫为固态;水为液态,气体密度与他们无关,当a:b=2:1时,几乎无气体剩余,此时容器内气体的质量最小,容器内气体密度最小,
故选A.
点评 本题考查有关范围讨论题的计算,题目难度不大,本题注意气体密度等于气体质量除以容器的容积.容积固定,保证气体质量最小,密度最小.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:选择题
| A. | IO3- | B. | Fe3+ | C. | SO2 | D. | MnO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | d元素的非金属性最强 | |
| B. | 它们均存在两种或两种以上的氧化物 | |
| C. | a的最高价氧化物对应的水化物是强碱 | |
| D. | b、c、d的气态氢化物的稳定性:b>c>d |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
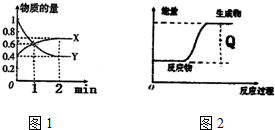
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知H+(aq)+OH-(aq)═H20(l)△H=-57.3kJ•mol-1,则H2SO4和Ba(OH)2反应的反应热△H=-2×(-57.3)kJ•mol-1 | |
| B. | 由4P(s,红磷)═P4(s,白磷)△H=+139.2kJ/mol可知,红磷比白磷稳定 | |
| C. | H2(g)的燃烧热是285.8kJ•mol-1,则2H2O═2H2(g)+O2(g)△H=+571.6KJ•mol-1 | |
| D. | 恒温恒容时,将2molA和1molB投入密闭容器中,发生反应:2A(g)+B(g)?2C(g).充分反应后测得放出的热量为QkJ,则该反应的△H=-QkJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 缩小体积使压强增大 | B. | 体积不变充入N2使气体压强增大 | ||
| C. | 体积不变充入He使气体压强增大 | D. | 压强不变,充入He使体积增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 | B. | 3 | C. | 1 | D. | 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com