
| A. | 2项 | B. | 3项 | C. | 4项 | D. | 5项 |
分析 ①78gNa2S的物质的量为1mol,1mol硫化钠中含有2mol钠离子、1mol硫离子,总共含有3mol离子;
②二氧化硫与氧气的反应为可逆反应,反应物不可能完全转化成生成物;
③Fe和稀硝酸反应方程式为:3Fe+8HNO3=3Fe(NO3)3+2NO↑+4H2O或Fe+4HNO3=Fe(NO3)3+NO↑+2H2O,根据方程式计算被还原的硝酸的物质的量,然后根据质量守恒计算出所得溶液中硝酸根离子的物质的量;
④标准状况下,氟化氢的状态不是气态;
⑤12.4g白磷中含有共用电子对数0.6NA,
解答 解:①78gNa2S的物质的量为:$\frac{78g}{78g/mol}$=1mol,1mol硫化钠中含有2mol钠离子、1mol硫离子,总共含有3mol离子,含有离子总数为3NA,故①错误;
②1molO2和2molSO2在一定条件下密闭容器中充分反应,反应消耗氧气的物质的量小于1mol,则转移电子的物质的量小于4mol,转移电子数小于4NA,故②错误;
③Fe和稀硝酸反应方程式为:3Fe+8HNO3=3Fe(NO3)3+2NO↑+4H2O或Fe+4HNO3=Fe(NO3)3+NO↑+2H2O,硝酸的物质的量是1mol,由方程式可知被还原硝酸的物质的量是:1mol×$\frac{1}{4}$=0.25mol,则所得溶液中硝酸根离子的物质的量为1mol-0.25mol=0.75mol,则所得溶液NO3-有0.75NA,故③正确;
④标准状况下,HF不是气态,不能使用标准状况下的气体摩尔体积计算33.6L氟化氢的物质的量,故④错误;
⑤白磷的分子式为P4,12.4g白磷的物质的量为:$\frac{12.4g}{124g/mol}$=0.1mol,1个P4分子含有6条共价键,故0.1molP4含有磷磷键数为0.6NA,故⑤正确;
根据分析可知,正确的有2项,
故选A.
点评 本题考查了物质的量的计算,题目难度中等,明确标准状况下气体摩尔体积的使用条件为解答关键,注意掌握物质的量与摩尔质量、阿伏伽德罗常数等之间的关系,试题培养了学生的化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | 氢氧燃料电池可将热能直接转变为电能 | |
| B. | 燃料电池的能量转化率可达100% | |
| C. | 燃料电池与干电池或蓄电池的主要差别在于反应物不是储存在电池内部,而是由外设装备提供燃料和氧化剂 | |
| D. | 氢氧燃料电池工作时氢气在正极被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油化工水平的标志是乙烯产量 | |
| B. | 天然气的主要成分是丙烷 | |
| C. | 糖尿病患者不可以用新制备的氢氧化铜检验 | |
| D. | 乙醇在铜丝的催化氧化下可生成无色无刺激性的乙醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应开始时的速率:甲<乙 | |
| B. | 反应开始时,酸的物质的量浓度:甲>乙 | |
| C. | 反应开始时,酸的物质的量浓度:甲<乙 | |
| D. | 反应所需时间:甲<乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲>乙>丙>丁 | B. | 乙>甲>丙>丁 | C. | 丁>丙>乙>甲 | D. | 乙>甲>丁>丙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Na>Mg>Al | B. | 碱性强弱:NaOH>Mg(OH)2>Ca(OH)2 | ||
| C. | 热稳定性:HCl>PH3>AsH3 | D. | 酸性强弱:H4SiO4<H3PO4<HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2O3和稀盐酸 | B. | Al2O3和水 | C. | Al2(SO4)3和NaOH | D. | AlCl3和氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
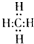 ,分子里各原子的空间分布呈正四面体结构.相对分子质量为212的烷烃的分子式为C15H32.分子式为C8Hm的烯烃,m值等于16;分子式为CnH8的苯的同系物,n值等于7.
,分子里各原子的空间分布呈正四面体结构.相对分子质量为212的烷烃的分子式为C15H32.分子式为C8Hm的烯烃,m值等于16;分子式为CnH8的苯的同系物,n值等于7.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com