
| A. | 将等物质的量的CH4和Cl2在光照下反应生成纯净的CH3Cl | |
| B. | 将苯与浓硝酸和浓硫酸混合水浴加热制取硝基苯 | |
| C. | 用新制Cu(OH)2悬浊液鉴别葡萄糖和蔗糖 | |
| D. | 用浓硝酸鉴别淀粉溶液和鸡蛋白溶液 |
分析 A.将等物质的量的CH4和Cl2在光照下反应生成多种氯代烃,同时生成HCl;
B.在浓硫酸作催化剂、加热条件下,苯和浓硝酸发生取代反应生成硝基苯;
C.新制氢氧化铜悬浊液和醛基发生氧化反应生成砖红色沉淀;
D.蛋白质遇浓硝酸发生颜色反应.
解答 解:A.将等物质的量的CH4和Cl2在光照下反应生成多种氯代烃,同时生成HCl,所以不能得到纯净的一氯甲烷,故A错误;
B.在浓硫酸作催化剂、加热条件下,苯和浓硝酸发生取代反应生成硝基苯,该反应温度较低,需要水浴加热,故B正确;
C.新制氢氧化铜悬浊液和醛基发生氧化反应生成砖红色沉淀,葡萄糖中含有醛基、蔗糖中不含醛基,所以可以用新制氢氧化铜悬浊液鉴别葡萄糖和蔗糖,故C正确;
D.蛋白质遇浓硝酸发生颜色反应,淀粉和浓硝酸不反应,所以可以用浓硝酸鉴别淀粉溶液和蛋白质溶液,故D正确;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及物质鉴别、物质制备等知识点,明确反应原理及物质性质是解本题关键,会从物质性质及实验操作方面进行评价,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | NH3的百分含量不变 | B. | N2的体积分数增大 | ||
| C. | N2的转化率增大 | D. | NH3的百分含量增小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
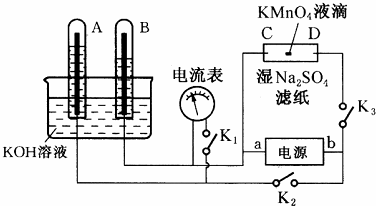
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 埃博拉病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的 | |
| B. | 气象环境报告中新增的“PM2.5”是对一种新分子的描述 | |
| C. | 用浸泡过高锰酸钾溶液的硅藻土保鲜水果 | |
| D. | 施肥时,草木灰(有效成分为K2CO3)与NH4Cl混合使用效果更好 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,化合物  的名称为2,4-二乙基-6-丙基辛烷 的名称为2,4-二乙基-6-丙基辛烷 | |
| B. | 月桂烯 (  )所有碳原子一定在同一平面上 )所有碳原子一定在同一平面上 | |
| C. | 取卤代烃,加入氢氧化钠的乙醇溶液加热一段时间后冷却,再加入稀硝酸酸化的硝酸银溶液,一定会产生沉淀,并根据沉淀颜色判断卤代烃中卤原子的种类 | |
| D. | 通常条件下,1mol的  分别与H2 和浓溴水完全反应时,消耗的H2和 分别与H2 和浓溴水完全反应时,消耗的H2和Br2的物质的量分别是 4mol、3mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素编号 | 元素性质或原子结构 |
| T | M层上的电子数是原子核外电子层数的2倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物的水溶液呈碱性, |
| Z | 元素最高正价是+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
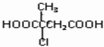 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:(RCH3CH=CH2+HCl$\stackrel{催化剂}{→}$RCH3CHClCH3)
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:(RCH3CH=CH2+HCl$\stackrel{催化剂}{→}$RCH3CHClCH3)  .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

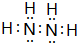 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com