
| A. | 单质的颜色逐渐变浅 | |
| B. | 气态氢化物的稳定性逐渐增强 | |
| C. | 从F→I,原子核对最外层电子的吸引能力依次减弱,原子的得电子能力依次减弱 | |
| D. | 单质的熔沸点逐渐降低 |
分析 卤族元素从上到下,随着原子序数的增大,原子半径逐渐增大,元素的非金属性逐渐减弱,对应单质的氧化性逐渐减弱,气态氢化物的稳定性减弱,单质的颜色逐渐加深,原子的得电子能力依次减弱,据此回答.
解答 解:A、卤族元素从上到下,单质的颜色逐渐加深,故A错误;
B、卤族元素从上到下,元素的非金属性逐渐减弱,气态氢化物的稳定性减弱,故B错误;
C、从F→I,原子半径逐渐增加,原子核对最外层电子的吸引能力依次减弱,原子的得电子能力依次减弱,故C正确;
D、卤素单质都属于分子晶体,从上到下单质的相对分子质量逐渐增大,分子间作用力逐渐增强,单质的沸点升高,故D错误;
故选C.
点评 本题考查同主族元素对应单质、化合物的性质的递变,题目难度不大,注意元素周期律的递变规律,注意把握卤素原子的结构及其性质.


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
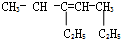 3-乙基-3-庚烯.
3-乙基-3-庚烯.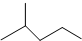 表示的分子式C6H14;一氯代物有5种.
表示的分子式C6H14;一氯代物有5种.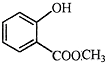 中含有的官能团的名称为羟基、酯基.
中含有的官能团的名称为羟基、酯基.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 图中A、B、C、D是同周期或同主族的相邻元素:
图中A、B、C、D是同周期或同主族的相邻元素:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铷与水反应的现象跟钠相似 | |
| B. | 硝酸铷易溶于水 | |
| C. | 在钠、钾、铷三种单质中,铷的熔点最高 | |
| D. | 氢氧化铷是弱碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | ||
| 2 | ① | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
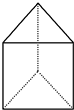 人们对苯及芳香烃的认识有一个不断深化的过程,回答下列问题.
人们对苯及芳香烃的认识有一个不断深化的过程,回答下列问题.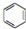 (Ⅱ)
(Ⅱ)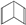
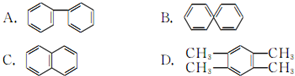
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 丙醛 | B. | 丙烯醛 | C. | 甲醛 | D. | 丁烯醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | K+ | Na+ | NH4+ | SO42- | NO3-[] | Cl- |
| 浓度/mol?L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5[] | 3×10-5 | 2×10-5 |
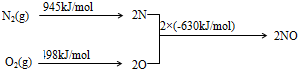
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com