
离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强弱,摩尔电导率越大,离子在溶液中的导电能力越强。已知Ca2+、OH-、HC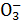 的摩尔电导率分别为0.60、1.98、0.45,据此可判断,往饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是 ( )
的摩尔电导率分别为0.60、1.98、0.45,据此可判断,往饱和的澄清石灰水中通入过量的CO2,溶液导电能力随CO2通入量的变化趋势正确的是 ( )
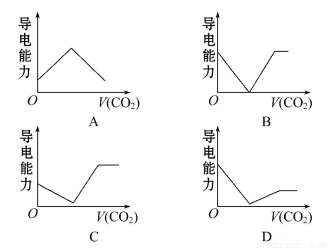
D
【解析】
试题分析:向澄清石灰水中通入CO2,当CO2适量时Ca(OH)2+CO2====CaCO3↓+H2O,其反应的离子方程式为Ca2++2OH-+CO2====CaCO3↓+H2O,当CO2过量时CaCO3+CO2+H2O====Ca(HCO3)2,其反应的离子方程式为CaCO3+CO2+H2O====Ca2++2HC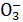 。所以向澄清石灰水中通入过量的CO2,先生成碳酸钙沉淀,钙离子、氢氧根离子浓度减小,溶液导电能力减弱,后沉淀溶解生成碳酸氢钙溶液,钙离子、碳酸氢根离子的浓度增大,钙离子的浓度与原来相等,碳酸氢根离子的浓度与原来氢氧根离子浓度相等,但OH-的摩尔电导率大于HC
。所以向澄清石灰水中通入过量的CO2,先生成碳酸钙沉淀,钙离子、氢氧根离子浓度减小,溶液导电能力减弱,后沉淀溶解生成碳酸氢钙溶液,钙离子、碳酸氢根离子的浓度增大,钙离子的浓度与原来相等,碳酸氢根离子的浓度与原来氢氧根离子浓度相等,但OH-的摩尔电导率大于HC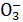 的摩尔电导率,所以最后溶液的导电性小于原来的导电性,最后CaCO3全部溶解后,溶液中离子的浓度不再发生变化,即导电能力不再发生变化。
的摩尔电导率,所以最后溶液的导电性小于原来的导电性,最后CaCO3全部溶解后,溶液中离子的浓度不再发生变化,即导电能力不再发生变化。
考点:离子反应


科目:高中化学 来源:2014-2015河北保定某重点中学同步课时作业(必修1苏教版)1.1.4分散系 题型:选择题
我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3×10-9m)恢复了磁性。“钴酞菁”的分子结构和性质与人体内的血红素及植物体内的叶绿素非常相似。下列说法不正确的是 ( )
A.“钴酞菁”分子所形成的分散系具有丁达尔效应
B.“钴酞菁”分子既能透过滤纸,也能透过半透膜
C.此项工作可以用来改变分子的某些物理性质
D.此工作可以广泛应用于光电器件、生物技术等方面
查看答案和解析>>
科目:高中化学 来源:2014-2015河北保定某重点中学同步作业(必修1苏教版)4.2.1氮的氧化物 题型:选择题
已知某氮的氧化物中氧元素的质量分数为0.696,则其化学式是( )
A.NO B.NO2 C.N2O4 D.N2O3
查看答案和解析>>
科目:高中化学 来源:2014-2015河北保定某重点中学同步作业(必修1苏教版)3.1.2铝的化合物 题型:填空题
下图所示是从铝土矿(主要成分是Al2O3,含Fe2O3、SiO2等杂质)中提取氧化铝的工艺流程之一。
已知:SiO2能和氢氧化钠反应,不和盐酸反应。
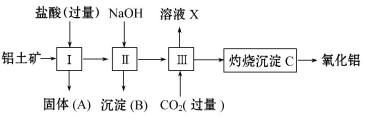
回答下列问题:
(1)用盐酸溶解铝土矿后,所得溶液中的阳离子有 。
(2)固体A的主要成分是 。
(3)进行操作Ⅱ时,为了达到分离要求,加入的NaOH应该 。
(4)进行操作Ⅲ时,一般通入过量CO2,其反应的化学方程式是
。
(5)溶液X和盐酸反应的离子方程式为
。
查看答案和解析>>
科目:高中化学 来源:2014-2015河北保定某重点中学同步作业(必修1苏教版)3.1.2铝的化合物 题型:选择题
用来除去溶液中Al3+效果最好的离子或物质是 ( )
A.Cl- B.OH- C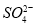 D.氨水
D.氨水
查看答案和解析>>
科目:高中化学 来源:2014-2015河北保定某重点中学同步作业(必修1苏教版)2.2.3离子反应 题型:填空题
某化合物的化学式为(NH4)2Fe(SO4)2,它在水溶液里电离时生成两种阳离子和一种酸根离子。
(1)写出(NH4)2Fe(SO4)2的电离方程式 。
(2)该化合物中氮元素与铁元素的质量比为 。
(3)若向该化合物的水溶液中通入氯气,一种离子很容易被氧化,该离子将变成(用离子符号表示) 。
(4)若向该溶液中加入过量的氨水,只能发生一个离子反应,则该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015河北保定某重点中学同步作业(必修1苏教版)2.2.3离子反应 题型:选择题
BaCO3与稀硝酸反应,正确的离子方程式是 ( )
A.Ba2++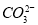 +2H++2N
+2H++2N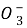 ====Ba(NO3)2+H2O+CO2↑
====Ba(NO3)2+H2O+CO2↑
B.BaCO3+2H++2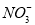 ===Ba(NO3)2+H2O+CO2↑
===Ba(NO3)2+H2O+CO2↑
C.BaCO3+2H+====Ba2++H2O+CO2↑
D.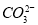 +2H+====H2O+CO2↑
+2H+====H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015河北保定某重点中学同步作业(必修1苏教版)2.1氧化还原反应 题型:选择题
下列反应(条件均省略)中,反应物中的各种元素都参加了氧化还原反应的是 ( )
A.2KNO3+S+3C====K2S+N2↑+3CO2↑
B.2KMnO4====K2MnO4+MnO2+O2↑
C.4HNO3====2H2O+4NO2↑+O2↑
D.HgS+O2====Hg+SO2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年黑龙江省高二上期开学考试化学试卷(解析版) 题型:实验题
(12分)某研究小组为了探究“铁与水蒸气”的反应的产物,进行了下列实验:用如图所示实验装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”(石棉绒高温下不与水和铁反应).

(1)如何检查该装置的气密性:
(2)写出铁与水蒸气反应的化学方程式
(3)验证固体产物中铁元素的价态
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹;1mol/L CuSO4、3mol/L H2SO4、3mol/L HNO3、30%H2O2、0.01mol/L KMnO4、20%KSCN、蒸馏水。
| 实验步骤 | 预期现象与结论 |
步骤1 | 取反应后干燥的固体ag于试管中,加入足量的1mol/L CuSO4溶液,充分振荡,经固液分离、洗涤后,再向固体中滴加足量的 ,振荡溶解,过滤后将滤液配成250mL溶液,待用。 |
|
步骤2 | 取少量步骤1中滤液于试管中,
|
|
步骤3 | 取少量步骤1中滤液于试管中, |
|
步骤1中加入足量1mol/L CuSO4溶液的作用是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com