
،¾جâؤ؟،؟دآ±يتاضـئع±يضذµؤز»²؟·ض£¬¸ù¾فA£Iشعضـئع±يضذµؤخ»ضأ£¬µع(1)~ (4)ذ،جâسأشھثط·û؛إ»ٍ»¯ر§ت½»ط´ً£¬£¨5£©،«£¨8£©ذ،جâ°´جâؤ؟زھاَ»ط´ً،£
×ه | I A | ¢ٍ A | ¢َ A | ¢ô A | ¢ُ A | ¢ِ A | ¢÷ A | O |
1 | A | |||||||
2 | D | E | G | I | ||||
3 | B | C | F | H |
(1)±يضذشھثط£¬»¯ر§ذشضت×î²»»îئأµؤتا £¬ض»سذ¸؛¼غ¶ّخقص¼غµؤتا £¬رُ»¯ذش×îا؟µؤµ¥ضتتا £¬»¹شذش×îا؟µؤµ¥ضتتا ،£
(2)×î¸ك¼غرُ»¯خïµؤث®»¯خï¼îذش×îا؟µؤتا £¬ثلذش×îا؟µؤتا £¬³تء½ذشµؤتا ،£
(3)A·ض±ًسëD،¢E،¢F،¢G،¢Hذخ³ةµؤ»¯؛دخïضذ£¬×îخب¶¨µؤ £¬
(4)شعB،¢C،¢E،¢F،¢G،¢Hضذ£¬ش×س°ë¾¶×î´َµؤتا £¬
£¨5£©A؛حD×é³ة»¯؛دخïµؤµç×ست½ £¬
£¨6£©A؛حE×é³ة»¯؛دخïµؤ»¯ر§ت½ £¬
£¨7£©سأµç×ست½±يت¾B؛حH×é³ة»¯؛دخïµؤذخ³ة¹³ج £¬
£¨8£©Bµؤ×î¸ك¼غرُ»¯خïµؤث®»¯خï؛حCµؤ×î¸ك¼غرُ»¯خïد໥·´س¦µؤہë×س·½³جت½
،£
،¾´ً°¸،؟£¨15·ض£©£¨1£©Ne،¢F،¢F2،¢Na £¨أ؟؟ص1·ض£¬¹²4·ض£©
£¨2£©NaOH،¢HClO4،¢Al(OH)3 £¨أ؟؟ص1·ض£¬¹²3·ض£©
£¨3£©HF £¨1·ض£© £¨4£©Na £¨1·ض£© £¨5£©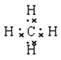 ،¢£¨6£©NH3،¢
،¢£¨6£©NH3،¢
£¨7£©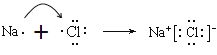 £¨¸÷2·ض£©
£¨¸÷2·ض£©
£¨8£©Al£¨OH£©3 + OH،ھ£½ AlO2،ھ + 2H2O £¨2·ض£©
،¾½âخِ،؟تشجâ£؛¸ù¾فA،«Iت®ضضشھثطشعضـئع±يضذµؤخ»ضأ؟ةضھ£¬ثüأا·ض±ًتاH،¢Na،¢Al،¢C،¢N،¢P،¢F،¢Ne،£¸ù¾فشھثطضـئعآة؟ةضھ£؛
£¨1£©»¯ر§ذشضت×î²»»îئأµؤتاNe،£ض»سذ¸؛¼غ¶ّخقص¼غµؤتاF£¬رُ»¯ذش×îا؟µؤµ¥ضتتاF2£¬»¹شذش×îا؟µؤµ¥ضتتاNa،£
£¨2£©½ًتôذش»ٍ·ا½ًتôذشش½ا؟£¬×î¸ك¼غرُ»¯خïµؤث®»¯خïµؤ¼îذش»ٍثلذشش½ا؟£¬شٍ×î¸ك¼غرُ»¯خïµؤث®»¯خï¼îذش×îا؟µؤتاNaOH£¬ثلذش×îا؟µؤتاHClO4£¬³تء½ذشµؤتاAl(OH)3،£
£¨3£©·ا½ًتôذشش½ا؟£¬ا⻯خïµؤخب¶¨ذشش½ا؟£¬زٍ´ثا⻯خï×îخب¶¨µؤتاHF،£
£¨4£©ح¬ز»ض÷×هشھثط´سةدµ½دآش×س°ë¾¶ضً½¥شِ´َ£¬ح¬ضـئع×ش×َدٍسز£¬ش×س°ë¾¶ضً½¥¼ُذ،£¬ثùزششعB،¢C،¢E،¢F،¢G،¢Hضذ£¬ش×س°ë¾¶×î´َµؤتاNa،£
£¨5£©A؛حD×é³ة»¯؛دخïتا¼×ح飬؛¬سذ¼«ذش¼üµؤ¹²¼غ»¯؛دخئنµç×ست½خھ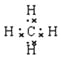 ،£
،£
£¨6£©A؛حE×é³ة»¯؛دخïµؤ»¯ر§ت½تاNH3،£
£¨7£©B؛حH×é³ة»¯؛دخïآب»¯ؤئ£¬ئنذخ³ة¹³ج؟ة±يت¾خھ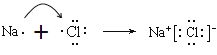 ،£
،£
£¨8£©اâرُ»¯آءتاء½ذشاâرُ»¯خؤـ؛حاâرُ»¯ؤئبـز؛·´س¦£¬شٍBµؤ×î¸ك¼غرُ»¯خïµؤث®»¯خï؛حCµؤ×î¸ك¼غرُ»¯خïد໥·´س¦µؤہë×س·½³جت½Al£¨OH£©3 + OH،ھ£½ AlO2،ھ + 2H2O،£


 شؤ¶ء؟ى³µدµءذ´ً°¸
شؤ¶ء؟ى³µدµءذ´ً°¸
| ؤ꼶 | ¸كضذ؟خ³ج | ؤ꼶 | ³ُضذ؟خ³ج |
| ¸كز» | ¸كز»أâ·ر؟خ³جحئ¼ِ£، | ³ُز» | ³ُز»أâ·ر؟خ³جحئ¼ِ£، |
| ¸ك¶ | ¸ك¶أâ·ر؟خ³جحئ¼ِ£، | ³ُ¶ | ³ُ¶أâ·ر؟خ³جحئ¼ِ£، |
| ¸كب | ¸كبأâ·ر؟خ³جحئ¼ِ£، | ³ُب | ³ُبأâ·ر؟خ³جحئ¼ِ£، |
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟»ط´ًثل¼îµخ¶¨تµرéضذµؤدآءذختجâ£؛ 
£¨1£©دآءذسذ¹طµخ¶¨²ظ×÷µؤث³ذٍصب·µؤتا£» ¢ظ¼ى²éµخ¶¨¹ـتا·ٌآ©ث® ¢عسأصôءَث®د´µس²£ء§زائ÷ ¢غسأ±ê×¼بـز؛بَد´ت¢±ê×¼بـز؛µؤµخ¶¨¹ـ£¬سأ´²âز؛بَد´ت¢´²âز؛µؤµخ¶¨¹ـ ¢ـµخ¶¨²ظ×÷ ¢ف×°±ê×¼بـز؛؛ح´²âز؛²¢µ÷صûز؛أو£¨¼اآ¼³ُت¼¶ءت£© ¢قب،ز»¶¨جه»µؤ´²âز؛سع׶ذخئ؟ضذ
A.¢ظ¢غ¢ع¢ـ¢ف¢ق
B.¢ظ¢ع¢غ¢ف¢ق¢ـ
C.¢ع¢غ¢ظ¢ـ¢ف¢ق
D.¢ـ¢ف¢ظ¢ع¢غ¢ق
£¨2£©بçح¼1±يت¾10 mLء؟ح²ضذز؛أوµؤخ»ضأ£¬AسëB،¢BسëC؟ج¶ب¼ندà²î1mL£¬بç¹û؟ج¶بAخھ4£¬ء؟ح²ضذز؛جهµؤجه»تاmL£®
£¨3£©بçح¼2±يت¾25.00mLµخ¶¨¹ـضذز؛أوµؤخ»ضأ£¬بç¹ûز؛أو´¦µؤ¶ءتتاa£¬شٍµخ¶¨¹ـضذز؛جهµؤجه»£¨جî´ْ؛إ£© £®
A.a mL
B.£¨25©پa£© mL
C.´َسعa mL
D.´َسع£¨25©پa£©mL
£¨4£©ح¼3خھسأز»±ê×¼إ¨¶بNaOHبـز؛µخ¶¨20.00mLخ´ضھإ¨¶بµؤرخثلت±µؤµخ¶¨اْدك£®شٍء½ضضبـز؛µؤخïضتµؤء؟إ¨¶ب·ض±ًتا£؛c£¨HCl£©= £¬ c£¨NaOH£©= £®
£¨5£©µخ¶¨¹³جضذ£¬دآءذ²ظ×÷ضذ»لت¹²â¶¨½ل¹ûئ«µحµؤسذ
A.ثلت½µخ¶¨¹ـخ´بَد´
B.׶ذخئ؟ؤعسذةظء؟ث®
C.µخ¶¨ا°£¬µخ¶¨¹ـ¼â×ى²؟·ضسذئّإف£¬µخ¶¨؛َئّإفدûت§
D.µخ¶¨ا°رِتسµخ¶¨¹ـ¶ءت£¬µخ¶¨؛َئ½تس؟ج¶ب¶ءت£®
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟دآءذ¹³جذèزھح¨µç؛َ²إ؟ةزش·¢ةْ»ٍ½ّذذµؤتا( )
¢ظµçہë ¢عµçس¾ ¢غµç½â ¢ـµç¶ئ ¢فµç»¯ر§¸¯ت´
A. ¢ظ¢ع B. ¢ع¢غ¢ـ
C. ¢ع¢غ¢ـ¢ف D. ب«²؟
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟ؤ³ز»¶àëؤء´ضذ²¢سذëؤ¼ü151¸ِ£¬شٍ´ث·ض×سضذضءةظ؛¬¶àةظ¸ِسخہëµؤôب»ù؛ح°±»ù
A. 152 152 B. 151 151 C. 1 1 D. 2 2
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟£¨1£©ؤ³ئّج¬جµؤؤ¦¶ûضتء؟خھ16g/mol,¸أجضذاâشھثطµؤضتء؟·ضتخھ25% £¬شٍ¸أجµؤ·ض×ست½خھ_______________½ل¹¹ت½خھ________ £¬؟ص¼ن¹¹ذحخھ__________ £¬شع¹âصصجُ¼دآ¸أج؛حآبئّ·´س¦ةْ³ةئّج¬سذ»ْخïµؤ·´س¦·½³جت½خھ___________________________________________ £¬·´س¦ہàذحخھ _________
£¨2£©»¯ر§ت½خھC8Hmµؤحéج£¬mضµµبسع______£»CnH22µؤحéج£¬nضµµبسع_______£»دà¶ش·ض×سضتء؟خھ212µؤحéجµؤ·ض×ست½خھ___________،£
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟îض¼°ئن»¯؛دخï¾كسذذي¶àسإء¼µؤذشؤـ£¬شعسî؛½،¢µç×س،¢³¬µ¼µب·½أوسذ×إ¹م·؛µؤس¦سأ،£´سîر°×¹¤زµ·دثل£¨؛¬îض،¢îر،¢جْ،¢أجµبہë×س£©ضذجلب،رُ»¯îض£¨Sc2O3£©µؤز»ضضء÷³جبçدآ£؛
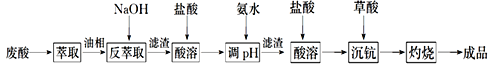
»ط´ًدآءذختجâ£؛
£¨l£©د´µس،°سحدà،±؟ة³ب¥´َء؟µؤîرہë×س،£د´µسث®تاسأ93%µؤءٍثل،¢27.5%µؤث«رُث®؛حث®°´ز»¶¨±بہ»ى؛د¶ّ³ة،£»ى؛دµؤتµرé²ظ×÷تا__________،£
£¨2£©دب¼سبë°±ث®µ÷½عpH =3£¬¹آث£¬آثشüض÷زھ³ة·ضتا_______£»شظدٍآثز؛¼سبë°±ث®µ÷½عpH=6£¬آثز؛ضذSc3+µؤإ¨¶بخھ________،£[¼؛ضھ£؛Ksp[Mn(OH)2]=1.9،ء10-13،¢Ksp[Fe(OH)3]=2.6،ء10-39£¬Ksp[Sc(OH)3]=9.0،ء10-31]
£¨3£©سأ²فثل،°³ءîض،±،£25،وت±pH=2µؤ²فثلبـز؛ضذ![]() =_______£¨±£ءôء½خ»سذذ§ت×ض£©،£ذ´³ِ،°³ءîض،±µأµ½²فثلîضµؤہë×س·½³جت½_________،£
=_______£¨±£ءôء½خ»سذذ§ت×ض£©،£ذ´³ِ،°³ءîض،±µأµ½²فثلîضµؤہë×س·½³جت½_________،£
£¨زرضھKal(H2C2O4)=5.9،ء10-2£¬Ka2(H2C2O4)=6.4،ء10-5£©
£¨4£©²فثلîض،°×ئةص،±رُ»¯µؤ»¯ر§·½³جت½خھ_____________،£
£¨5£©·دثلضذ؛¬îضء؟خھ15mg/L£¬V L·دثل×î¶à؟ةجلب،Sc2O3µؤضتء؟خھ____________،£
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟ث®µ¾؟ة´سحءبہضذخüتصNH4+£¬ئنضذµؤNشھثط؟ةسأہ´؛د³ة
A. µي·غ؛حدثخ¬ثط B. µ°°×ضت؛ح؛ثثل C. ض¬·¾؛حDNA D. آَر؟جا؛حء×ض¬
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟ؤ³»¯ر§ذثب¤ذ،×éخھءثج½¾؟آءµç¼«شعµç³طضذµؤ×÷سأ£¬ةè¼ئ²¢½ّذذءثزشدآز»دµءذتµر飬تµرé½ل¹û¼اآ¼بçدآ±ي£؛
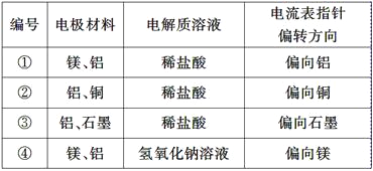
تش¸ù¾ف±يضذµؤتµرéدضدَحê³ةدآءذختجâ£؛
(1)تµرé¢ظ،¢¢عضذآءثù×÷µؤµç¼«(ض¸ص¼«»ٍ¸؛¼«)________(جî،°دàح¬،±»ٍ،°²»دàح¬،±)،£
(2)تµرé¢غضذآءخھ________¼«£¬µç¼«·´س¦ت½خھ_________________________________________£»ت¯ؤ«خھ________¼«£¬µç¼«·´س¦ت½خھ______________£»µç³ط×ـ·´س¦ت½خھ____________________،£
(3)تµرé¢ـضذآء×÷¸؛¼«»¹تاص¼«£؟____________£¬ہيسةتا_________________________£¬آءµç¼«µؤµç¼«·´س¦ت½خھ__________________________________________________________،£
(4)¸ù¾فتµرé½ل¹û×ـ½ل³ِس°دىآءشعشµç³طضذ×÷ص¼«»ٍ¸؛¼«µؤزٍثطخھ______________________،£
²é؟´´ً°¸؛ح½âخِ>>
؟ئؤ؟£؛¸كضذ»¯ر§ ہ´ش´£؛ جâذح£؛
،¾جâؤ؟،؟دآءذسذ¹طجاہà،¢سحض¬؛حµ°°×ضتµؤثµ·¨صب·µؤتا
A. سحض¬ببء؟¸ك£¬شعةْخïجهجهؤعح¨¹رُ»¯جل¹©ؤـء؟
B. ´س»ى؛دخïضذ·ضہëجل´؟µ°°×ضت؟ة²ةسأ¹آثµؤ·½·¨
C. µي·غ،¢سحض¬؛حµ°°×ضت¶¼ؤـشعNaOHبـز؛ضذ·¢ةْث®½â
D. صلجا¼°ئنث®½â²ْخﶼؤـ·¢ةْزّ¾µ·´س¦
²é؟´´ً°¸؛ح½âخِ>>
°ظ¶بضآذإ - ء·د°²لءذ±ي - تشجâءذ±ي
؛±±ت،»¥ءھحّخ¥·¨؛ح²»ء¼ذإد¢¾ظ±¨ئ½ج¨ | حّةدسذ؛¦ذإد¢¾ظ±¨×¨اّ | µçذإص©ئ¾ظ±¨×¨اّ | ةوہْت·ذéخقض÷زهسذ؛¦ذإد¢¾ظ±¨×¨اّ | ةوئَاضب¨¾ظ±¨×¨اّ
خ¥·¨؛ح²»ء¼ذإد¢¾ظ±¨µç»°£؛027-86699610 ¾ظ±¨ستدن£؛58377363@163.com