
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
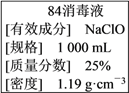
(1)消毒液”的物质的量浓度约为______ mol·L-1。
(2)某同学取100 mL 该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=________ mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下列说法正确的是________(填字母)。
A.如图所示的仪器中,有三种是不需要的,还需要一种玻璃仪器
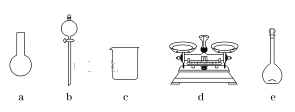
B.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制
C.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低
D.需要称量NaClO固体的质量为143.0 g
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制2 000 mL 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为________ mol·L-1。
②需用浓硫酸的体积为________ mL。
【答案】 4.0 0.04 C 4.6 250
【解析】(1)由c=![]() 得,c(NaClO)=
得,c(NaClO)=![]() ≈4.0(mol·L-1)。
≈4.0(mol·L-1)。
(2)稀释前后溶液中NaClO的物质的量不变,则有:100 mL×10-3L·mL-1×4.0 mol·L-1=100 mL×100×10-3L·mL-1×c(NaClO),解得稀释后c(NaClO)=0.04 mol·L-1,c(Na+)=c(NaClO)=0.04 mol·L-1。(3)选项A,需用托盘天平称量NaClO固体,需用烧杯来溶解NaClO,需用玻璃棒进行搅拌和引流,需用容量瓶和胶头滴管来定容,图示的A、B不需要,但还需玻璃棒和胶头滴管。选项B,配制过程中需要加入水,所以经洗涤干净的容量瓶不必烘干后再使用。选项C,未洗涤烧杯和玻璃棒将导致配制的溶液中溶质的物质的量减小,结果偏低。选项D,应选取500 mL的容量瓶进行配制,然后取出480 mL即可,所以需要NaClO的质量:0.5 L×4.0 mol·L-1×74.5 g·mol-1=149.0 g。(4)①根据H2SO4的组成可知,溶液中c(H+)=2c(H2SO4)=4.6 mol·L-1。②2 000 mL 2.3 mol·L-1的稀硫酸中溶质的物质的量为2 L×2.3 mol·L-1=4.6 mol,设需要98%(密度为1.84 g·cm-3)的浓硫酸的体积为V mL,则有: ![]() =4.6 mol,解得V=250。
=4.6 mol,解得V=250。


科目:高中化学 来源: 题型:
【题目】鲨鱼是世界上惟一不患癌症的动物,科学研究表明,鲨鱼体内含有一种角鲨烯,具有抗癌性.。已知角鲨烯分子中含有30个碳原子及6个C=C且不含环状结构,则其分子式为
A. C30H60B. C30H56C. C30H52D. C30H50
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物M的结构简式为CH3CH=CHCH2COOH,下列有关说法正确的是( )
A. 能与乙醇发生酯化反应
B. 不能使酸性高锰酸钾溶液褪色
C. 能与溴的四氯化碳溶液发生取代反应
D. 1 mol M与足量Na完全反应能生成1 mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应一定属于放热反应的是
A. 氢氧化钡晶体和氯化铵晶体的反应
B. 反应物能量比生成物能量低的反应
C. 化学键断裂吸收的能量比化学键形成放出的能量少的反应
D. 不需要加热就能发生的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用下列方法测定某水样中O2的含量。

(1)实验原理
①用如图所示装置,使溶解在水中的O2在碱性条件下将Mn2+氧化成MnO(OH)2,反应的离子方程式为_____________________________。
②在酸性条件下,再用I-将生成的MnO(OH)2,还原为Mn2+,反应的离子方程式为_____________________________。然后用Na2S2O3标准溶液滴定生成的I2,反应方程式为I2+2 Na2S2O3=2Na1+Na2S4O6。
(2)实验步骤
①打开止水夹a和b,从A处向装置内鼓入过量N2,此操作的目的是___________________________;
②用注射器抽取某水样20. 00mL从A处注入锥形瓶;
③再分别从A处注入含m mol NaOH溶液及过量的MnSO4溶液;
④完成上述操作后,关闭a、b,将锥形瓶中溶液充分振荡;
⑤打开止水夹a、b,分别从A处注入足量NaI溶液及含n mol H2SO4的硫酸;
⑥重复④的操作;
⑦取下锥形瓶,向其中加入23滴_______作指示剂;
⑧用0.005 mol L -1 Na2S2O3溶液滴定至终点。滴定终点的现象是___________________________。
(3)数据分析
①若滴定过程中消耗的Na2S2O3标准溶液体积为3.90 mL,则此水样中氧(O2)的含量为________ mg L-1。
②若未用Na2S2O3标准溶液润洗滴定管,则测得水样中O2的含量将_________ (填“偏大”“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在水溶液中能大量共存的是( )
A.H+、Fe2+、NO3-、Cl-B.S-、Na+、H+、K+
C.K+、CO32-、Br-、AlO2-D.H+、Cl-、Na+、S2O32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式碳酸铝镁[MgaAlb(OH)c(CO3)dxH2O]常用作塑料阻燃剂. 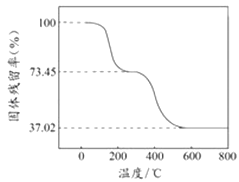
(1)碱式碳酸铝镁具有阻燃作用,是由于其受热分解需吸收大量热量和 .
(2)[MgaAlb(OH)c(CO3)dxH2O]中的a、b、c、d的代数关系式为 .
(3)为确定碱式碳酸铝镁的组成,进行如下实验:
①准确称取3.390g样品与足量稀盐酸充分反应,生成CO2 0.560L(已换算成标准状况下).
②另取一定量样品在空气中加热,样品的固体残留率( ![]() ×100%)随温度的变化如图所示(样品在270℃时已完全失去结晶水,600℃以上残留固体为金属氧化物的混合物).
×100%)随温度的变化如图所示(样品在270℃时已完全失去结晶水,600℃以上残留固体为金属氧化物的混合物).
根据以上实验数据计算碱式碳酸铝镁样品中的n(OH﹣):n(CO32﹣)(写出计算过程).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】归纳法是高中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结:归纳正确的是( ) ①向0.1molL﹣1 CH3COOH溶液中加入少量冰醋酸,平衡向正反应方向移动,电离程度增大;②常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则有c(Na+)+c(H+)=c(OH﹣)+c(CH3COO﹣)
③常温下,AgCl在同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同;④常温下,已知醋酸电离平衡常数为Ka;醋酸根水解平衡常数为Kh;水的离子积为Kw;则有:KaKh=Kw .
A.①②④
B.②④
C.②③
D.①②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com