
| Va |
| Vb |
| Va |
| Vb |
| Va |
| Vb |
| Va |
| Vb |
| Va |
| Vb |


科目:高中化学 来源: 题型:
| 热化学方程式 | △H大小比较 | |||
| A | S(g)+O2(g)=SO2(g)△H1 | △H1>△H2 | ||
| S(s)+O2(g)=SO2(g)△H2 | ||||
| B | 2H2(g)+O2(g)=2H2O(1)△H1 | △H1<△H2 | ||
| 2H2(g)+O2(g)=2H2O(g)△H2 | ||||
| C | CH3COOH(aq)+NaOH(aq)=CH3COOHNa(aq)+H2O(1)△H1 | △H1<△H2 | ||
| HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(1)△H2 | ||||
| D | 2Na(s)+
| △H1>△H2 | ||
| 2Na(s)+O2(g)=Na2O2 △H2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
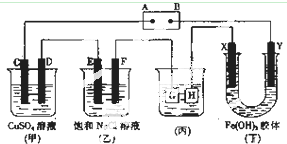 如图所示的装置,C、D、E、F、X、Y都是惰性电极.将电源接通后,向乙中滴入酚酞液,在F极附近显红色.
如图所示的装置,C、D、E、F、X、Y都是惰性电极.将电源接通后,向乙中滴入酚酞液,在F极附近显红色.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 降低温度 | 充入SO3气体 | 增大压强 | 加入正催化剂 |
| 降低温度 | 充入SO3气体 | 增大压强 | 加入正催化剂 |
| 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用排饱和食盐水的方法收集氯气 |
| B、合成氨工业选择高温 |
| C、增大压强,有利于SO2和O2反应生成SO3 |
| D、在Fe3++3SCN -?Fe(SCN)3反应达平衡时,增加KSCN的浓度,体系颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | |
| 弱电解质 | HBr | CH3COOH | HF | Ca(OH)2 |
| 强电解质 | H3PO4 | FeCl3 | BaSO4 | HI |
| 非电解质 | CCl4 | Cu | C2H5OH | H2O |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在图中A和B两容器里,分别收集着两种互不作用的理想气体.若将中间活塞打开(如图所示),两种气体分子立即都分布在两个容器中.这是一个不伴随能量变化的自发过程.关于此过程的下列说法错误的是( )
在图中A和B两容器里,分别收集着两种互不作用的理想气体.若将中间活塞打开(如图所示),两种气体分子立即都分布在两个容器中.这是一个不伴随能量变化的自发过程.关于此过程的下列说法错误的是( )| A、此过程为混乱程度小的向混乱程度大的方向的变化过程,即熵增大的过程 |
| B、此过程为自发过程,而且没有热量的吸收或放出 |
| C、此过程从有序到无序,混乱度增大 |
| D、此过程是自发可逆的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com