
【题目】相同体积、相同pH的某一元强酸溶液①和某一元弱酸溶液②分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是( )
A.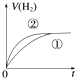
B.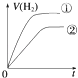
C.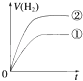
D.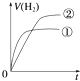
【答案】C
【解析】因为强酸完全电离,一元弱酸部分电离,因此要有相同的PH值,一元弱酸的浓度必须比强酸高,由于体积相等,因此一元弱酸的物质的量大于强酸,因此产生的H2也比强酸多.反应过程由于H+不断被消耗掉,促使一元弱酸继续电离,这就延缓了H+浓度下降的速率,而强酸没有H+的补充途径,浓度下降的更快,由于其他条件都相同,反应速率取决于H+浓度,由于开始时H+浓度相等,因此反应速率也相等(在图中反应速率就是斜率),后面强酸的反应速率下降得快,斜率也就更小,曲线更平坦.最终生成H2的体积也比一元弱酸少,因此曲线在一元弱酸下面;所以选C.
【考点精析】掌握弱电解质在水溶液中的电离平衡是解答本题的根本,需要知道当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列反应既属于氧化还原反应,又是吸热反应的是:
A.锌粒与稀硫酸的反应B.灼热的木炭与CO2的反应
C.甲烷在空气中燃烧的反应D.Ba(OH)28H2O晶体与NH4Cl晶体的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.60 g SiO2晶体中含有Si﹣O键数目为2NA
B.常温常压下,1.6 9 O2和O3的混合气体所含电子数为0.8NA
C.1 mol/L AICl3溶液中,所含Al3+数目小于NA
D.密闭容器中2 mol NO与l mol 02充分反应,产物的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.分子式为C7H16的烷烃,含有3个甲基的同分异构体有2种
B.丙烯能发生取代反应、加成反应,还能使酸性KMnO4溶液褪色
C.甲苯中所有原子都处于同一平面
D.相同质量的甲烷和乙烷完全燃烧乙烷耗氧量多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关浓硫酸说法中错误的是()
A. 浓硫酸具有吸水性,可用于干燥某些气体B. 浓硫酸具有脱水性,可以使纸张碳化
C. 浓硫酸具有酸性,可与铜反应生成氢气D. 浓硫酸具有强氧化性,常温下可以使铝片发生钝化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列实验所选择的装置或仪器不正确的是( )
A | B | C | D | |
实 验 | 实验分离水和酒精 | 用铵盐和碱制取氨气 | 用排空气法收集二氧化氮 | 用自来水制取蒸馏水 |
装置或仪器 |
|
|
|
|
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在①二氧化碳②二氧化硫③氟氯烃中,造成酸雨的主要因素是______含量的增加;全球气候变暖是由于______含量的急剧增加;造成臭氧空洞的主要物质是______(以上均要求填序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温时,0.1mol/L某一元酸HA在水中有0.1%发生电离,回答下列问题:
(1)该溶液中c(H+)= .
(2)HA的电离平衡常数K=;
(3)升高温度时,K(填“增大”,“减小”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,一密闭容器被无摩擦、可滑动的两隔板a、b分成甲、乙两室;标准状况下,在乙室中充入NH3 0.4mol,甲室中充入HCl、N2的混合气体,静止时隔板位置如图所示.已知甲、乙两室中气体的质量差为17.3g.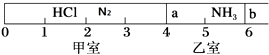
(1)甲室中气体的质量为 .
(2)甲室中HCl、N2的物质的量之比为 .
(3)将隔板a去掉,当HCl与NH3充分反应生成NH4Cl固体后(仅发生此反应),隔板b将位于刻度“”处(填数字,不考虑固体物质产生的压强),此时体系的平均摩尔质量 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com